CPIC 指南註解:mercaptopurine 與 NUDT15、TPMT 基因
摘要
對於TPMT或NUDT15 弱代謝型(Poor metabolizer)的患者,考慮使用替代藥物或極端減少mercaptopurine的劑量。對於中間代謝型(Intermediate metabolizer)的患者,無論是TPMT或NUDT15,應從目標劑量的30-80%開始。對於中間代謝型(Intermediate metabolizer)的患者,同時具有TPMT和NUDT15,應從目標劑量的20-50%開始。該指導方針自原始發佈以來已更新。請參閱指導方針註釋以獲取更多信息。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC® 關於硫嘌呤和TPMT及NUDT15的指引。
2024年2月更新
CPIC已更新對於中間代謝型(Intermediate metabolizer)的患者的建議,這些患者同時是TPMT和NUDT15的中間代謝型(Intermediate metabolizer)或可能為中間代謝型(Possible intermediate metabolizer)。建議這些患者以正常劑量的20-50%開始。基因型選擇工具中的建議和此註釋頁面已相應更新。
2018年10月更新
2018年11月在線提前發表。
- 2018年CPIC關於azathioprine、thioguanine和mercaptopurine的指引更新已發表於《Clinical Pharmacology and Therapeutics》期刊。審查了2012年10月至2017年6月間發表的文獻,更新了建議和補充信息。
- 這些指引適用於:
- 兒科患者
- 成人患者
- 2018年硫嘌呤劑量指引更新摘錄:
- 「TPMT活性表現為單基因共顯性遺傳,並催化硫嘌呤。TPMT變異等位基因與低酶活性和硫嘌呤的顯著藥理效應相關。」
- 「NUDT15基因中的功能缺失等位基因在亞洲人和西班牙裔中常見,並減少活性硫嘌呤核苷酸代謝物的降解,也使其易於骨髓抑制。」
- 下載並閱讀:
表1:根據TPMT 表現型推薦的mercaptopurine劑量
改編自2018年指引更新的表1和表2。
| TPMT 表現型 | 基因型 | 雙倍型的例子 | 影響 | 劑量建議 | 建議等級 |
|---|---|---|---|---|---|
| 正常代謝型(Normal metabolizer) | 攜帶兩個功能正常 等位基因的個體 | *1/*1 | TGN代謝物濃度較低,meTIMP較高,這是「正常」模式。thiopurine相關 白血球減少、嗜中性白血球低下症、骨髓抑制的正常風險。 | 以正常起始劑量開始a(例如,75 mg/m2/天或1.5 mg/kg/天),並調整mercaptopurine(及任何其他骨髓抑制療法)的劑量,無需特別強調mercaptopurine相較於其他藥物。每次劑量調整後至少需2週達到穩定狀態。 | 強烈建議 |
| 中間代謝型(Intermediate metabolizer) | 攜帶一個功能正常 等位基因和一個功能缺失 等位基因的個體 | *1/*2, *1/*3A, *1/*3B, *1/*3C, *1/*4 | 中等建議至高濃度的TGN代謝物;meTIMP濃度低。thiopurine相關 白血球減少、嗜中性白血球低下症、骨髓抑制的風險增加。 | 如果正常起始劑量a大於或等於75 mg/m2/天或大於或等於1.5 mg/kg/天,則以減少的起始劑量(正常劑量的30-80%)開始(例如,開始於25-60 mg/m2/天或0.45-1.2 mg/kg/天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需2-4週達到穩定狀態。如果發生骨髓抑制,並根據其他療法,應強調減少mercaptopurine而非其他藥物。如果正常起始劑量已低於75 mg/m2/天或低於1.5 mg/kg/天,可能不建議減少劑量。 | 強烈建議 |
| 可能為中間代謝型(Possible intermediate metabolizer) | 攜帶一個不確定/功能未知 等位基因和一個功能缺失 等位基因的個體 | *2/*8, *3A/*7 | 中等建議至高濃度的TGN代謝物;meTIMP濃度低。thiopurine相關 白血球減少、嗜中性白血球低下症、骨髓抑制的風險增加。 | 如果正常起始劑量a大於或等於75 mg/m2/天或大於或等於1.5 mg/kg/天,則以減少的起始劑量(正常劑量的30-80%)開始(例如,開始於25-60 mg/m2/天或0.45-1.2 mg/kg/天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需2-4週達到穩定狀態。如果發生骨髓抑制,並根據其他療法,應強調減少mercaptopurine而非其他藥物。如果正常起始劑量已低於75 mg/m2/天或低於1.5 mg/kg/天,可能不建議減少劑量。 | 強烈建議 |
| 弱代謝型(Poor metabolizer) | 攜帶兩個功能缺失 等位基因的個體 | *3A/*3A, *2/*3A, *3A/*3C, *3C/*4, *2/*3C, *3A/*4 | TGN代謝物濃度極高;若不減少劑量,可能發生致命毒性;無meTIMP代謝物 | 對於惡性nan,以大幅減少的劑量開始(將每日劑量a減少10倍,並將頻率從每日改為每週三次,例如,10 mg/m2/天僅給予每週3天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需4-6週達到穩定狀態。如果發生骨髓抑制,應強調減少mercaptopurine而非其他藥物。對於非惡性nan情況,考慮使用非硫嘌呤免疫抑制療法。 | 強烈建議 |
| 無法判定 | 攜帶兩個不確定/功能未知 等位基因或一個功能正常 等位基因和一個不確定/功能未知 等位基因的個體 | *6/*8, *1/*8 | 無 | 無 | 無 |
| a正常起始劑量因種族/族裔和治療方案而異。如果標準劑量低於正常推薦劑量,可能不建議對中間代謝型(Intermediate metabolizer)進行劑量減少。 |
表2:根據NUDT15 表現型推薦的mercaptopurine劑量
改編自2018年指引更新的表1和表2。
| NUDT15 表現型 | 基因型 | 雙倍型的例子 | 影響 | 劑量建議 | 建議等級 |
|---|---|---|---|---|---|
| 正常代謝型(Normal metabolizer) | 攜帶兩個功能正常 等位基因的個體 | *1/*1 | thiopurine相關 白血球減少、嗜中性白血球低下症、骨髓抑制的正常風險 | 以正常起始劑量開始a(例如,75 mg/m2/天或1.5 mg/kg/天),並調整mercaptopurine(及任何其他骨髓抑制療法)的劑量,無需特別強調mercaptopurine相較於其他藥物。每次劑量調整後至少需2週達到穩定狀態。 | 強烈建議 |
| 中間代謝型(Intermediate metabolizer) | 攜帶一個功能正常 等位基因和一個功能缺失 等位基因的個體 | *1/*2, *1/*3 | thiopurine相關 白血球減少、嗜中性白血球低下症、骨髓抑制的風險增加。 | 如果正常起始劑量a大於或等於75 mg/m2/天或大於或等於1.5 mg/kg/天,則以減少的起始劑量(正常劑量的30-80%)開始(例如,開始於25-60 mg/m2/天或0.45-1.2 mg/kg/天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需2-4週達到穩定狀態。如果發生骨髓抑制,並根據其他療法,應強調減少mercaptopurine而非其他藥物。如果正常起始劑量已低於75 mg/m2/天或1.5 mg/kg/天,可能不建議減少劑量。 | 強烈建議 |
| 可能為中間代謝型(Possible intermediate metabolizer) | 攜帶一個功能尚未確定 等位基因和一個功能缺失 等位基因的個體 | *2/*5, *3/*6 | thiopurine相關 白血球減少、嗜中性白血球低下症、骨髓抑制的風險增加。 | 如果正常起始劑量a大於或等於75 mg/m2/天或大於或等於1.5 mg/kg/天,則以減少的起始劑量(正常劑量的30-80%)開始(例如,開始於25-60 mg/m2/天或0.45-1.2 mg/kg/天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需2-4週達到穩定狀態。如果發生骨髓抑制,並根據其他療法,應強調減少mercaptopurine而非其他藥物。如果正常起始劑量已低於75 mg/m2/天或1.5 mg/kg/天,可能不建議減少劑量。 | 強烈建議 |
| 弱代謝型(Poor metabolizer) | 攜帶兩個功能缺失 等位基因的個體 | *2/*2, *2/*3, *3/*3 | thiopurine相關 白血球減少、嗜中性白血球低下症、骨髓抑制的風險大幅增加 | 對於惡性nan,以10 mg/m2/天開始劑量,並根據骨髓抑制和疾病別指引調整劑量。每次劑量調整後需4-6週達到穩定狀態(Steady state)。如果發生骨髓抑制,應強調減少mercaptopurine而非其他藥物。對於非惡性nan情況,考慮使用非硫嘌呤免疫抑制療法。 | 強烈建議 |
| 無法判定 | 攜帶兩個功能尚未確定 等位基因或一個功能正常 等位基因和一個功能尚未確定 等位基因的個體 | *1/*4, *1/*5, *4/*5, *5/*6 | 無 | 無 | 無 |
| a正常起始劑量因種族/族裔和治療方案而異。如果標準劑量低於正常推薦劑量,可能不建議對中間代謝型(Intermediate metabolizer)進行劑量減少。 |
表3:根據TPMT和NUDT15 表現型推薦的mercaptopurine劑量
改編自2018年指引更新的圖2和表2。
| 表現型 | TPMT 正常代謝型(Normal metabolizer) | TPMT 中間代謝型(Intermediate metabolizer) | TPMT 可能為中間代謝型(Possible intermediate metabolizer) | TPMT 弱代謝型(Poor metabolizer) | 無法判定 |
|---|---|---|---|---|---|
| NUDT 15 正常代謝型(Normal metabolizer) | 使用標準劑量 | 如果正常起始劑量大於或等於75 mg/m2/天或大於或等於1.5 mg/kg/天,則以減少的起始劑量(正常劑量的20%-50%)開始(例如,開始於15-37.5 mg/m2/天或0.3-0.75 mg/kg/天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後至少需2-4週達到穩定狀態。如果發生骨髓抑制,並根據其他療法,應強調減少mercaptopurine而非其他藥物(PMID 20354201,18685564, 8857546, 18987654, 20010622, 16401827, 11302950, 16530532, 9634537, 38230823)。如果正常起始劑量已低於37.5 mg/m2/天或低於0.75 mg/kg/天,可能不建議減少劑量。 | 參見TPMT 中間代謝型(Intermediate metabolizer)/NUDT15 中間代謝型(Intermediate metabolizer)。 | 對於惡性nan,以大幅減少的劑量開始(將每日劑量a減少10倍,並將頻率從每日改為每週三次,例如,10 mg/m2/天僅給予每週3天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需4-6週達到穩定狀態。如果發生骨髓抑制,應強調減少mercaptopurine而非其他藥物。對於非惡性nan情況,考慮使用非硫嘌呤免疫抑制療法。 | 無 |
| NUDT15 中間代謝型(Intermediate metabolizer) | 如果正常起始劑量a大於或等於75 mg/m2/天或大於或等於1.5 mg/kg/天,則以減少的起始劑量(正常劑量的30-80%)開始(例如,開始於25-60 mg/m2/天或0.45-1.2 mg/kg/天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需2-4週達到穩定狀態。如果發生骨髓抑制,並根據其他療法,應強調減少mercaptopurine而非其他藥物。如果正常起始劑量已低於75 mg/m2/天或1.5 mg/kg/天,可能不建議減少劑量。 | 參見TPMT 中間代謝型(Intermediate metabolizer)/NUDT15 中間代謝型(Intermediate metabolizer)。 | 參見TPMT 中間代謝型(Intermediate metabolizer)/NUDT15 中間代謝型(Intermediate metabolizer)。 | 對於惡性nan,以大幅減少的劑量開始(將每日劑量a減少10倍,並將頻率從每日改為每週三次,例如,10 mg/m2/天僅給予每週3天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需4-6週達到穩定狀態。如果發生骨髓抑制,應強調減少mercaptopurine而非其他藥物。對於非惡性nan情況,考慮使用非硫嘌呤免疫抑制療法。 | 無 |
| NUDT15 可能為中間代謝型(Possible intermediate metabolizer) | 參見NUDT15 中間代謝型(Intermediate metabolizer)。 | 參見NUDT15 中間代謝型(Intermediate metabolizer)。 | 參見TPMT 中間代謝型(Intermediate metabolizer)/NUDT15 中間代謝型(Intermediate metabolizer)。 | 參見NUDT15 中間代謝型(Intermediate metabolizer)。 | 無 |
| NUDT15 Poor Metabolizer | 對於惡性nan,以10 mg/m2/天開始劑量,並根據骨髓抑制和疾病別指引調整劑量。每次劑量調整後需4-6週達到穩定狀態(Steady state)。如果發生骨髓抑制,應強調減少mercaptopurine而非其他藥物。對於非惡性nan情況,考慮使用非硫嘌呤免疫抑制療法。 | 對於惡性nan,以10 mg/m2/天開始劑量,並根據骨髓抑制和疾病別指引調整劑量。每次劑量調整後需4-6週達到穩定狀態(Steady state)。如果發生骨髓抑制,應強調減少mercaptopurine而非其他藥物。對於非惡性nan情況,考慮使用非硫嘌呤免疫抑制療法。 | 參見TPMT 中間代謝型(Intermediate metabolizer)。 | 對於惡性nan,以大幅減少的劑量開始(將每日劑量a減少10倍,並將頻率從每日改為每週三次,例如,10 mg/m2/天僅給予每週3天),並根據骨髓抑制和疾病別指引調整mercaptopurine劑量。每次劑量調整後需4-6週達到穩定狀態。如果發生骨髓抑制,應強調減少mercaptopurine而非其他藥物。對於非惡性nan情況,考慮使用非硫嘌呤免疫抑制療法。 | 無 |
| NUDT15 無法判定 | 無 | 無 | 無 | 無 | 無 |
| a正常起始劑量因種族/族裔和治療方案而異。如果標準劑量低於正常推薦劑量,可能不建議對中間代謝型(Intermediate metabolizer)進行劑量減少。 |
2016年5月更新
多項研究報告指出,攜帶低功能等位基因的NUDT15個體無法耐受通常劑量的硫嘌呤。[文章:25108385, 25624441, 26033531, 26076924, 26405151, 26503813, 26590936, 26735160, 26878724] 這些等位基因在亞洲和西班牙裔中較為常見。[文章:25624441, 26878724] 攜帶兩個低功能等位基因的個體所能耐受的劑量僅為無低功能NUDT15或TPMT 等位基因的個體所能耐受劑量的約10%。[文章:25624441, 26878724] CPIC計劃制定一項指引,以解決NUDT15變異和可能的硫嘌呤劑量建議。
2013年4月更新
2013年1月在線提前發表
- 2013年CPIC關於azathioprine、thioguanine和mercaptopurine的指引更新已發表於《Clinical Pharmacology and Therapeutics》期刊。審查了2010年6月至2012年11月間發表的文獻,並無新證據會改變原始指引。因此,原始發表中的劑量建議仍然在臨床上有效。
- 這些指引適用於:
- 兒科患者
- 成人患者
- 下載並閱讀:
2011年3月
2011年1月在線提前發表。
- 關於azathioprine、thioguanine和mercaptopurine劑量中使用藥物基因組學測試的指引已由臨床藥物基因體學實施聯盟(CPIC)發表於《Clinical Pharmacology and Therapeutics》期刊。
- 2011年硫嘌呤劑量指引摘錄:
- 「硫嘌呤最常用於治療非惡性nan情況,但也是關鍵的抗癌藥物。根據TPMT狀態進行劑量調整的方法可能因臨床指徵和起始劑量的高低而異。我們和其他人主張在開始硫嘌呤療法之前測試TPMT狀態,以便相應調整起始劑量。」
- 下載並閱讀:
Thiopurine 途徑, 藥物動力學/藥效學
概括
非組織特異性 癌細胞 的圖示表示,顯示參與 Thiopurine 代謝和作用的候選基因。
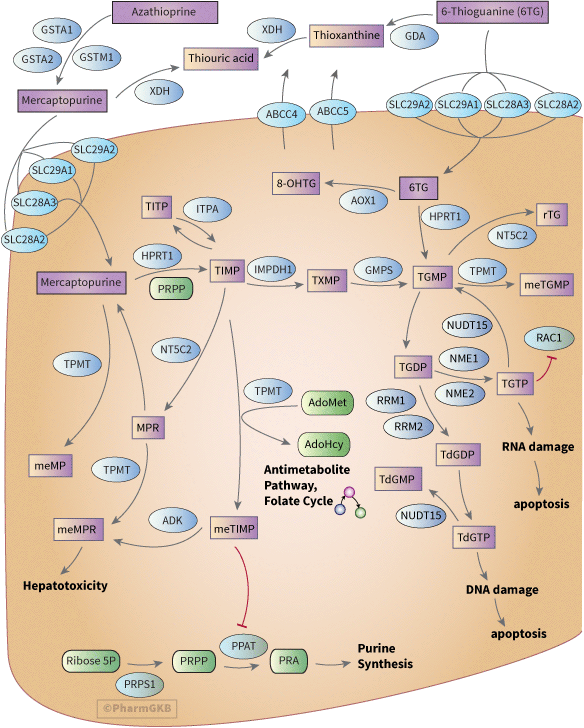
描述
背景
這些 Thiopurine 藥物是嘌呤抗代謝物,廣泛用於治療急性淋巴母細胞白血病、自身免疫疾病(例如克隆病和類風濕性關節炎)以及器官移植受者(詳見 [Articles:16550163、26067482])。它們是最早被研究其藥物基因組學(PGx)反應的藥物之一 [Article:7191632][Article:8644731],也是最早將 PGx 加入藥物 仿單 [Article:17108808] 並獲得臨床 藥物基因體學 實施委員會 (CPIC) [Article:21270794] 的指導方針的藥物之一。Thiopurine 藥物的副作用範圍從輕微的皮疹、類流感症狀到嚴重的危及生命的 骨髓抑制 和肝毒性 [Article:26876431]。在 IBD 人群中,副作用的發生率範圍為 0-39%,在亞洲人群中增加 [Article:18557712]。 Thiopurine 藥物最早於 1950 年代由 Hitchings 和 Elion 開發 [Article:14907641]。構成這篇 途徑 的文獻,即形成的代謝物,追溯至這些時期,通常無法在線上獲得完整文本。這些文獻可以在組件標籤或 Pathvisio 途徑 數據文件中找到,而不是作為本文中的參考。由於本文專注於 Thiopurine 的 PGx 與 途徑 的關係,因此傾向於引用討論涉及過程的候選基因的新文獻,這些文獻通常可以在線上獲得。
藥物動力學
作為不活躍的前藥,6-mercaptopurine (6-MP)、6-thioguanine (6-TG) 和 azathioprine (AZA) 需要細胞內激活,由多種酶催化,以發揮細胞毒性。AZA 激活的第一步是釋放 6-MP。雖然藥物 仿單 提到非酶促轉化,但已發表的體外研究表明,這僅佔 ALL 生物轉化的不到 1% [Article:16717136]。GSTM1、GSTA1 和 GSTA2 能夠在生理相關水平下代謝 AZA [Article:16717136]。雖然 GSTA2 對 AZA 的活性最高,但其表達水平低於 GSTA1 和 GSTM1,因此認為它們對 azathioprine 的生物轉化貢獻在正常表達的個體中將是定量相似的 [Article:16717136]。GSTM1 是一個高度多態的基因,存在無表達(缺失變異)和多個基因拷貝的個體(有關此變異的更多詳細信息請參見 VIP,對於 AZA 特定的 PGx 請見下文)。GSTA3、GSTA4、GSTK1 和 GSTM2 ALL 的活性較低(比 GSTA1 低一個數量級),GSTP1 和 GSTT1 則無活性 [Article:16717136]。 候選的 Thiopurine 輸送進入細胞的運輸蛋白包括 SLC28A2 (CNT2)、SLC28A3 (CNT3)、SLC29A1 (ENT1) 和 SLC29A2 (ENT2) [Articles:17996297、16530731]。對 6-MP 和 6-TG 耐藥的細胞系已下調進口運輸蛋白 [Articles:16530731、17996297、21723252]。耐藥性也可以通過 Thiopurine 和 ABCC4 及 ABCC5 的過度外排來賦予 [Articles:12435799、10840050、17996297]。ABCC4 的變異可以影響對 Thiopurine 的敏感性並影響其毒性(在下文的 PGx 部分進一步討論)[Articles:18593894、20393862]。 在攝取後,6-MP 轉化為 thioinosine monophosphate (TIMP),由 HPRT1 催化,5-磷酸-D-核糖-1-焦磷酸 (PRPP) 作為磷酸核糖供體。以類似的方式,6-TG 可以轉化為 thioguanosine monophosphate (TGMP)。 TGMP 也可以從 TIMP 以兩步驟形成:首先,通過 IMPDH 形成硫黃嘌呤單磷酸 (TXMP);其次,通過 GMPS 形成 TGMP [Article:18662289]。隨後,TGMP 可以轉化為活性代謝物 thioguanine 核苷酸二磷酸 (TGDP) 和三磷酸 (TGTP),並被納入 RNA(見下文的 PD 部分),這是由核苷酸二磷酸激酶 NME1 和 NME2 催化的 [Article:20216118]。TGDP 可以轉化為 TdGDP 並納入 DNA [Article:1157053]。TdGDP 的形成可能是由核糖核苷酸還原酶(由基因 RRM1、RRM2 和 RRM2B 編碼)催化的(在 [Article:[ 中描述但未引用或顯示)])。這些酶通常催化 GDP 轉化為 dGDP,儘管缺乏對其對特定 thioguanine 的作用的直接證據,但 azathioprine 和 RRM1 被記錄為相互作用,這表明 TGDP 與 RRM1 的結合不會被硫醇基團阻礙 [Article:22662200]。 TIMP 可以通過 NT5C2 轉化為 MPR 或通過 TPMT 轉化為甲基 TGMP 或通過 AOX1 轉化為 8-OHTG [Article:10525111]。在一項對接受持續輸注 TG 的小兒白血病患者的研究中,8-OHTG 是主要的循環代謝物 [Article:10525111]。 在 6MP 方面的 途徑 也有分支,導致損傷 RNA 和 DNA 的形成;6MP 被 XDH 氧化形成 thiouric acid(細胞外) [Article:24415675],以及 TPMT(細胞內)的甲基化 [Article:24415675]。TG 也可以形成 thiouric acid,這是一個兩步驟的過程,由鳥嘌呤脫胺酶 GDA 催化,形成 thioxanthine,隨後由 XDH 氧化 [Article:10525111]。
藥效學
Thiopurine 藥物的細胞毒性效應是通過四條途徑實現的:
- 將硫代去氧鳥苷三磷酸 (TdGTP) 納入 DNA
- 將 TGTP 納入 RNA
- 通過 methylmercaptopurine 核苷酸(主要是 meTIMP)抑制新生嘌呤合成 [Article:23811272]
- 通過 RAC1 抑制 TGTP(這種抑制會誘導活化 T 細胞的凋亡) [Article:16365460].
將 TdGTP 納入 DNA 抑制多種參與 DNA 複製和修復的酶的功能。它還誘導 DNA 損傷,例如單鏈斷裂、DNA- 蛋白交聯和染色單體交換 [Articles:6204746、7682415、10606189]。同樣,將 thioguanine 核苷酸 (TGNs) 納入 RNA 也會導致損傷。這種對 RNA 和 DNA 的損傷最終導致細胞毒性和凋亡。
每條 藥效學 子 途徑 的相對量影響 Thiopurine 的療效和毒性。在炎症性疾病中,TGNs 被認為是藥理學上活躍的代謝物,而 meMP [Articles:28130685、22261533]、meMPR 和 6MMPR(甲基 mercaptopurine 核糖核苷酸,包括 meTIMP 和 meTGMP) [Articles:27943397、25853923] 與肝毒性相關。
藥物基因體學
TPMT
在 Thiopurine PGx 的背景下,最廣泛研究的基因是 TPMT。Thiopurine PGx 在 TPMT VIP 中詳細討論,並且關鍵變異的臨床 PGx 信息以及變異註釋可用 單倍型 [Article:20154640]。CPIC 指導方針提供臨床 PGx 信息以及有關 TPMT 等位基因 頻率和在不同種族和民族群體中的分佈的背景數據 [Articles:21270794、23422873]。雖然 同型合子(Homozygous) 的失活變異對 TPMT 相關毒性具有高度預測性(100% 的正預測值) [Article:21270794],但 TPMT 變異相對罕見:在白人群體中約為 5%,在亞洲人群中約為 3%,在黑人群體中約為 6% [Article:23422873],而純合子患者的比例在 1/178 到 1/3,736 之間 [Articles:23422873、21270794]。
其他基因和變異對變異毒性有貢獻:
NUDT15
首次由 GWAS 在 IBD 患者中識別 [Article:25108385],也在急性淋巴母細胞白血病的兒童中發現(PMID 25624441),NUDT15 變異 rs116855232 T 與 thiopurine相關 造血毒性相關。這個候選基因在幾項其他研究中被確認與 Thiopurine 的耐受性和/或 thiopurine相關 毒性相關,無論是在 IBD 還是白血病患者中 [Articles:26878724、26405151、26033531、26503813、26735160、26590936、26076924。T 等位基因 的頻率在 HapMap 人群中範圍為 1-10% ,在 dbSNP] 中顯示。
NUDT15 將活性代謝物 TdGTP 和 TGTP 轉化為無活性的 TdGMP 和 TGMP,從而防止 TdGTP 納入 DNA 和 TGTP 進入 RNA [Article:25624441]。
ITPA
幾項研究已檢查 ITPA 變異在 Thiopurine 代謝、劑量、療效和毒性中的作用;然而,結果有些矛盾,反映了這一 途徑 的複雜性,以及不同分支可能與不同藥物或潛在條件或人群的相關性更大。大多數研究檢查了 94C>A 變異(rs1127354),其在 HapMap 人群中的頻率為 3-10%,在非洲人群中頻率較低,而在亞洲人群中頻率較高 ,詳見 dbSNP。 對小兒白血病患者的 ITPA 研究顯示,ITPA 94A 與血液學或骨髓毒性(白血球減少、嗜中性白血球低下症、貧血)相關 [Article:26237184][Article:18685564],儘管一項針對亞洲患者的研究未見相關性 [Article:26405151]。ITPA 94A 與增加的 methylmercaptopurine 水平相關,這與肝毒性增加的可能性相關 [Article:21395650]。這在沒有 TPMT 變異的患者中最為顯著。該變異對肝毒性的直接影響未明確說明,但研究規模較小 ALL,可能無法檢測到這一點(n=65) [Article:21395650]。 2007 年對 6 項白人成人 IBD 患者的元分析得出結論,認為對於 ITPA 94C>A 預測毒性證據不足。顯示正相關的研究包括一項在荷蘭對接受 azathioprine 的患者(n=262)的研究,其中 A 等位基因 與增加的 白血球減少 可能性相關 [Article:16431304],以及一項來自英國的成人 IBD 患者接受 azathioprine(n=207)的研究,其中 ITPA 94A 與一組類流感症狀相關,但與其他任何 ADR 包括 嗜中性白血球低下症 無關 [Article:18616518]。一項針對日本 IBD 患者的研究表明,94A 可能降低 白血球減少 的風險,94A 與較低的 6-TGNs 相關,但作者未單獨檢查此變異對 白血球減少 的作用,當與 ABCC4 rs3765534 T(該變異對 白血球減少 的風險較高)結合時,結果為中性 [Article:20393862]。 ITPA 的內含子變異 rs7270101 SNP 在 ITPA 中被報導會改變剪接,並與降低的 ITPA 表達和酶活性相關,腫瘤細胞中降低的 ITPA 表達導致 Thiopurine 耐藥性 [Article:24624911]。與 ITPA 多態性相關的生存率降低在亞洲 ALL 患者中報導。
ABCC4
幾個 ABCC4 的變異在 GWAS 中顯示對 Thiopurine 代謝和細胞 表現型 具有影響 [Article:24624911]。 變異 rs3765534 C>T 是一個非同義變異,導致蛋白質變化為 Glu757Lys。具有 rs3765534 TT 變異基因型的細胞(如在此負鏈基因的正染色體鏈上報導)對 6MP 毒性具有更高的敏感性。與參考 等位基因 相比,TT 變異的細胞對 6-MP 代謝物的排除能力較差,這是由於細胞表面表達較低 [Article:18593894]。這在一項針對日本 IBD 患者的研究中得到了確認,其中 rs3765534 TT 和 CT 基因型與白血球計數降低、6-TGNs 增加以及在接受 azathioprine 或 mercaptopurine 治療時增加的 白血球減少 可能性相關,與 CC 基因型相比 [Article:20393862]。一項針對日本小兒 ALL 患者的研究發現,那些對任何 ABCC4 變異 rs3765534、rs2274407 或 rs11568658 的次要 同型合子(Homozygous) 具有純合子的患者需要較低的每日劑量 [Article:25403995]。 對於編碼變化 p.Lys304Asn rs2274407C>A 的結果是矛盾的。在一項針對與 6MP 和甲氨蝶呤共同治療的白人加拿大小兒 ALL 患者的研究中,AC 基因型與較高的血小板減少症和較低的 EFS 相關,與 CC 基因型相比 [Article:19515727]。而在一項針對埃及小兒 ALL 患者的研究中,該患者也接受了 6MP 和 MTX 治療,報導了相反的關係,其中 CC 與較高的骨髓毒性相關,與 AA 和 AC(嗜中性白血球低下症 和 白血球減少)相比 [Article:26237184]。對於這一變異的進一步功能研究可能會澄清其作用。
其他基因
其他各種基因和變異在單一研究中顯示對 Thiopurine 表現型 的影響,包括 AOX1 [Article:19500084]、PACSIN2 [Article:22846425]、HLA 同種型 [Article:25217962]、微 RNA [Article:23358152]、ATP6AP2、GNG2、FRMD4B、NME1、UTP18 和 KCNMA1 [Article:24624911],以及其他。這些在 PGx 標籤下的變異註釋中有描述。
注意 此圖已於 2017 年更新,以包含 2010 年發表的圖中未顯示的新候選基因。