CPIC 指南註解:abacavir 與 HLA-B
摘要
對於攜帶HLA-B*57:01變異等位基因("HLA-B*57:01陽性")的個體,不建議使用abacavir,只有在特殊情況下才考慮使用。詳細的免責聲明、更多細節與支持證據,請參見完整指南。
為特定註釋指定基因型或表現型
註釋
本註解基於藥物基因體學臨床應用聯盟 (Clinical Pharmacogenetics Implementation Consortium, CPIC®) 關於 abacavir 與 HLA-B 的指南:CPIC® guideline for abacavir and HLA-B。
2014 年 5 月更新
線上接受文章預覽 2014 年 2 月 21 日;線上提前發表 2014 年 3 月 12 日
關於 abacavir 的 2014 年 CPIC 指南更新 已發表於期刊《Clinical Pharmacology and Therapeutics》。文獻回顧範圍為 2011 年 4 月至 2013 年 11 月。結果顯示無新證據會改變原始指南。因此,原始出版物中的劑量建議仍具臨床適用性。
- 本指南適用於:
- HIV 病人
- 「雖然將 HLA-B*57:01 與 abacavir 過敏反應相關性的多數證據來自成人研究,但沒有理由推測 HLA-B*57:01 陽性的兒童比陽性的成人承受較低風險。此外,Panel on Antiretroviral Therapy and Medical Management of HIV-Infected Children(Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection;http://aidsinfo.nih.gov/con-tentfiles/lvguidelines/pediatricguidelines.pdf)建議對 HLA-B*57:01 檢測呈陽性的兒童,應避免使用 abacavir。」
- 下載與閱讀:
2012 年 4 月
線上提前發表 2012 年 2 月
- 下載與閱讀:
以下為 abacavir 劑量指南之節錄:
我們同意他人之建議*,應在所有尚未接觸過 abacavir 的個體開始含 abacavir 之治療前,進行 HLA-B*57:01 篩檢(見下表 1);此一建議與 FDA、美國衛生與公共服務部及歐洲藥品管理局之建議一致。對於尚未使用過 abacavir 且呈 HLA-B*57:01 陽性的個體,不建議使用 abacavir。僅在潛在利益(基於抗藥性模式與治療史)明顯大於風險之特殊情況下,方可考慮使用。
*[文章:18826546, 19640227, 21174626, 21412232] Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents (PDF)
表 1:根據 HLA-B 基因型對 abacavir 的推薦治療用法
改編自 2012 年指南手稿之表 1 與表 2。
| 可能之表型 | 基因型 | 雙倍型(diplotype)範例 | 對表型測量之意涵 | abacavir 治療建議 | abacavir 治療建議分級 a |
|---|---|---|---|---|---|
| 過敏反應風險極低(約占患者之 ~94% b) | 未檢出 *57:01 等位基因(基因分型報告為「negative」) | *X/*X c | abacavir 過敏反應之風險低或降低 | 依標準劑量指引使用 abacavir | 強烈建議 |
| 過敏反應風險高(約占患者之 ~6%) | 至少存在一個 *57:01 等位基因(基因分型報告為「positive」) | *57:01/*X c;*57:01/*57:01 | abacavir 過敏反應之風險顯著增加 | 不建議使用 abacavir | 強烈建議 |
a 評分方案見 2012 Supplement
b 不同族群/地理群之基因型頻率估計,見 2012 Supplement
c *X = 任何除 *57:01 以外之 HLA-B 基因型。
HLA-B = human leukocyte antigen B
收聽主要作者訪談: podcast
abacavir 途徑, 藥物動力學/藥效學
概括
abacavir 的代謝及作用機制的示意圖。潛在的 abacavir 過敏反應機制亦顯示於此。
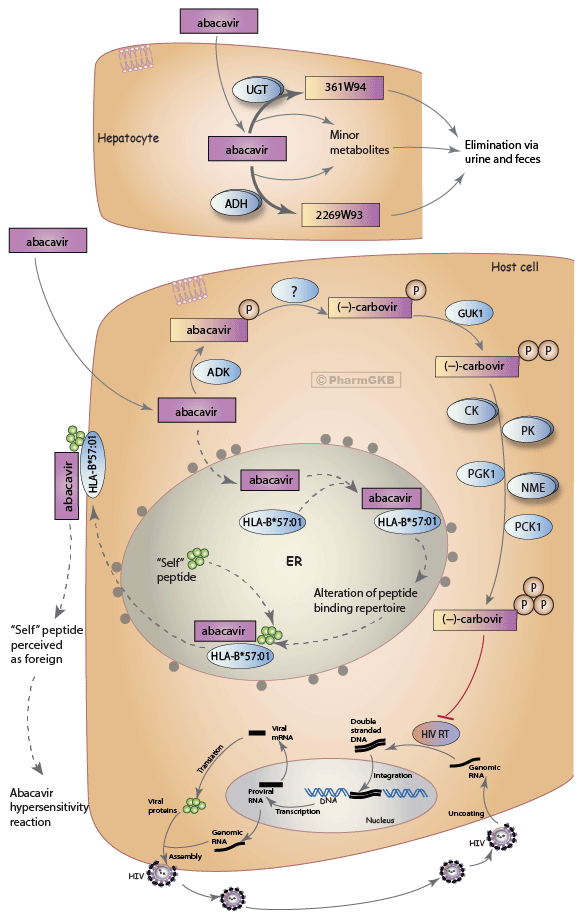
描述
引言
abacavir 是一種核苷類逆轉錄酶抑制劑 (NRTI),用於治療人類免疫缺陷病毒 (HIV) 感染。HIV 感染通常使用抗逆轉錄病毒療法 (ART) 方案進行治療,這些方案由三種或更多不同的藥物組合而成。這些方案中常用的抗逆轉錄病毒藥物包括 NRTI、非核苷類逆轉錄酶抑制劑 (NNRTIs)、蛋白酶抑制劑 (PIs) 和整合酶鏈抑制劑 (InSTIs) [Article:22820792]。abacavir 由於其劑量靈活性,使其成為這類組合療法的理想補充。它可以每天給藥一次或兩次,以匹配其他藥物的劑量模式,並且可以與其他抗逆轉錄病毒藥物如拉米夫定或齊多夫定的片劑一起給藥,從而減少藥丸數量 [Article:18479171]。abacavir 通常耐受性良好,常見的副作用包括噁心、頭痛和腹瀉 [Article:18479171]。然而,大約 5-8% 的患者在治療的前 6 週內會出現過敏反應 ([HSR)。過敏反應的症狀包括至少兩種以下情況:發燒、皮疹、咳嗽、胃腸道症狀(例如噁心、嘔吐、腹痛)、呼吸困難和疲勞 [Article:22378157]。這些症狀在持續治療時會加重,但通常在停藥後 24 小時內改善。然而,因 abacavir 停藥後重新挑戰藥物可能會在幾小時內導致症狀復發,並可能引發潛在危及生命的過敏反應 [Articles:11888582, 10449301。這種過敏反應與 強烈建議 相關,與 HLA-B*57:01 等位基因 的存在密切相關, 美國食品藥品監督管理局 (FDA)、 歐洲藥品管理局 (EMA)、藥物基因體學臨床應用聯盟(CPIC) 和 荷蘭藥物基因體學工作小組 (DPWG)] 建議在 abacavir 治療前進行 等位基因 測試。abacavir 也被報導與心肌梗死的風險較其他 NRTIs 相關 [Articles:18387667, 19682101, 20660842, 18753925]。然而,FDA 在 2012 年進行的一項荟萃分析未能發現任何此類關聯 [Article:22932321]。
藥物相互作用
由於 abacavir 主要通過細胞質醇脫氫酶 (cytosolic alcohol dehydrogenase , ADH) 和尿苷二磷酸葡萄糖醛酸轉移酶 (uridine diphosphate glucuronosyltransferase, UGT) 代謝,因此預測 abacavir 與細胞色素 P450 (CYP) 酶的誘導劑或抑制劑之間不會有相互作用 [Article:18479171]。此外,體外研究顯示 abacavir 在臨床相關濃度下不太可能抑制 CYP 酶 [Article:10898676]。由於 NNRTIs 和 PIs 主要由 CYP 酶代謝 [Article:12416447],這可能消除了與這類抗逆轉錄病毒藥物的藥物相互作用的潛力。當 abacavir 與其他 NRTIs(如lamivudine或zidovudine)聯合給藥時,未觀察到臨床上顯著的藥代動力學變化 [Articles:18479171, 10320951]。由於酒精也由 ADH 代謝,因此已分析該藥物與乙醇之間的藥代動力學相互作用,但未報告臨床上顯著的變化或新的不良事件 [Article:10817729]。此外,與 UGT 誘導劑如rifampicin和phenobarbital的同時治療可能會降低 abacavir 的血漿濃度,但這些相互作用的臨床意義尚不清楚 [Article:14709631] [抗逆轉錄病毒藥物與結核病治療] [EMA 歐洲公共評估報告:Trizivir]。幾項研究發現 abacavir 的給藥與同時感染 HIV 的肝炎 C 患者在接受ribavirin和pegylated interferon治療時的病毒學反應之間存在聯繫;在這些患者中,abacavir 的使用被發現與早期病毒學失敗顯著相關 [Article:17460476] 以及缺乏持續的病毒學反應 (SVR) [Articles:18572756, 18854330]。然而,來自兩項研究的亞群分析發現,abacavir 對 SVR 的影響僅在基線肝炎 C 病毒 RNA 超過某一水平的患者中顯著 [Article:18854330],ribavirin每日劑量低於某一水平 [Article:18854330],或ribavirin血清谷濃度(Ctrough) 低於某一水平 [Article:18572756]。此外,許多研究未發現 abacavir 的使用與病毒學反應之間的關聯 [Articles:20167995, 17938129, 19043930, 22781224],因此不確定這兩種藥物是否存在顯著且有害的相互作用。
藥物動力學
一個關於 abacavir 在體內分佈的示意圖如上所示。abacavir 在口服給藥後迅速被吸收,平均絕對生物利用度約為 83% [Articles:18479171, 10453964]。該藥物具有脂溶性,但也顯示出高水溶性,允許其僅通過被動擴散穿過細胞膜。這些特性可能解釋其高生物利用度,並使該藥物能夠輕易滲透到血腦屏障等組織中 [Articles:9145874, 18479171]。吸收後,abacavir 在肝臟內被廣泛代謝,未變化的藥物在尿液中排泄的比例低於 2% [Article:10582871]。ADH 和 UGT 是肝細胞內 abacavir 代謝的主要酶。ADH 的代謝產生無活性的羧酸代謝物 2269W93;UGT 酶的代謝產生無活性的葡萄糖醛酸代謝物 361W94 [Article:10582871]。一項質量平衡研究發現,83% 的原始劑量通過尿液排出,16% 通過糞便排出。在通過尿液排出的 83% 中,36% 的劑量回收為葡萄糖醛酸代謝物,30% 為羧酸代謝物。剩餘的劑量為母藥或微量代謝物 [Article:10582871]。
未被肝細胞代謝的母藥在病毒感染的細胞內通過不同的細胞內酶進行合成,將藥物轉化為其藥理活性代謝物。最初,abacavir 被腺苷磷酸轉移酶(由 ADK 基因編碼)合成為 abacavir 5'-單磷酸。然後,它通過一種未知的細胞質酶脫胺,轉化為 (-)-羧維 5'-單磷酸;在細胞內未檢測到 abacavir 的二磷酸或三磷酸 [Articles:9145874, 9145876]。羧維 5'-單磷酸隨後由酶鳥苷酸激酶 (GUK1) 轉化為羧維 5'-二磷酸,該酶對 (-) 立體異構體的羧維 5'-單磷酸具有立體選擇性 [Articles:1383219, 9145876, 10066527]。一項研究發現,(-)-羧維 5'-單磷酸作為鳥苷酸激酶的底物的效率比 (+) 立體異構體高 7000 倍 [Article:1383219]。羧維 5'-二磷酸隨後由各種細胞激酶轉化為活性 5'-三磷酸形式。這些包括肌酸激酶(由 CK 基因組表示)、丙酮酸激酶 (PK 基因組)、核苷二磷酸激酶 (NME 基因組)、磷酸甘油酸激酶 (PGK1) 和磷酸烯醇丙酮酸羧激酶 (PCK1)。考慮到鳥苷酸激酶的立體選擇性,只有 (-)-羧維 5'-三磷酸以任何顯著數量形成。然而,(+)-立體異構體具有相等的抗病毒活性 [Articles:1383219, 9145876]。
abacavir 也可以通過其他次要 途徑 轉化為羧維 5'-單磷酸,例如轉化為羧維,然後通過腺苷磷酸轉移酶將羧維磷酸化為羧維 5'-單磷酸。由於這些 途徑 佔 abacavir 合成的比例低於 2%,因此未在圖中顯示 [Article:9145876]。
藥效學
一個關於 abacavir 在宿主細胞內作用機制的風格化描述如 途徑 圖所示。羧維 5'-三磷酸 (CBV-TP) 代表 abacavir 的活性形式,通過阻止 HIV 逆轉錄酶 (HIV-RT) 的作用來發揮作用。HIV 通過利用宿主細胞現有的遺傳機制以及病毒酶逆轉錄酶進行複製,該酶負責將病毒 RNA 轉換為雙鏈 DNA。病毒 DNA 隨後可以被納入宿主 DNA,此時宿主機制可能將 DNA 轉換為病毒 RNA。病毒 RNA 隨後被翻譯為病毒蛋白,這些蛋白組裝形成 HIV 病毒 [Article:11309630]。CBV-TP 作為鳥苷的類似物,並與由 HIV-RT 從病毒 RNA 產生的核苷酸鏈競爭以進行整合 [Article:9145874]。其他 NRTIs 可以作為不同核苷的衍生物,導致相同類型的抑制。例如,didanosine 與 adenosine, zalcitabine 與 cytidine ,以及 zidovudine 與 thymidine [Article:10929917]。在 CBV-TP 被納入核苷酸鏈後,其在核糖上缺乏 3'-OH 使得無法添加後續的核苷,從而阻止病毒 DNA 的持續合成 [Articles:9145876, 11309630]。羧維三磷酸和鳥苷三磷酸的結構比較,以及 abacavir 的結構可見於下圖中的圖 1。
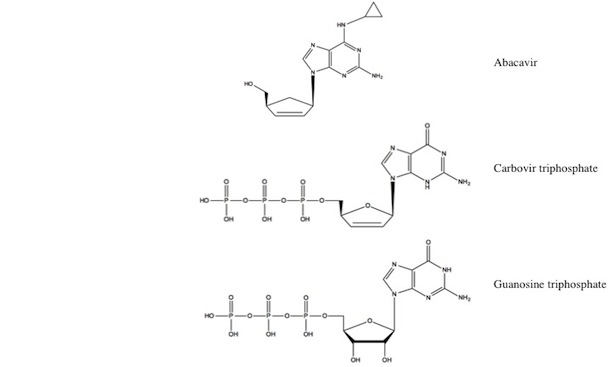
圖 1。 abacavir、羧維三磷酸 (CBV-TP) 和鳥苷三磷酸 (GTP ) 的結構。注意 CBV-TP 和 GTP 之間的結構相似性,排除 CBV-TP 中核糖糖環上缺乏關鍵的自由 3'-OH 基團。這一缺失阻止了任何額外核苷的添加,並阻止了進一步的病毒 DNA 合成。結構改編自 [Article:18479171] 和 ChemSpider。
CBV-TP 對於這一角色特別合適,因為其對逆轉錄酶的選擇性高於 DNA 聚合酶 α、β、γ 和 ε。事實上,DNA 聚合酶 α、β、γ 和 ε 的 Ki 值分別比 HIV-RT 的 Ki 值高 90、2900、1200 和 1900 倍 [Article:9145874]。這種對逆轉錄酶的選擇性避免了抑制 DNA 聚合酶時可能出現的毒性副作用。許多抗逆轉錄病毒 NRTIs 與一系列不良事件相關,這些事件歸因於線粒體功能障礙,如乳酸酸中毒和肝脂肪變性。這被認為是由於這些藥物抑制了線粒體 DNA 聚合酶 γ,導致線粒體 DNA 複製的改變和隨之而來的線粒體 肌肉病變 和毒性。abacavir 對聚合酶 γ 的抑制最低,而zalcitabine, didanosine 和 stavudine的抑制最高 [Article:10929917]。
藥物基因體學
Abacavir 的藥物基因體學特性已相當明確,且幾乎完全與人類白血球抗原 B (human leukocyte antigen B, HLA-B) 基因及其變異等位基因 *57:01 相關。大量研究已明確指出,該等位基因與 abacavir 引起的過敏反應(hypersensitivity reaction, HSR)之間具有高度相關性,如下所述。然而,該等位基因的陽性預測值約為 50% [Article:18256392],顯示 HSR 的發生可能尚涉及其他遺傳因素。在這一領域的研究有限,但有一些潛在的變異存在於 HSP70-HOM 基因中(也稱為 HSP1AL),其蛋白質被假設直接參與刺激對 abacavir 的免疫反應 [Article:17545699]。
HLA-B*57:01
HLA-B 基因是位於第 6 號染色體的主要組織相容性複合體 (MHC) 區域的一部分。這一基因組區域編碼三組參與免疫系統的基因。HLA-B 是 I 類組的一部分,與 HLA-A 和 HLA-C 一起編碼其同名蛋白質。HLA-B 蛋白質及其他 I 類組成員是細胞表面分子,負責將內源性肽呈現給免疫系統細胞,並存在於幾乎所有有核細胞上。這與 II 類分子形成對比,後者顯示外源性肽,僅存在於抗原呈現細胞 (APCs) 如巨噬細胞或樹突細胞上。簡而言之,I 類分子如 HLA-B 是由一條 α 鏈(由 HLA-B 基因編碼)和一種稱為 β2-微球蛋白的蛋白質組成,該蛋白質在第 15 號染色體上編碼。HLA-B 的 α 鏈有四個結構域:一個細胞質結構域、一個跨膜結構域、一個與 CD8+ 細胞毒性 T 細胞結合的結構域,以及一個構成肽結合槽的結構域,待呈現的肽在其中安置。這一基因的特定區域具有高度多態性,允許呈現各種肽。HLA-B 呈現的大多數肽來自細胞蛋白的正常降解,並被免疫系統識別為“自我”肽。然而,當細胞被病原體感染時,呈現的蛋白質將來自病原體並被識別為外來或“非自我”。CD8+ 細胞毒性 T 細胞上的 T 細胞抗原受體 (TCRs) 負責這一識別,並將刺激免疫反應並摧毀該細胞 [免疫生物學,Janeway,第 3 和第 5 章]。
在 2002 年,兩個獨立的研究小組發表了證據,顯示 等位基因 被稱為 HLA-B*57:01 在顯示 abacavir HSR 的患者中出現的比例顯著高於未出現反應的患者。一項是在北美人群中進行的 [Article:11943262],另一項是在被稱為西澳大利亞 HIV 群體中進行的 [Article:11888582]。這兩項研究均包括 200 名患者。這一結果在英國一項包含 64 名參與者的研究中得到了確認 [Article:15247625]。然而,這三項研究主要是在以白人男性為主的樣本中進行的,限制了其範圍。儘管存在這一限制,幾個診所開始實施這些 等位基因 的前瞻性篩查,取得了良好的效果 [Articles:18025891, 17356469, 16758424]。後來的一項研究認識到 等位基因 在白人女性和西班牙裔人群中的重要性,但在黑人群體中未發現任何顯著的關聯 [Article:15016610]。這可能是由於該研究中黑人患者的數量較少(與西班牙裔或白人相比)以及黑人群體對 等位基因 的攜帶率較低 [Articles:11543903, 15016610]。歐洲人群的 *57:01 等位基因頻率 約為 6-7%,但非洲人群的頻率通常低於 2.5%。此外,一些亞洲人群,如日本人或南韓人,具有極低的 等位基因 頻率,為 0.5% 或更低;相比之下,一些印度人群的 *57:01 頻率可高於 16% [Article:22378157]。在 2007 年,一項名為 SHAPE 的研究(該研究包括相似數量的白人和黑人參與者)發現黑人患者的 abacavir HSRs 數量較少。然而,在免疫學上確認的 HSRs 患者中,100% 的白人和黑人患者均對 HLA-B*57:01 等位基因 呈陽性。這表明,儘管在黑人群體中,由於對 等位基因 的攜帶率降低,免疫學確認的 HSRs 是罕見的,但 HLA-B*57:01 等位基因 在兩個群體中具有相同的臨床意義 [Article:18444831]。2008 年,PREDICT-1 研究的結果顯示了這一 等位基因 與 abacavir HSRs 之間的明確關聯,這是一項雙盲、前瞻性、隨機研究,涉及來自 19 個國家的 1956 名患者。患者觀察了六週,並分為兩類:接受 HLA-B*57:01 等位基因 篩查的患者,若測試陽性則被排除,以及接受標準護理而未進行任何篩查的患者。abacavir HSRs 透過皮膚貼片測試進行免疫學確認。研究結果顯示,篩查完全消除了 HSRs - 0% 的篩查患者出現 HSR,而對照人群中有 2.7%。這使得篩查的陰性預測值達到 100%。然而,該研究發現陽性預測值為 47.9%,這表明約一半的 HLA-B*57:01 陽性患者不會發展為 abacavir HSR [Article:18256392。這表明其他基因可能參與了 HSR 的發展。這篇論文以及大量現有證據促使 FDA 在 2008 年實施了盒裝警告,詳細說明了 HSR 的風險,針對接受 abacavir 治療的 HLA-B*57:01 等位基因。FDA,以及 EMA、CPIC 和 DPWG 也建議所有患者在接受治療前進行篩查,並且不應在 abacavir 的 HLA-B*57:01 陽性個體中使用。
HLA-B 蛋白質對 abacavir 藥物動力學 或 藥效學 沒有直接影響,且目前尚不清楚 HLA-B*57:01 等位基因 如何影響對藥物過敏的易感性。目前存在幾種假說。一種理論是半抗原概念,認為小化合物如藥物(稱為“半抗原”, haptens)與結合到免疫受體如 HLA-B 的肽結合,導致 T 細胞反應並刺激免疫反應 [Article:17075282]。另一種理論是 p-i 概念(與免疫受體的藥理學相互作用),認為藥物直接且可逆地與免疫受體結合,刺激免疫反應 [Article:17075282]。最近的證據似乎支持另一種假說。兩項於 2012 年發表的研究發現 abacavir 可以非共價且特異性地結合在 HLA-B*57:01 的肽結合槽的 F 口袋中 [Articles:22645359, 22722860]。由於 *57:01 特有的氨基酸殘基,abacavir 只能結合到這一特定形式的 HLA-B。abacavir 與 HLA-B*57:01 的結合被認為改變了抗原結合裂縫的 SHAPE 和化學性質,從而改變了可以結合該分子的肽的範疇。事實上,這兩篇論文以及 Norcross 等人的另一篇論文均發現,在 abacavir 存在的情況下,HLA-B*57:01 呈現的肽發生了特定的變化,與藥物缺失時相比 [Articles:22645359, 22722860, 22617051]。傳統的 HLA-B*57:01 表位通常在其 C 末端具有大疏水性氨基酸,如色氨酸或苯丙氨酸;Illing 等人、Ostrov 等人和 Norcross 等人均發現,在 abacavir 存在下,脫附的肽在此位置更偏好異亮氨酸或亮氨酸 [Articles:22722860, 22645359, 22617051]。這一結合及隨後的肽改變在 途徑 圖中顯示 - 使用虛線,因為這一機制目前尚未得到充分確立。肽加載和運輸到細胞表面質膜的典型循環 ([Article:14511229])也顯示在圖中。由於 T 細胞在胸腺發育過程中被訓練對特定肽的範疇產生耐受性,因此可以呈現的肽的變化可能意味著這些新肽被視為外來物。這一變化將刺激 CD8+ T 細胞的產生和反應,並表現為 abacavir HSR [Articles:22722860, 22645359]。事實上,CD8+ T 細胞在出現皮疹的患者的皮膚活檢中豐富存在,這些患者在 abacavir HSR 中 [Article:18549801]。
HSP70-HOM
對於 HLA-B*57:01 等位基因 和 abacavir HSRs 的陽性預測值約為 50%,這表明需要進一步研究以闡明可能影響 HSR 發展的其他基因。這一領域的研究相對稀少,但幾項研究已經提出 70 千道爾頓熱休克蛋白 (HSP70) 家族的成員作為潛在因素。HSP70 蛋白質負責保護細胞免受壓力,以及其他細胞活動,如協助蛋白質折疊 [Article:9222585]。人類 MHC 區域中的三個基因編碼 HSP70 家族的成員:HSP70-1、HSP70-2 和 HSP70-HOM [Article:1356099]。HSP70-1 和 -2 編碼相同的熱誘導蛋白產物,而 HSP70-HOM 編碼類似但非熱誘導的蛋白質 [Article:1356099]。一項使用西澳大利亞 HIV 群體的研究發現,rs2227956基因中的參考 C 等位基因(導致第 493 位殘基為threonine而非methionine)與 HLA-B*57:01 等位基因的組合出現在 94.4% 的免疫學確認過敏病例中,而在對照組中僅為 0.4%;而 HLA-B*57:01 等位基因則在 94.4% 的過敏病例和 1.7% 的對照組中單獨出現。作者建議除了 HLA-B*57:01 ,考慮 HSP70-HOM等位基因可能會提高區分會發展為 HSR 的患者與耐受對照組的能力。該人群由 230 名對照組和 18 名 HSR 患者組成,等位基因被發現在強烈連鎖不平衡 [Article:15024131]。需要在更大的人群中進行進一步研究以驗證這一關聯。然而,後來的一項研究確實發現 HSP70-HOM 蛋白質與 HLA-B*57:01 蛋白質和 abacavir 在內質網中共定位。這暗示著 HSP70-HOM 493Thr 變異可能導致一種蛋白質,從而促進 abacavir 抗原向 CD8+ T 細胞的呈現,可能通過在抗原處理中護送藥物 [Article:17545699]。
結論
在 abacavir 治療前實施 HLA-B*57:01 測試是藥物基因體學 研究在臨床上應用的最佳例子之一,並且這一基因分型在西方世界廣泛可用。儘管如此,應進一步研究導致 abacavir HSR 的其他基因。這可能提高陽性預測值,使更多可能受益於治療的患者能夠接受 abacavir。目前對其他基因的參與幾乎沒有證據,僅有 HSP70-HOM 基因的變異出現作為潛在因素。在這一領域的進一步理解可能防止對能夠耐受的患者不當拒絕 abacavir,並希望進一步闡明 abacavir 引發其過敏反應的機制。