CPIC 指南註解:carbamazepine 與 HLA-A、HLA-B 基因
摘要
CPIC 對於 carbamazepine 的劑量指引更新建議,對於攜帶至少一個 拷貝 的 HLA-B*15:02 或 HLA-A*31:01 的 carbamazepine 初次使用患者,應考慮使用替代藥物,因為這些 等位基因 與 史蒂芬-強森症候群及毒性表皮壞死溶解症(SJS/TEN) 的風險增加有關。此外,HLA-A*31:01 也與 藥物反應合併嗜酸性球及全身症狀(drug reaction with eosinophilia and systemic symptoms, DRESS)和 斑丘疹型皮疹(Maculopapular exanthema, MPE) 的風險增加有關。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC®關於carbamazepine、HLA-B和HLA-A的指引。
2017年12月
文章預覽於2018年1月線上接受;2018年2月提前線上發表
- 2017年CPIC指引更新有關carbamazepine劑量的藥物基因體學測試已在《Clinical Pharmacology and Therapeutics》期刊由藥物基因體學臨床應用聯盟(CPIC)發表。文獻回顧至2016年6月,更新了建議和補充信息。
- 2017年劑量指引更新摘錄:
- 「有證據顯示HLA-B*15:02基因型與carbamazepine和oxcarbazepine引起的SJS/TEN風險相關,並且HLA-A*31:01基因型與carbamazepine引起的SJS/TEN、DRESS和MPE風險相關。」
- 「描述HLA-B*15:02和HLA-A*31:01基因型與兒科患者carbamazepine或oxcarbazepine引起的皮膚不良反應之間關係的數據稀少。在缺乏數據顯示這些HLA等位基因與兒科患者藥物誘發過敏反應之間存在不同關係的情況下,建議可用於指導成人和兒科患者使用carbamazepine和oxcarbazepine。」
- 下載並閱讀:
表1:基於HLA-B和HLA-A基因型的carbamazepine治療建議
改編自2017指引更新的表1和表2
| 可能表現型 | 基因型 | 雙倍型示例 | 表型影響 | 治療建議 | 建議分類a | 其他芳香族抗癲癇藥的考量 |
|---|---|---|---|---|---|---|
| 同型合子(Homozygous)對於等位基因s以外的HLA-B*15:02和HLA-A*31:01 | 非HLA-B*15:02或HLA-A*31:01攜帶者。無HLA-B*15:02或HLA-A*31:01等位基因s報告,基因分型測試中通常報告為「陰性」。 | *X/*X b *Y/*Y c |
carbamazepine引起的SJS/TEN、DRESS和MPE的正常或降低風險。 | 按照標準劑量指引使用carbamazepine。d | 強烈建議 | |
| 同型合子(Homozygous)或同型合子(Homozygous)為HLA-A*31:01和同型合子(Homozygous)為HLA-B等位基因s以外的*15:02 | HLA-A*31:01攜帶者。一個或兩個*31:01等位基因s,基因分型測試中通常報告為「陽性」。非HLA-B*15:02攜帶者。無HLA-B*15:02等位基因s報告,基因分型測試中通常報告為「陰性」。 | *X/*X b *31:01/*Y c *31:01/*31:01 |
carbamazepine引起的SJS/TEN、DRESS和MPE的風險增加 | A. 如果患者對carbamazepine是初次使用且有替代藥物可用,則不使用carbamazepine。 B. 如果患者對carbamazepine是初次使用且無替代藥物可用,考慮使用carbamazepine並增加臨床監測頻率。在首次出現皮膚不良反應的證據時停止治療。 C. 藥物誘發皮膚不良反應的潛伏期取決於表現型,但通常在規律劑量的3個月內發生。因此,如果患者之前使用carbamazepine超過3個月而未發生皮膚不良反應,則可謹慎考慮使用carbamazepine。 |
A. 強烈建議 B. 可選建議 C. 可選建議 |
A. 其他芳香族抗癲癇藥(例如eslicarbazepine、lamotrigine、phenytoin、fosphenytoin和phenoarbital)與_HLA-A*31:01 等位基因的SJS/TEN、DRESS和/或MPE的關聯證據非常有限,因此無建議可以在選擇其他芳香族抗癲癇藥作為替代藥物時做出。 C. 之前對carbamazepine的耐受性不代表對其他芳香族抗癲癇藥的耐受性。 |
| 同型合子(Homozygous)或同型合子(Homozygous)為HLA-B*15:02和任何HLA-A*31:01基因型(或HLA-A*31:01基因型未知) | HLA-B*15:02攜帶者。一個或兩個*15:02等位基因s,基因分型測試中通常報告為「陽性」。 | *15:02/*X b *15:02/*15:02 |
carbamazepine引起的SJS/TEN風險增加 | A. 如果患者對carbamazepine是初次使用,則不使用carbamazepine。 B. 藥物誘發SJS/TEN的潛伏期在持續劑量和遵從治療的情況下較短(約4-28天),通常在劑量的3個月內發生;因此,如果患者之前持續使用carbamazepine超過3個月而未發生皮膚不良反應,則可謹慎考慮未來使用carbamazepine。 |
A. 強烈建議 B. 可選建議 |
A. 其他芳香族抗癲癇藥(例如eslicarbazepine、lamotrigine、phenytoin、fosphenytoin和phenoarbital)與HLA-B*15:02等位基因的SJS/TEN關聯證據較弱;然而,在選擇替代藥物時仍應謹慎。 B. 之前對carbamazepine的耐受性不代表對其他芳香族抗癲癇藥的耐受性。 |
a 評分方案描述於2017更新補充(見上文)
b *X = 任何HLA-B基因型以外的*15:02
c *Y = 任何HLA-A基因型以外的*31:01
HLA-B = 人類白血球抗原 B
HLA-A = 人類白血球抗原 A
d HLA-B*15:02對carbamazepine引起的SJS/TEN具有100%的陰性預測值,目前建議其用於指導carbamazepine和oxcarbazepine的使用。由於HLA-B*15:02與其他芳香族抗癲癇藥相關的SJS/TEN的關聯性較弱且陰性預測值低於100%,在東南亞人群中進行陰性HLA-B*15:02測試後使用這些藥物代替carbamazepine或oxcarbazepine不會預防抗癲癇藥相關的SJS/TEN。
2013年9月
文章預覽於2013年5月線上接受;2013年6月提前線上發表
- 有關carbamazepine劑量的藥物基因體學測試指引已在《Clinical Pharmacology and Therapeutics》期刊由臨床藥物基因體學s實施聯盟(CPIC)發表。
- 2013年carbamazepine劑量指引摘錄:
人類白血球抗原 B (HLA-B)是一個編碼細胞表面蛋白的基因,該蛋白參與向免疫系統呈遞抗原。變異等位基因HLA-B*15:02與carbamazepine治療反應中的史蒂芬-強森症候群及毒性表皮壞死溶解症(SJS/TEN)風險增加相關。我們總結了支持此關聯的已發表文獻證據,並根據HLA-B基因型提供carbamazepine使用建議。
Carbamazepine 途徑, 藥物動力學
概括
風格化的肝細胞,描繪參與藥物動力學的候選基因,與Carbamazepine相關。
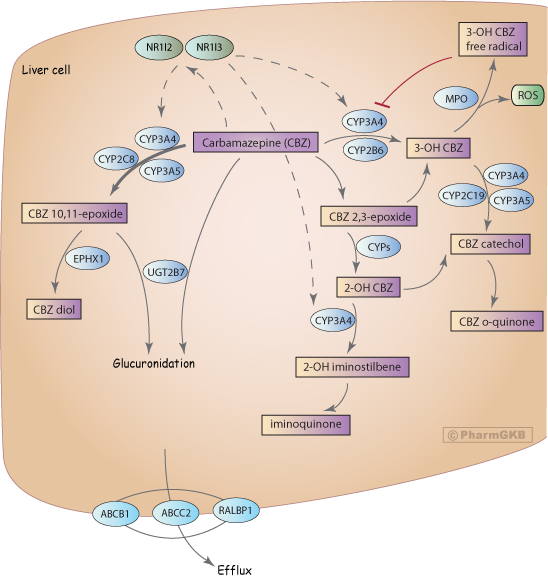
描述
背景
Carbamazepine (CBZ), 一種二苯並氮雜環化合物,是一種三環類抗癲癇藥,用於治療癲癇、三叉神經痛及精神疾病 [Article:18463198]。已報告與CBZ相關的嚴重不良事件,包括史蒂文斯-約翰遜症候群 (SJS)、毒性表皮壞死症 (TEN) 和 藥物反應合併嗜酸性球及全身症狀(DRESS) (DRESS) [Articles:20235791、18717872]。其他類型的過敏反應也與CBZ相關,包括輕微皮疹、發燒、嗜酸性粒細胞增多症及對其他抗癲癇藥的交叉反應。高達80%的對CBZ藥物有特發性藥物反應的患者,對其他抗癲癇藥也會出現不良反應,進一步限制了治療選擇 [Article:3198757]。除了不良事件外,療效不足也可能成為問題,約30%的癲癇患者會經歷藥物抗藥性 [Articles:18088268、19415824]。這些事件發生的機制尚不完全清楚,儘管有幾個候選藥物基因與CBZ的治療反應相關。目前個體化治療的方法包括治療藥物監測(TDM),在治療後測量患者樣本中的藥物代謝物,並隨後進行劑量調整。雖然這提供了藥物反應的準確視圖表現型,但仍然存在不良事件和交叉敏感的風險。能夠識別將從CBZ中受益的患者,避免不良事件並在治療前確定劑量,將是一個非常有價值的臨床工具。在此,我們呈現CBZ 藥物基因體學 (PGx) 的當前知識,作為藥物動力學的基因中心視角,並彙總與CBZ反應相關的基因變異。
]藥物動力學
CBZ幾乎完全在肝臟中代謝,只有約5%的藥物以未改變的形式排泄 [Article:15915352]。主要的代謝途徑是轉化為CBZ 10.11-環氧化物 (CBZ-E)[Article:18463198]。這一反應主要由CYP3A4催化,儘管CYP2C8也起到一定作用,並且也有建議涉及CYP3A5 [Articles:18463198、8010982]。次要的代謝途徑包括環羥基化形成2-羥基-CBZ (2-OH-CBZ)和3-羥基CBZ (3-OH CBZ)。每種的形成大概是通過環氧化物中間體(稱為芳香烴氧化物中間體)進行的,其中CYP2B6和CYP3A4是3-OH-CBZ形成的主要催化劑 [Article:18463198],而多種CYP參與2-OH-CBZ的形成 [Article:12386121]。2-OH-CBZ和3-OH-CBZ的次級代謝由CYP3A4代表兩種不同的潛在生物活化途徑。CYP3A4-依賴的次級氧化反應2-OH-Carbamazepine導致通過亞胺醌中間體形成硫醇反應性代謝物 [Article:16135660],而CYP3A4-依賴的次級氧化反應3-OH-CBZ則導致形成能夠使CYP3A4失活的反應性代謝物 [Article:18463198],並形成共價加合物 [Article:18096676]。3-OH CBZ,以及在較小程度上2-OH CBZ和CBZ,可以被髓過氧化物酶 (MPO)代謝形成自由基 [Article:18463199]。這釋放了反應性氧物種,並可能導致蛋白質加合物的形成。共價結合和蛋白質加合物的形成也已在另一種抗癲癇藥物苯妥英中觀察到,並且通常被認為是此類MPO化合物特發性反應發病機制中的必要步驟 [Article:18463199]。
CBZ刺激參與其自身代謝的基因的轉錄上調,通過CYP3A4和CYP2B6的自誘導,經由NR1I2 (PXR)和[[KEEP_75de6FDA]] (CAR) [Articles:3319544、17112801、19702527]。藥物交互作用通過CYP3A4 [Article:10668858]和CYP2B6 [Article:19223624]已被充分記錄,並可能使CBZ在多重療法中使用變得複雜。
一些研究表明,葡萄糖醛酸化在CBZ和CBZ-E的代謝中可能僅起到次要作用 [Article:15915352]。但其他文獻則對此提出異議,記錄了UGT2B7的參與 [Articles:15292462、17495417]。
運輸
CBZ的變異運輸,特別是穿越血腦屏障的變異,可能是導致CBZ反應變異的原因。增加從大腦的排出被討論為一種藥物抗藥性的方法,主要集中在P-糖蛋白 (PgP,編碼於ABCB1) [Article:18088268]。儘管在老鼠的研究中建議PgP運輸CBZ [Article:11733711],但體外測試和小鼠的研究未顯示PgP對CBZ的運輸證據 [Articles:11318771、18824002]。最近的研究確認CBZ不被PgP運輸,儘管它確實運輸CBZ 10, 11-環氧化物 [Article:21692796]。RALBP1,也稱為RLIP76,已被證明能運輸CBZ並參與藥物抗藥性 [Article:16188027]。額外的PGx證據表明ABCC2是CBZ的潛在藥物基因 [Article:20216337],然而細胞研究顯示ABCC1、ABCC2和ABCC5在體外未運輸CBZ [Article:20080116]。見下文有關運輸體和CBZ PGx的特定基因變異的討論。
藥物基因體學
主要組織相容性位點變異
與CBZ相關的最為研究的PGx變異是位於人類白血球抗原基因HLA-B中的主要組織相容性 (MHC) 位點的變異 [Article:18370849]。HLA-B編碼一種向免疫系統呈遞肽段的蛋白質,識別外來或感染的細胞 [Article:518865。根據IMGT/HLA數據庫,已知有超過1500個等位基因的HLA-B linkout][Article:21071412]。歷史上這些變異是通過血清型表型鑑定的,儘管現在測序已經很普遍,但與這些變異相關的確定基因變異尚未得到良好描述。這一位點在不同族群中的極端多樣性意味著不同的標籤SNP與不同人群中的不同血清型相關 [Article:16998491]。與嚴重ADR、SJS和TEN的風險最相關的等位基因是HLA-B*1502 [Article:15057820]。有一種機制被提出來解釋CBZ過敏反應的觸發,涉及蛋白酶體降解和MHC-依賴的CBZ代謝物的呈遞 [Article:18991696]。自由基的生成被認為是另一種可能的機制。通過與CYP3A4酶形成加合物,自由基可能也會促進與其他抗癲癇藥物有時出現的交叉反應性過敏 [Article:18096676]。一項體外研究顯示CBZ-修飾的肽與HLA-B*1502蛋白的共價結合可能導致T細胞的激活和SJS,具體與此等位基因相關 [Article:17697703]。
HLA*1502 等位基因與CBZ-誘導的SJS/TEN在台灣人、中國人、印度人和華裔美國人中有密切關聯,但在白人或日本人中則無 [Articles:15057820、16538176、20833111、19915237、16415921、16981842、18637831、19018717。這導致臨床仿單從FDA建議僅在基因風險人群中對有祖源的個體進行測試 FDA linkout。在漢族中國HapMap樣本中,SNP的標籤是SNPs rs3909184和rs2844682] [Article:16998491]。
HLA-A*3101與CBZ-誘導的ADR在亞洲人中有關聯 [Article:16538176]。最近兩項獨立的GWAS研究顯示HLA-A*3101與CBZ-誘導的ADR在白人 [Article:21428769]和亞洲人 [Article:21149285中有關聯。與HLA-A*3101在亞洲人群中的連鎖標籤是rs1633021] [Article:21149285,而在白人群體中則是rs1061235] [Article:21428769]。
由於MHC區域的高度連鎖,標籤SNP可能標記另一基因中的功能變異。變異rs3909184(位於FLOT1基因內)、rs2844682(MUC21)、rs1059510(HLA-E)、rs1264511(基因間)、rs3130690(基因間)、rs2848716(基因間)、rs750332(BAT2)、rs2227956(HSPA1A、HSPA1L、LSM2)、rs1043620(HSPA1A、HSPA1L、LSM2)、rs506770(HSPA1A、HSPA1L)、rs2395402(LEMD2)、rs986475(LST1、LTB、NCR3)、rs2894342(MLN)和rs1800629(TNF:(-308)G>A)已與CBZ-誘導的ADR有關 [Articles:16538176、16538175、11294926]。此外,HLA-B*0702 等位基因在一項小型白人研究中顯示能夠保護免受嚴重CBZ過敏 [Article:16981842]。由於並非所有擁有HLA*1502 等位基因的個體都會經歷ADR,因此仍不清楚哪些特定的SNP是致病的,哪些僅僅是標籤SNP。確定哪些SNP是致病的將有助於更好地識別那些有ADR風險的患者,特別是在那些沒有亞洲祖源的患者中。
代謝酶變異
代謝酶中的變異已被證明會影響CBZ 藥物動力學,儘管相關研究較少且未經重複驗證。功能降低的蛋白質CYP3A4*16 (rs12721627)在體外系統中顯示出清除率降低 [Articles:19255940、20847137],因此可能需要對具有此變異的個體進行劑量調整(在日本、韓國和墨西哥人群中的頻率為1-5%)。CBZ的清除率可能會受到CYP3A5變異的影響 [Articles:19744012、16678552。一項針對韓國癲癇患者的小型研究發現,CYP3A5的非表達者 (CYP3A5*3, rs776746])的CBZ清除率較高,且血漿水平也高於CYP3A5的表達者,這一發現似乎不一致,但可以通過CYP3A基因的自誘導來解釋 [Article:19744012]。然而,對日本癲癇患者的更大研究未發現差異,儘管該研究包括可能進一步誘導CYP3A4的合併用藥 [Article:16678552。[[KEEP_7347285]]的變異也與[[KEEP_d0FDAd23]]的代謝改變相關 [Article:15692831。單倍型的rs1051740 (EPHX1: Y113H)和rs2234922] (EPHX1: H139R)在日本癲癇患者中顯示出增加的血漿CBZ-二醇/CBZ-E環氧化物比率 [Article:15692831。對代謝藥物的多態性研究及其對CBZ-誘導的ADR的影響大多為陰性[],其中一項研究將SNP與CYP2B6的3'UTR的變異 (rs1042389)與斑丘疹和過敏綜合症相關,但在Bonferroni校正後並不顯著 [Article:16538176]。
運輸體變異
有關CBZ運輸和抗藥性的PGx研究同樣存在矛盾,並需要在更大的人群中進行重複驗證。著名的ABCB1變異3435C>T,rs1045642 CC基因型與315名英國患者中的藥物抗藥性癲癇相關,儘管該研究中使用的藥物未具體說明 [Article:12686700]。隨後的幾項研究未發現此變異的關聯(見Bournissen等人的綜合分析),這些研究也未按治療分開患者 [Article:19178561。對464名中國癲癇患者的研究將ABCB1變異rs3789243和rs2032582]與CBZ抗藥性相關 [Article:19450124],但對228名北印度癲癇患者的研究未能重複此關聯 [Article:20417680]。雖然不同的單倍型結構或種族背景可能影響這些結果,但Bournissen綜合分析的子分析分別檢查歐洲和亞洲人群,也未發現ABCB1:3435C>T與藥物抗藥性的關聯 [Article:19178561]。
對RALBP1表達的初步研究指向其在藥物抗藥性癲癇中的作用 [Article:16188027],然而對英國人群中RALBP1變異的兩項研究未能發現所有治療的關聯 [Articles:17437410、18086001。在僅有81名患者的小子集中,對CBZ的變異rs329017]存在弱相關,但p值不顯著,作者認為值得進一步研究 [Article:18086001。已重複的關聯是與ABCC2 SNP c.1249G>A (p.V417I,rs2273697])。該變異與146名接受CBZ的韓國癲癇患者中的神經ADR相關,並在同一族裔的獨立隊列中進行了驗證 [Article:20216337。另一個在ABCC2中的變異(-24C > T,rs717620])與年輕白人癲癇患者對CBZ的缺乏反應相關 [Article:19415824]。
藥效變異
雖然未在圖中顯示,但CBZ的靶點——大腦鈉通道SCN1A、SCN1B、SCN2A和SCN3A具有藥物基因組學的影響。變異SCN1A IVS5N+5 G>A (rs3812718,也報導為SCN1A IVS4-91G>A)與癲癇患者的高劑量需求相關 [Articles:15805193、17436242]。SCN2A和SCN3A的變異可能會促進CBZ的抗藥性 [Articles:18784617、18242854]。來自小鼠的體外證據也表明SCN1B是CBZ的潛在藥物基因,可能值得進一步研究 [Article:20573896]。
結論
至今,HLA 等位基因 (HLA-B*1502 和 HLA-A*3101) 是與Carbamazepine最重要的藥物基因組學變異。雖然令人鼓舞的是,已對CBZ進行了變更,以防止嚴重副作用 [Article:21428768],但我們仍需了解這些事件發生的機制以及種族如何影響這一點,以便在未知或混合祖源的個體中更可靠地進行測試。
儘管已收集初步數據以顯示基因變異對CBZ代謝的影響,但研究規模較小且未經驗證。對藥物抗藥性的PGx定義工作因多種抗癲癇藥的共同治療而變得複雜。需要進行更大規模的研究,以確保每個記錄的治療組中有足夠的樣本數,並明確定義表現型。還需要更多的工作將觀察到的代謝差異和藥物動力學轉化為使用基因變異進行預測劑量。