CPIC 指南註解:peginterferon alfa-2a、peginterferon alfa-2b、ribavirin 與 IFNL3 基因
摘要
IFNL3 (IL28B) 變異(rs12979860)是 HCV 基因型 1 患者對含 PEG-interferon-alpha 治療方案反應的強烈建議佳基線預測因子。具有有利反應基因型(rs12979860 CC)的患者相比具有不利反應基因型(rs12979860 CT 或 TT)的患者,更有可能對含 PEG-interferon-alpha 的治療方案產生反應(較高的 SVR 率)。在開始含 PEG-IFN alpha 和 RBV 的治療方案之前,請考慮其影響。
註釋
此註釋基於CPIC® 指南,針對PEG interferon-alpha為基礎的方案和IFNL3。
2014年2月
文章預覽於2013年10月線上接受;2013年11月提前線上發表。
-
關於PEG-interferon-alpha (PEG-IFN alpha) 和 ribavirin (RBV) 治療中藥物基因體學測試的使用指南已於《Clinical Pharmacology and Therapeutics》期刊由藥物基因體學臨床應用聯盟(CPIC)發表。
-
這些指南適用於
- 成人
-
摘錄自2013年PEG-interferon-alpha治療劑量指南:
- 「IFNL3基因分型的作用取決於治療選擇。IFNL3基因型只是影響HCV基因型1感染中PEG-IFN alpha和RBV治療反應率的因素之一,應在其他臨床和遺傳因素的背景下解釋。」
- 「對於僅接受PEG-IFN alpha和RBV治療的患者,IFNL3基因型是HCV治療反應的強烈建議最佳預測因子。在原始發現隊列的意向治療分析中,rs12979860的高加索CC基因型患者比CT或TT患者更有可能在第4週時病毒不可檢測(28%對5%和5%,P<0.0001),並達到持續病毒學應答(SVR)(69%對33%和27%,P<0.0001)。在這個隊列中,西班牙裔和非裔美國患者也觀察到了類似的模式。HCV治療與顯著的副作用相關,反應治療的可能性影響臨床醫師和患者之間關於開始治療的共同決策。」
- 「對於接受蛋白酶抑制劑組合治療的基因型1感染的初治患者,所有IFNL3基因型的反應率均比僅用PEG-IFN alpha和RBV提高。然而,具有有利IFNL3基因型的患者在初治患者中仍然具有更高的反應率,這些反應率可能指導患者和臨床醫師的治療決策。在boceprevir的第三期初治研究中,與PEG-IFN alpha和RBV的組合,rs12979860 CC患者接受boceprevir的SVR率範圍為80-82%,而CT患者為65-71%,TT患者為59-65%。此外,多變量回歸分析顯示rs12979860 CC是SVR的預測因子,相較於CT(比值比(OR)2.6,95% CI 1.3-5.1)和TT基因型(OR 2.1,95% CI 1.2-3.7)。」
-
下載並閱讀:
表1:基於IFNL3基因型的PEG-interferon-alpha含量方案的推薦治療用途
改編自2013年指南手稿的表1和表2
| rs12979860的基因型 | 表現型 | PEG-IFN alpha和RBV的影響a | 蛋白酶抑制劑與PEG-IFN alpha和RBV治療組合的影響 | 建議等級 b |
|---|---|---|---|---|
| CC | 有利的反應基因型 | 治療48週後約有70%的機會達到SVRc。在開始PEG-IFN alpha和RBV含量方案之前考慮影響。 | 治療24-48週後約有90%的機會達到SVR。約80-90%的患者有資格接受縮短療程(24-28週對48週)d。有利於使用PEG-IFN alpha和RBV含量方案。 | 強烈建議 |
| CT或TT | 不利的反應基因型 | 治療48週後約有30%的機會達到SVRc。在開始PEG-IFN alpha和RBV含量方案之前考慮影響。 | 治療24-48週後約有60%的機會達到SVR。約50%的患者有資格接受縮短療程(24-28週)d。在開始PEG-IFN alpha和RBV含量方案之前考慮影響。 | 強烈建議 |
a 在蛋白酶抑制劑不可用的情況下。
b 評分方案在補充中描述。
c SVR;持續病毒學應答(定義為治療結束後12-24週血清病毒RNA不可檢測)。
d 接受boceprevir的患者如果在第八週HCV RNA不可檢測,則有資格接受24-28週的療程,而不是標準的48週。接受telaprevir的患者如果在第四週HCV RNA不可檢測,則有資格接受24週的療程,而不是標準的48週。
PEG-IFN alpha:聚乙二醇化干擾素alpha 2a或2b;RBV:ribavirin
Peginterferon alpha-2a/Peginterferon alpha-2b 途徑 (肝細胞),藥效學
概括
建議的作用機制為針對慢性丙型肝炎的聚乙二醇干擾素α (PEG-IFN-α) 基礎療法。
描述
引言
PEG化干擾素-alpha(PEG干擾素-alfa 或 PEG-IFN-α)是一種抗病毒和免疫調節藥物,已作為治療丙型肝炎病毒(HCV)感染的基礎,已有超過二十年的歷史。目前,市場上有兩種PEG-IFN與廣譜抗病毒藥物利巴韋林(RBV)聯合使用,治療慢性HCV:PEG-IFN-α 2a 和 PEG-IFN-α 2b。這兩種藥物的區別在於其共價結合的聚乙烯醇(PEG)基團的大小和性質。雖然PEG-IFN-α 2a 和 2b 在藥物動力學和劑量方案上存在差異,但共識認為這兩種藥物在臨床上是等效的[Article:20108989]。
丙型肝炎感染影響全球1.7至2億人,是肝硬化和肝細胞癌的主要原因(世界衛生組織。丙型肝炎。WHO事實表164。瑞士日內瓦:世界衛生組織;2000年。查閱日期:2014年4月28日。http://www.WHO.int/mediacentre/factsheets/fs164/en/)。儘管在大多數發達國家中,HCV的流行率似乎正在下降,但由於HCV感染引起的肝病死亡率預計在未來20年內將持續上升[Article:23280550]。雖然少數急性HCV感染的患者能夠自發清除病毒,但55-85%的患者會發展為慢性HCV感染,定義為可檢測的HCV RNA持續超過6個月[Article:12407573]。一旦建立慢性感染,通常不會自發解決[Article:17151366]。治療的主要目標是實現持續的病毒學反應(SVR),其特徵是在治療結束後24周內血清病毒RNA不可檢測,這被臨床認為是感染的治癒,並與較低的發病率和死亡率相關[Article:23268517]。HCV分為七個已知的基因型(1-7),在30-35%的核苷酸位點上存在差異[Article:8175159]。HCV基因型在全球的分佈不同,其中基因型1在北美、南美和歐洲最為流行[Article:25069599。此外,HCV基因型與[[KEEP_77FDAcb1]]-α/RBV聯合療法的反應高度相關,且基因型1和4的患者治療引起的SVR的比率最低[Article:19330875]。
在2011年之前,慢性HCV患者的標準治療是聯合使用PEG-IFN-α/RBV療法(無論是PEG-IFN-α 2a還是2b),治療時間為48周,針對基因型1、4、5和6,或24周針對基因型2和3。然而,這些聯合療法在[[KEEP_09aFDA6d]]基因型1患者中的SVR率僅為40-50%[Article:21696309]。相比之下,基因型2和3的SVR率約為70-80%,儘管這些適用於沒有伴隨HCV的選定人群[Articles:21696309, 11583749, 12324553, 14996676, 12407598]。此外,聯合療法成本高,與多種中等建議至嚴重副作用(流感樣症狀、抑鬱、血小板減少症和溶血性貧血)相關[Article:16107837],並且在許多患者中禁忌(肝功能失代償、門脈高壓、脾功能亢進、重度精神抑鬱、重大系統損害和懷孕)(世界丙型肝炎:全球警報與應對。瑞士日內瓦:世界衛生組織;2000年。查閱日期:2015年2月8日。http://www.WHO.int/csr/disease/hepatitis/WHOcdscsrlyo2003/en/index5.html)。達到SVR的正向預測因素包括年輕、女性和低治療前HCV-RNA水平[Article:25114601]。相反,SVR率在基線HCV-RNA水平高(>800,000 IU/mL)、脂肪變性、胰島素抵抗、與HIV的共感染以及更進展的肝纖維化的HCV患者中較不可能發生[Articles:25114601, 17151366]。
強烈建議的最佳治療前預測因子是位於19號染色體上的IFNL3的變異(以前稱為IL28B)。該基因編碼IFN-lambda 3(IFN-λ3),屬於3型IFN-λ家族,具有抗病毒、抗增殖和免疫調節活性[Article:20712453。強烈建議最常測試的多態性是rs12979860和rs8099917],分別位於IFNL3的3 kb和8 kb上游,並顯示出強烈建議 連鎖不平衡 [Article:22118055。如下面詳細描述,具有有利的rs12979860 CC或rs8099917] TT基因型的患者有超過2倍的可能性達到治療引起的SVR。該藥物基因體學臨床應用聯盟(CPIC)為臨床醫生提供了如何利用基因信息進行治療決策的建議,並根據IFNL3基因分型制定了詳細的指導方針,以用於PEG-IFN-α/RBV-基礎的治療方案[Article:24096968。IFNL3基因型可以幫助決定是否開始PEG-IFN-α/RBV療法,考慮到不良事件和治療失敗的風險。一旦決定開始治療,IFNL3基因型可用於指導治療組合(例如,是否開處方PEG-IFN-α/RBV雙重療法或包括DAA的三重療法)和持續時間(例如,是否在某些患者中縮短治療時間)。目前的共識是,rs1297860(合併為rs154739)基因型是SNP最有可能預測治療反應的基因型,如果必須選擇單一SNP作為診斷目的,儘管針對rs12979860和rs8099917]的基因分型測試在商業上可用[Articles:21254181, 24114761]。
最近,直接作用抗病毒藥物(DAA)的出現,這些藥物直接針對HCV生命周期的特定階段,使得SVR在HCV基因型1患者中達到更高的比率。DAA直接針對HCV生命周期的特定階段。儘管PEG-IFN和RBV仍然是這些藥物第一波療法的基本組成部分,但它們不再是推薦的方案之一。第一個方案被稱為三重療法,包括一種DAA與PEG-IFN和RBV的組合。這些方案顯著提高了SVR的比率,並使許多患者的治療方案縮短[Article:21898493]。在2011年,美國肝病研究協會(AASLD)更新了其針對慢性HCV基因型1患者的實踐指導方針,改為包括任一種“第一代”蛋白酶抑制劑DAA(BOCeprevir(BOC)或telaprevir(TVR)的三重療法[Article:21898493]。這些三重療法顯示出65-75%的SVR率[Articles:21449784, 21696307, 21696308]。第二代蛋白酶抑制劑simeprevir於2013年獲得批准,將SVR的比率提高至約80%[Article:25192745]。最近獲批的sofosbuvir顯示出進一步提高SVR比率的巨大潛力,無論是作為與PEG-IFN-α/RBV的三重療法[Articles:24266912, 23944316, 23499440],還是作為IFN-自由療法的一部分[Articles:24262278, 24209977]。最後,最近獲批的FDA-自由方案由paritaprevir(ABT-450)經ritonavir增強、ombitasvir、dasabuvir和利巴韋林組成,已在治療未接受過治療的患者和之前未反應的患者中顯示出超過95%的SVR率,這些患者均為HCV基因型1且無肝硬化24720703, 24720679。因此,AASLD最近修訂了其針對HCV基因型1患者的實踐指導方針,只包括IFN-自由方案,這不僅提高了耐受性,還提高了療效(美國肝病研究協會。丙型肝炎的檢測、管理和治療建議;2014年。查閱日期:2014年4月28日。http://www.HCVguidelines.org)。
藥物動力學
聚乙烯醇(PEG)基團的附加(PEG化)是改善藥物動力學的重大進展。與每週三次給藥的未修飾IFN-α相比,PEG-IFN允許每週一次的給藥,並避免血清濃度的大幅波動。PEG-IFN-α 2a具有一條分支的40 kDa PEG鏈共價附著於賴氨酸殘基,並以完整分子的形式循環,而PEG-IFN-α 2b則具有一條線性的12 kDa PEG鏈,通過不穩定的氨基甲酸酯鍵共價附著,並在注射後水解。附著的PEG基團的大小和性質導致藥物的藥物動力學和劑量方案的差異[Article:22233411]。
未修飾IFN-α的吸收半衰期為2.3小時,而PEG-IFN-α 2a和2b的半衰期分別約為50小時和4.6小時[Article:12934165]。除了較長的半衰期外,PEG-IFN-α 2a的局部化程度高於PEG-IFN-α 2b,分佈體積較小(0.99 L/kg),最高濃度出現在肝臟[Article:12934165]。接受單劑量PEG-IFN-α 2a的患者在給藥後78小時達到平均最大血清濃度14.2 µg/L[Article:20951922]。在多次給藥(每週180 µg)後,平均最大血清濃度為25.6 µg/L,平均達到時間為45小時。相比之下,PEG-IFN-α 2b的最大血清濃度在給藥後15至44小時之間達到,並持續48至72小時。PEG-IFN-α 2a的峰谷比為1.5至2,而多次給藥後的峰谷比則大於10。因此,PEG-IFN-α 2a在一週劑量間隔期間血清濃度波動較小[Article:12934165]。
PEG-IFN-α 2a的較長半衰期和有限分佈允許固定的每週劑量。相反,PEG-IFN-α 2b的每週劑量必須根據體重進行調整[Article:20108989]。由於PEG-IFNα 2b的血清半衰期相對較短,許多患者在每週劑量間隔結束時可能會有不可檢測的藥物水平,這可能導致病毒反彈[Articles:15456079, 17875007]。因此,有人建議對PEG-IFN-α 2b採用較短的劑量間隔,例如每週兩次的方案,儘管這尚未正式測試[Article:20951922]。
PEG-IFN-α 2a由肝臟和腎臟清除;約30%的PEG-IFN-α 2b由腎臟清除,其餘由肝臟清除或在與細胞IFN受體相互作用後降解[Article:12934165]。與標準IFN-α相比,PEG-IFN-α 2a和2b的腎清除率顯著降低[Article:12052715]。
RBV的共同給藥不影響PEG-IFN的藥物動力學,也不會影響PEG-IFN對RBV的影響[Article:10960463。對於接受[[KEEP_f5FDA583]]-α 2b/RBV聯合療法的患者,第一週的平均峰值血漿RBV濃度分別為741 ng/mL、799 ng/mL和1101 ng/mL,對應於每日RBV劑量600、800和1000-1200 mg。在第四週,這些劑量方案產生的平均峰值血漿RBV濃度分別為1770 ng/mL、2297 ng/mL和2750 ng/mL,累積達到5倍。無論劑量組如何,RBV的表觀清除率始終為23-26 L/h[Article:12934165]。
藥效學
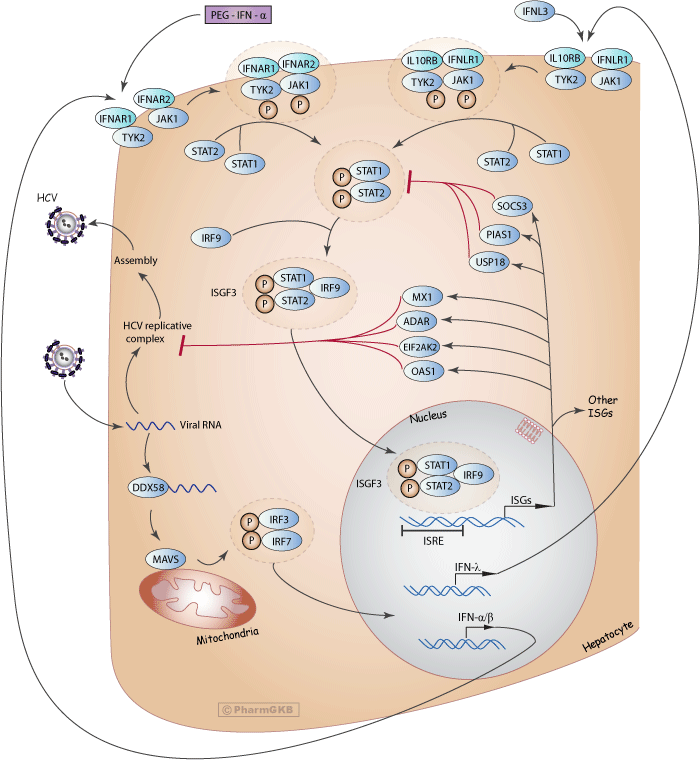
IFN-α同時以直接和間接的方式發揮抗病毒作用,儘管PEG-IFN-α抑制HCV複製的確切機制仍不清楚[Article:20108989]。IFN-α通過誘導細胞中的非病毒特異性免疫反應來發揮作用,通過上調許多IFN-刺激基因(ISG)來編碼抗病毒效應蛋白。如上圖所示(圖1),當HCV RNA被宿主的先天免疫系統檢測到時,它會被幾種病原體識別受體(PRRs)識別,例如視黃酸誘導基因-1(RIG-1),由DDX58基因編碼。RIG-1激活適配器線粒體抗病毒信號蛋白(MAVS),進而誘導IFN調節因子3(IRF3)和IRF7的磷酸化。這兩種蛋白質異二聚化,然後轉位到細胞核,誘導各種IFN的表達和分泌,包括IFN-α、IFN-β和IFN-λ。
循環的IFN-α與兩個獨特的細胞表面受體亞基結合,IFN-α R1(IFNAR1)和IFN-α R2(IFNAR2)。一旦與IFNAR1和IFNAR2結合,形成異二聚體並激活Janus激活和酪氨酸激酶(JAK),這反過來又磷酸化細胞質信號轉導和轉錄激活因子(STAT)蛋白,其中包括STAT1和STAT2。磷酸化的STAT1和STAT2異二聚化並結合IFN調節因子9(IRF9),形成IFN-刺激基因因子3(ISGF3)複合物。ISGF3然後轉位到細胞核,與IFN-刺激反應元件(ISRE)結合,誘導ISG mRNAs的轉錄,編碼多種效應蛋白。
微陣列分析顯示,IFN-α誘導數百種ISG,其中許多與抗病毒活性相關,但其他則涉及脂質代謝、細胞凋亡、蛋白質降解和炎症反應[Article:11404376]。在抑制HCV複製方面,認為主要的ISG包括2',5'寡腺苷酸合成酶1(OAS1)、真核翻譯起始因子2-alpha激酶2(EIF2AK2,以前稱為PKR)、腺苷脫氨酶RNA-特異性(ADAR)和MX動力學樣GTP酶1(MX1)。相反,抗病毒信號由抗炎ISG控制,例如泛素特異性肽酶18(USP18)、細胞因子信號抑制因子3(SOCS3)和活化蛋白抑制劑1(PIAS1),這些因子作為負反饋迴路的一部分,通過直接或間接抑制STAT信號來限制IFN反應的範圍和持續時間[Articles:22956738, 17525754]。
除了抗病毒活性外,IFN-α還通過與適應性和先天免疫反應的相互作用來發揮免疫學效應,以促進記憶T細胞增殖、預防T細胞凋亡、刺激自然殺手細胞活化和樹突細胞成熟[Article:9041265]。最後,IFN-α已被證明能增加主要組織相容性複合體(MHC)I類和II類分子的產生[Article:10790425]。然而,這些免疫學特性可能與HCV的清除並無直接關聯,IFN-基礎的療法被認為主要是由其抗病毒活性發揮作用[Article:23886001]。
病毒學下降,通常稱為“病毒反應的動力學”,是治療期間達到SVR的重要預測因子。在PEG-IFN-α/RBV療法中,快速的病毒清除(RVR)和早期病毒反應(EVR),分別定義為4周後血清HCV RNA不可檢測和12周後HCV RNA下降2個對數,均已顯示與SVR相關[Articles:21371579, 21898493]。事實上,SVR率對於達到RVR的患者超過70%,在這些情況下可以縮短治療方案[Articles:18069698, 19780879]。
PEG-IFN-α 2a與2b的藥效學似乎相似。藥效學比較顯示這兩種PEG-IFN-α形式表現出相似的生物活性,這從2',5' OAS、neopterin和MHCI類分子β 2-微球蛋白的誘導模式中得以證實[Articles:17635371, 20108989]。然而,一項研究發現PEG-IFN-α 2b在31名HCV基因型1感染患者中表現出更強的ISG激活[Article:16780997]。
與IFN-α類似,IFN-λ激活Janus激酶-信號轉導和轉錄激活因子(JAK-STAT) 途徑,通過與IFN-刺激反應元件(ISRE)結合,上調多種ISG。IFN-λ在實驗模型中已被證明能抑制HCV複製,並且當與IFN-α共同給藥時,這種抗病毒效應是相加的[Articles:15731279, 17087946]。儘管IFN-α和IFN-λ通過相同的下游途徑上調類似的ISG,但它們通過獨特的受體進行信號傳導:IFN-λ與IL10R-IL28R受體複合物結合,該複合物僅在肝細胞中高度表達[Article:12483210]。此外,兩者之間的反應動力學不同:IFN-λ表現出更快速的磷酸化,但與IFN-α相比,各種ISG的表達延遲且持續時間更長[Article:17087946]。由於IFN-λ受體的分佈更有限等因素,已建議IFN-λ的PEG化形式可能比PEG-IFN-α更易於耐受[Articles:21147189, 20564352]。
RBV對HCV的作用機制仍不清楚。有人提出RBV直接抑制HCV複製或抑制宿主酶肌苷單磷酸脫氫酶(IMPDH)[Article:11981750]。相反,RBV可能通過導致病毒顆粒的快速和致命突變或耗竭細胞內的鳥苷三磷酸(GTP)來間接對抗HCV病毒複製,這是病毒RNA合成所需的[Articles:11602568, 11100123]。最後,有人提出RBV可能通過免疫調節活性發揮作用[Article:17151366]。
藥物基因體學
IFNL3變異和PEG-IFN-α/RBV治療反應
不同族群之間以及感染相同HCV基因型的患者之間,HCV清除和對PEG-IFN-α的反應存在顯著變異,這長期以來指向宿主基因因素作為治療成功的決定因素[Article:22641049。在2009年,幾項全基因組關聯研究(GWAS)獨立顯示,位於19號染色體上的幾個SNP,接近IFNL3,與感染HCV基因型1或4的個體對PEG-IFN-α/RBV療法的反應強烈建議相關。這些研究顯示,具有IFNL3位點的HCV基因型1患者(rs12979860 CC或rs8099917] TT)在接受PEG-IFN-α/RBV聯合療法時,達到SVR的可能性是2至3倍,並且在沒有治療的情況下,自發HCV清除的比率也較高,與具有不利的T或C基因型的患者相比[Articles:19684573, 19749758, 19759533, 19749757, 20060832, 19759533, 20637200, 21413051]。這些發現後來在幾項候選基因研究中得到了驗證[Articles:20728570, 20578254, 20576307, 20176026]。IFNL3基因型與SVR的關聯已在來自亞洲、歐洲和拉丁美洲的各種人群中得到獨立研究的確認[Articles:19749757, 21911885, 22301466, 21907615, 21987611,21346780, 22368681, 21447862, 24114761]。因此,IFNL3變異構成了強烈建議最佳的治療前指標,預測PEG-IFN-α/RBV對HCV基因型1患者的反應,即使考慮到已知的臨床預測因素[Articles:19684573, 20060832。一旦開始PEG-IFN-α/RBV療法,具有有利的rs12979860] CC基因型的患者在2、4、12和48周的治療時間點上也與顯著更高的病毒清除率相關,顯示出更好的病毒動力學,以及更高的RVR、EVR、治療結束反應和降低的病毒學復發率[Article:20399780]。
大多數感染HCV基因型2和3的患者研究發現,IFNL3基因型與治療反應之間的相關性相對較弱,但大多數研究未能達到STAT的統計顯著性[Articles:21612542, 20060832, 20621700, 21112657, 21360545, 21112660],這可能是因為這類患者的SVR率通常較高[Article:24114761]。此外,由於感染HCV基因型2和3的患者之間不同基因型的SVR率變化通常較小,因此IFNL3基因分型在預測SVR方面的價值可能不大。然而,在HCV基因型2和3患者的研究中,已顯示IFNL3基因型與RVR之間存在顯著關聯[Articles:21916985, 21254157, 21145807, 21374656]。IFNL3基因型在感染HCV基因型2和3的患者中可能更有助於預測RVR,這可以幫助決定縮短治療時間並最小化與治療相關的不良反應[Article:24325405]。
IFNL3基因在HCV-HIV共感染和肝移植患者中的作用
與HCV的共感染在感染人類免疫缺陷病毒(HIV)的患者中相對常見(15-40%),這可能是由於共同的傳播途徑[Article:17502718]。由於共感染患者的HCV-相關肝病進展加速[Articles:11462196, 14679458],HCV已成為感染HIV-個體中重要的發病率和死亡率原因[Article:16908797]。不幸的是,HIV-HCV共感染患者對PEG-IFN-α/RBV療法的反應也較單一感染患者差[Article:17502718]。因此,對PEG-IFN-α/RBV治療反應的預測因子對於識別當前療法的最佳候選者非常有用。IFNL3基因型與PEG-IFN-α/RBV療法結果之間的關聯在對HCV基因型1和4的共感染患者的研究中一致顯示,但在基因型3和4的患者中則未見相關[Articles:21612542, 21916985。幾項研究顯示,具有有利的IFNL3基因型(rs12979860 CC或rs8099917] TT)與較高的SVR率相關[Articles:21612542, 21916985, 20389235, 20804372, 21048934,儘管一項比較兩者的研究發現rs12979860]是反應的更好預測因子[Article:22328925]。IFNL3基因分型在與HIV和HCV基因型1或4的共感染患者中也可能有用,這些患者之前未能對PEG-IFN-α/RBV療法產生反應,以識別非反應者WHO可能受益於再治療[Articles:1916985, 21537116]。
此外,IFNL3基因型已被證明是肝移植患者再感染的重要預測因子。在幾個獨立的隊列中,捐贈者和受贈者的有利rs12979860 CC和rs8099917 TT基因型已被證明與較高的SVR率相關[Articles:21466653, 22411462, 22766768, 21384511]。然而,大多數識別相關性的研究是在HCV基因型1患者中進行的,對其他基因型的關聯證據較少[Article:24114761]。
不同族群中IFNL3 等位基因的分佈
有利的IFNL3 rs12979860多態性在不同族群中分佈不均,非裔美國人的頻率最低(等位基因頻率 0.39),東亞和東南亞人群的頻率最高(接近0.9),而高加索人和西班牙裔的頻率則居中(分別為0.63和0.55)[Articles:19684573, 19759533, 20399780, 22438096。SNP的rs12979860和rs8099917]在患者中表現出強烈建議 連鎖不平衡,但在非洲祖源患者中則有部分連鎖不平衡,在高加索人中為部分連鎖不平衡,在亞洲人中幾乎完全連鎖不平衡[Articles:19684573, 20060832]。有利的等位基因的不同頻率有助於解釋不同SVR率之間的差異[Articles:19684573, 19826275。例如,估計約一半的歐洲裔美國人和非裔美國人之間的SVR率差異是由於rs12979860] C 等位基因所致[Article:19684573]。然而,在具有有利的rs1297860 CC基因型的非裔美國患者中,病毒動力學顯示出較慢,SVR率低於相同基因型的歐洲裔美國人。這可能表明,族裔仍然是結果的獨立預測因子,並指出目前尚未發現的基因變異影響治療反應,特別是在非裔美國人中[Article:20399780]。
IFNL3變異對治療反應的擬議機制
IFNL3變異的生物學意義,以及IFNL3基因型對PEG-IFN-α和RBV反應的實際機制仍不清楚。雖然IFNL3多態性對IFN-λ的產生和肝內ISG的表達影響仍存在爭議,但有人提出ISG的表達模式可能在一定程度上解釋了SVR率的差異。有趣的是,具有不利的IFNL3基因型(rs1297860 CT/TT)的患者在基線時發現肝內ISG的表達較高,這與未能對PEG-IFN-α/RBV治療產生反應相關[Articles:18467494, 20434452]。這一解釋是,具有不利基因型的患者表現出持續的、無效的肝內ISG的表達。同時,IFN-信號抑制劑如SOC3和PIAS1也被上調;這種預先激活的ISG反應可能不足以清除病毒,同時通過負調節JAK-STAT信號來降低對PEG-IFN-α療法的敏感性,這是由IFN-信號抑制劑引起的[Articles:18467494, 21898478]。因此,即使在給予PEG-IFN-α的情況下,細胞也可能無法誘導強烈建議足夠的ISG表達,無法清除病毒[Article:21898478]。
相反,具有有利的IFNL3基因型的患者可能對HCV RNA的反應較弱,因此發生的IFN表達較少,導致基線時的ISG水平較低和病毒載量較高。當給予IFN-α時,可能對負調節分子的信號抑制較少,導致細胞對IFN的敏感性更高,並且可能誘導更強的強烈建議的ISG。最終,這種不受限制的IFN信號轉導和強烈建議 ISG的刺激可能導致更有效的病毒清除。事實上,具有有利的IFNL3基因型的患者在治療的每個時間點上都被觀察到更有效地消除HCV,顯示出更好的病毒動力學[Article:20931559]。然而,儘管已知與治療反應相關並提出了其影響的機制,但尚不清楚有利的IFNL3 SNP是否實際上發揮生物學效應,或僅僅與其他功能性多態性相關聯。
IFN4(ss469415590)和PEG-IFN-α/RBV治療反應
最近,對IFNL3上游的基因區域的研究發現了一個新的瞬時誘導區域,該區域包含一個二核苷酸變異,rs368234815 TT/ΔG(最初指定為ss469415590),與rs12979860高度相關,並被建議作為可能的因果變異[Articles:24786669, 23291588, 23712427]。ss469415590ΔG是一種框移變異,創建了一個新基因IFNL4,編碼IFN-lambda4蛋白(IFN-λ4)。IFN-λ4與IFN-λ3相似但不完全相同[Article:23291588]。像現有的三個IFN-λ家族成員一樣,IFN-λ4在體外表現出抗病毒活性,並與IL10RB/IFNLR1受體複合物結合以激活JAK-STAT 途徑。表達ss469415590ΔG的患者表達完整的蛋白質,而TT 等位基因則導致框移,從而導致IFN-λ4蛋白的消失[Article:23291588]。有趣的是,TT 等位基因與自發或治療誘導的SVR相關,這表明破壞IFNL4是有利的[Articles:23291588, 23712427]。儘管機制尚不清楚,但IFN-λ4的產生與自發或PEG-IFN-α/RBV療法誘導的清除的可能性降低之間的明顯關聯表明,這種新型IFN可能是觀察到的臨床表現型的原因[Article:23291588。與大多數IFN不同,IFN-λ4蛋白的分泌較差,並且有人假設它可能通過阻止其他IFN-λ與IL10RB/IFNLR1受體結合來損害HCV的清除。值得注意的是,ss469415590,但不rs12979860],已在外周血單核細胞中顯示參與刺激IFN-α和IFN-γ-誘導蛋白10(IP-10)mRNA,其高血漿水平與治療失敗相關[Article:23712427]。
由於ss469415590與rs12979860在IFNL3中高度相關,這一新變異對於預測白人患者的治療反應並未提供額外信息。相反,IFNL4僅與rs8099917在白人患者中呈現弱相關,這表明它可能是治療結果的更好預測因子[Articles:24205831, 24308755。同樣,IFNL4基因型可能是非洲祖源患者治療反應的更好預測因子,因為ss469415590與rs8099917的相關性較弱,且與rs12979860]的相關性在這些人群中[Article:23291588]。綜合來看,對ss469415590ΔG功能變異的識別和特徵化代表了闡明HCV清除的基因機制以及IFN多態性在預測HCV治療反應中的作用的新一步。
IFNL3在DAA時代
隨著DAA的引入到HCV治療武器中,出現了一個問題,即IFNL3基因型是否仍然在預測包括這些新藥物的三重作用療法的治療結果中具有相關性。初步數據表明,IFNL3基因型可能仍然有用,但不如傳統的PEG-IFN-α/RBV雙重療法那麼有效[Articles:21628662, 20648473。迄今為止,研究最充分的三重療法是將PEG-IFN-α和RBV與“第一代”蛋白酶抑制劑BOC和TVR結合的療法。在未接受過治療的患者中,接受包括BOC或TVR的三重療法的患者,對於具有有利的rs12979860] CC基因型的患者,治療率分別為80%和90%,而CT(71%和71%)或TT(59%和73%)基因型的患者則較低[Articles:21696307, 21449783, 22626609]。此外,患者表現出更好的病毒反應動力學,並且選擇抗藥性HCV變異的風險較低[Articles:22626609, 23321318。在之前接受過PEG-IFN-α/RBV療法的患者中,IFNL3基因型與那些WHO復發或部分反應者的SVR並無顯著相關,但具有有利的rs12979860] CC基因型的之前無反應者的治療率高於不利基因型的患者[Article:20375406]。
關於最新開發的“第二代”蛋白酶抑制劑,IFNL3基因型對治療反應的影響已顯示較弱,但預計仍將在預測反應中保持有用,特別是在未接受過治療的患者中。例如,IFNL3基因型已被證明與接受三重療法的NS3蛋白酶抑制劑simeprevir的12周治療反應顯著相關[Article:24907225。同樣,rs12979860]被確定為接受NS5B聚合酶抑制劑sofosbuvir與PEG-IFN-α/RBV治療的HCV基因型1、4、5和6患者的獨立治療前預測因子[Article:23944316]。還有建議在新療法的臨床試驗中根據IFNL3基因型對患者進行分層,這將有助於個性化未來的三重療法並優化結果[Article:25114601]
最後,[[KEEP_93