CPIC 指南註解:dapsone、methylene blue、pegloticase、rasburicase、tafenoquine、toluidine blue 與 G6PD 基因
摘要
高風險藥物應避免用於G6PD 缺乏患者,不論是否患有慢性非球形溶血性貧血(chronic non-spherocytic hemolytic anemia, CNSHA)。在G6PD 可變型(Variable)或無法判定 表現型患者中,應在開始藥物治療前進行酶活性測試。
G6PD基因位於X染色體上。因此,一些患者可能只有一個拷貝,而其他患者可能有兩個拷貝。請參閱完整指南以獲取免責聲明、更多詳情和支持證據。
為特定註釋指定基因型或表現型
註釋
此註釋基於擴展的CPIC®指引,針對G6PD基因型的藥物使用。CPIC作者評估了攜帶G6PD變異的患者使用各種藥物的可用證據。
2022年9月
-
擴展的CPIC®指引,針對G6PD基因型的藥物使用已在《Clinical Pharmacology and Therapeutics》期刊中發表。作為該指引的一部分,作者將藥物按其在G6PD缺乏症患者中引起急性溶血性貧血(AHA)的風險進行分類。Dapsone、methylene blue、pegloticase、rasburicase、tafenoquine和toluidine blue被分類為高風險藥物,如指引出版物的表2所示。此指引取代了2014年原始的G6PD和rasburicase指引。
-
這些指引適用於:
- 成人患者
- 兒科患者
-
指引摘錄:
- 「在此CPIC指引中增加了一個步驟,將藥物分為三組:在G6PD缺乏症的情況下可被視為高風險的藥物(因此通常應避免使用),在G6PD缺乏症中被視為中等風險的藥物(因此應謹慎使用),以及可被視為低至無風險的藥物(在G6PD缺乏症患者中不會增加AHA風險,與正常G6PD狀態者相比)。」
- 「為了將藥物分配到風險組別,作者不僅考慮了主要同行評審文獻中的證據強度,還考慮了藥物使用頻率、監管機構警告的存在以及是否存在可能產生活性氧物質並在G6PD缺乏症中促成溶血的機制(補充材料,分配風險等級)」
- 「Rasburicase和pegloticase(高風險藥物) 在G6PD缺乏症中rasburicase和pegloticase的風險類別基於文獻強度(高水平證據)將AHA和高鐵血紅蛋白血症與在G6PD缺乏症情境下使用這些藥物聯繫起來(表S1),尿酸氧化酶的作用機制(產生過氧化氫)(31),以及強烈建議,一致的監管警告(表S3),rasburicase和pegloticase被認為屬於高風險類別。」
- 「治療建議.作為高風險藥物,rasburicase和pegloticase應避免在G6PD缺乏症患者中使用(表3)。然而,對於任何藥物,必須權衡不良反應(AHA和/或高鐵血紅蛋白血症)的風險與高尿酸血症的風險,特別是在預期腫瘤溶解的剛診斷惡性腫瘤患者中。腫瘤溶解綜合症本身可能危及生命,替代的尿酸降低療法,如allopurinol,可能不如rasburicase有效降低尿酸水平,並且具有其他潛在不良反應。」
-
下載並閱讀:
- 擴展的藥物基因體學臨床應用聯盟(CPIC)指引,針對G6PD基因型的藥物使用
- 2022補充材料
- G6PD 基因資訊表
- Drug Resource Mappings
- Pre and Post Test Alerts
- 高風險藥物流程圖
表1:高風險藥物在G6PD 表現型中的推薦治療使用
改編自指引的表1、2和3
| 預測表現型 | 基因型a | 基因型範例b | 影響 | 治療建議 | 建議等級c | 考量 |
|---|---|---|---|---|---|---|
| 正常 | 攜帶一個X染色體,帶有非缺乏(IV類)等位基因 或攜帶兩個非缺乏(IV類)等位基因s |
B, Sao Boria, IV B/B, B/Sao Boria, B/A, IV/IV |
急性溶血性貧血風險低 | 基於G6PD狀態,無理由避免高風險藥物 | 強烈建議 | Tafenoquine的安全性已在G6PD酶活性≥正常的70%時確立 |
| 缺乏 | 攜帶一個X染色體,帶有缺乏(II-III類)等位基因 或攜帶兩個缺乏(II-III類)等位基因s或一個I類等位基因和一個II或III類等位基因 |
A-, Orissa, Kalyan-Kerala, Mediterranean, Canton, Chatham, II, III A-/A-, A-/Orissa, Orissa/ Kalyan-Kerala, Mediterranean/ Mediterranean, Chatham /Mediterranean, Canton/ Viangchan, II/II, II/III, III/III, I/II, I/III |
急性溶血性貧血風險高 | 避免使用高風險藥物 | Methylene blue和toluidine bluef: 中等建議. 所有其他高風險藥物: 強烈建議 |
|
| 嚴重缺乏合併慢性非球形紅細胞溶血性貧血(Deficient with CNSHA) | 攜帶一個X染色體,帶有缺乏(I類)等位基因 或攜帶兩個缺乏(I類)等位基因sd |
Bangkok, Villeurbanne, I Bangkok/Bangkok, Bangkok/Villeurbanne, I/I |
慢性溶血性貧血急性加重的高風險 | 避免使用高風險藥物 | 強烈建議 | 雖然在G6PD 嚴重缺乏合併慢性非球形紅細胞溶血性貧血(Deficient with CNSHA) 表現型個體中沒有發表的數據,但基於G6PD 缺乏個體的證據,有強烈建議理由避免這些藥物 |
| 可變型(Variable)e | 攜帶一個非缺乏(IV類)等位基因和一個缺乏(I-III類)等位基因 | B /Bangkok, B/Mediterranean, B/A-, IV/I, IV/II, IV/III | 可變型(Variable)急性溶血性貧血風險 | 基於G6PD狀態,無理由在標準劑量下避免低至無風險藥物 | 中等建議 | 由於X 染色體聯鎖嵌合現象(X-linked mosaicism),攜帶多於一個X染色體的個體(例如,女性,Klinefelter綜合症患者)和異型合子(Heterozygous)一個非缺乏(IV類)和一個缺乏(I-III類)等位基因可能顯示正常或缺乏 表現型;在此類情況下需要進行酶活性測試以分配G6PD 表現型。 Tafenoquine的安全性已在G6PD酶活性≥正常的70%時確立 |
| 無法判定 | 攜帶至少一個等位基因具有功能尚未確定 | Dagua B/Dagua |
急性溶血性貧血風險未知 | 為確定G6PD狀態,必須測量酶活性。藥物使用應根據基於活性表現型的建議進行指導 | 中等建議 |
CNSHA: 慢性非球形紅細胞溶血性貧血
a WHO分類來自[文章:22293322],其他細節來自[文章:4963040]。I類等位基因s極為罕見;II類和III類等位基因s之間的區分不明確。幾乎所有患者都會攜帶II類、III類或IV類等位基因s
b 由於G6PD 等位基因s數量龐大,除了這裡給出的例子外,還可能存在其他基因型;請參見G6PD 等位基因定義表以獲得更全面的等位基因s列表和G6PD 等位基因功能表以了解其分配的功能(WHO類別)。注意某些實驗室使用“B 等位基因”來指示不攜帶已知I-III類變異的等位基因。G6PD頻率表可用於查閱主要生物地理群體中的G6PD 等位基因s頻率
c 評分方案在指引補充材料的建議強度部分中描述
d 此類基因型從未見過,推測極為罕見
e 由於X 染色體聯鎖嵌合現象(X-linked mosaicism),異型合子(Heterozygous)(通常為女性)攜帶一個非缺乏(IV類)和一個缺乏(I-III 等位基因s)等位基因可能顯示正常或缺乏 表現型。因此很難預測這些個體的表現型(見補充材料,G6PD異合子)
f
2018年9月更新
CPIC作者建議將G6PD A變異分類為IV/功能正常(先前為II-IV/缺乏-功能正常),基於支持功能的新證據[文章:27040960]和[文章:30206300]。此變更已納入G6PD 等位基因定義表
2014年8月
2014年5月在線接受文章預覽,2014年6月11日提前在線發表
- 關於使用藥物基因組學測試來確定是否應進行rasburicase治療的指引已由臨床藥物基因體學實施聯盟(CPIC)在《Clinical Pharmacology and Therapeutics》期刊中發表
- 2014年rasburicase指引摘錄:
- 「如上所述,FDA、EMA和PMDA在G6PD缺乏症患者中禁用rasburicase(32-34)(見表2)。如果基於基因分型可以明確地分配缺乏狀態,那將是使用rasburicase的充分禁忌。然而,由於基因測試的局限性(如上所述),在大多數情況下,必須進行G6PD酶測試以分配G6PD狀態。」
- 這些指引適用於
- 新生兒
- 兒科
- 成人
- 下載並閱讀:
表1:根據G6PD 表現型推薦的rasburicase劑量
改編自2014年指引的表1和表2
| 表現型(基因型)a | 雙倍型範例b | 對表型測量的影響 | rasburicase的劑量建議 | 建議等級 c |
|---|---|---|---|---|
| 正常d。攜帶非缺乏(IV類)等位基因的男性或攜帶兩個非缺乏(IV類)等位基因s的女性 | 男性:B, Sao Boria。女性:B/B, B/Sao Boria | 溶血性貧血風險低或降低 | 基於G6PD狀態,無理由停止rasburicase d | 強烈建議 |
| 缺乏或嚴重缺乏合併慢性非球形紅細胞溶血性貧血(Deficient with CNSHA)。攜帶I、II或III類等位基因的男性,攜帶兩個缺乏 I-III類等位基因s的女性 | 男性:A-, Orissa, Kalyan-Kerala, Mediterranean, Canton, Chatham, Bangkok, Villeurbanne。女性:A-/A-, A-/Orissa, Orissa/Kalyan-Kerala, Mediterranean/Mediterranean, Chatham/Mediterranean, Canton/Viangchan, Bangkok/Bangkok, Bangkok/Villeurbanne | 急性溶血性貧血風險 | rasburicase禁用;替代方案包括allopurinol e | 強烈建議 |
| 可變型(Variable) d,f。攜帶一個非缺乏(IV類)和一個缺乏(I-III變異)等位基因的女性 | B/A-, B/Mediterranean, B/Bangkok | 溶血性貧血風險未知 | 為確定G6PD狀態正常,必須測量酶活性;替代方案包括allopurinol e | 中等建議 |
a「類別」指的是WHO分類,來自[文章:22293322],其他細節來自[文章:4963040]。I類變異極為罕見;II類和III類變異之間的區分不明確;而「V類」非常高活性變異僅在一個案例中報導過[文章:4963040]。因此,幾乎所有患者都會攜帶II類、III類或IV類等位基因s。應注意,變異的類別可能僅根據患者的臨床表現分配,隨後識別出變異
(*) Luzzatto, L. & Poggi, V. 葡萄糖-6-磷酸脫氫酶缺乏症 在:Nathan和Oski的嬰幼兒和兒童血液學,第7版(編輯:Meloni, D., Anderson, A. 書籍作者:Orkin, S.H., Fisher, D.E., Look, A.T., Lux IV, S.E., Ginsburg, D., Nathan, D.G.)(Saunders, Elsevier., 2009)
b 由於G6PD變異數量龐大,除了這裡給出的例子外,還可能存在其他雙倍型;請參見補充表S1以獲得更全面的變異等位基因s列表及其分配的WHO類別
c 評分方案在補充材料中描述(見建議強度材料)
d 陰性或不確定的基因測試不能被認為表示正常的G6PD 表現型;在此類情況下需要進行酶活性測試以分配G6PD 表現型
e allopurinol與攜帶HLA-B*58:01 等位基因的罕見攜帶者的嚴重皮膚反應相關[文章:23232549]
f 由於X 染色體聯鎖嵌合現象(X-linked mosaicism),女性異型合子(Heterozygous)攜帶一個非缺乏(IV類)和一個缺乏(I-III變異)等位基因可能顯示正常或缺乏 表現型。因此很難預測這些個體的表現型(補充材料,G6PD異合子)
圖1:解釋G6PD基因型和評估是否需要酶活性測試的工作流程
圖1來自指引
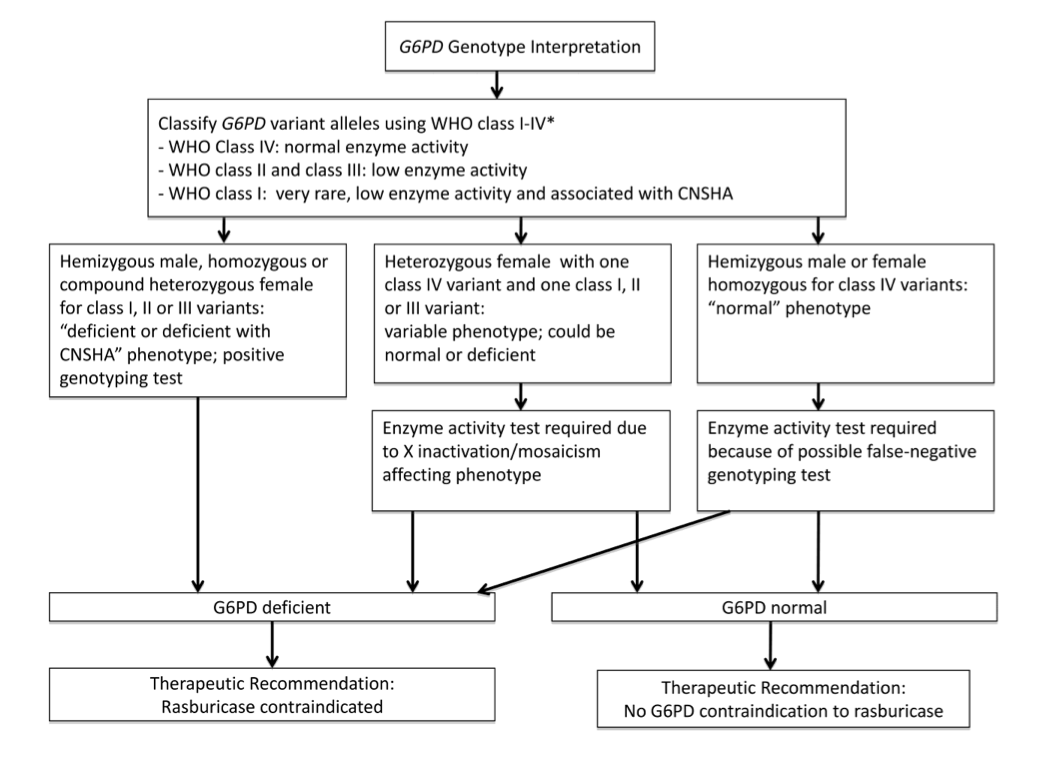
*應注意,變異的類別可能僅根據患者的臨床表現分配,隨後識別出變異[文章:22293322]
methylene blue 途徑, 藥效學
概括
一個風格化的圖示顯示了在紅血球中可能導致亞硝基血紅蛋白產生的機制,以及防止亞硝基血紅蛋白血症的控制機制,包括需要methylene blue治療的NADPH來自五碳磷酸途徑途徑。
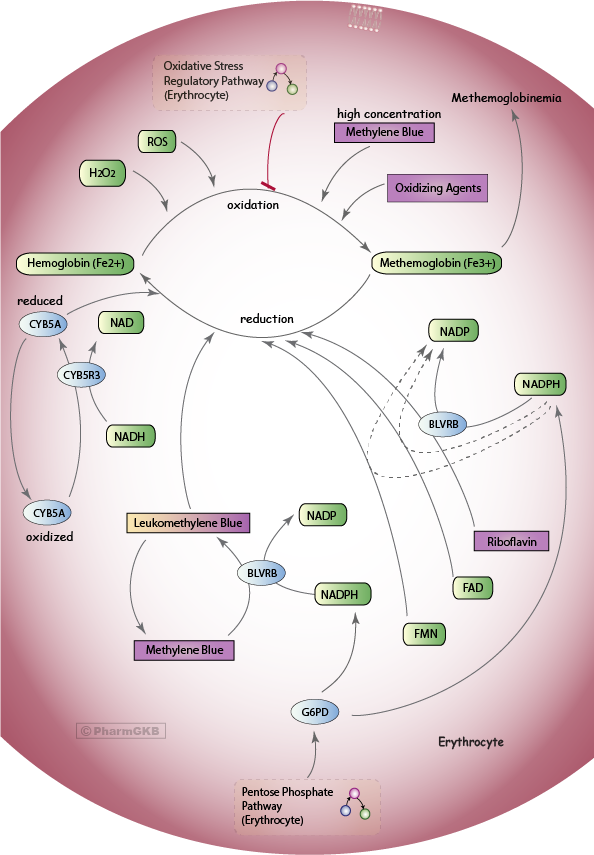
描述
Methylene Blue
Methylene Blue 有多種用途 - in vivo 中,它被 indiCATed 用作藥物引起的高鐵血紅蛋白症的治療,還可用於感染、病理或中毒的治療,以及作為診斷用染料。它也常用作 in vitro 的染料 - 例如作為細胞、組織、DNA、寄生蟲和細菌染色的組成部分 [Articles:21235292, 14714878, 21316815]。臨床使用的例子包括抗瘧疾療法、治療依福沙明引起的神經毒性(儘管治療報告顯示無效)、氰化物中毒的解毒劑、可視化輸卵管或破裂膜、腫瘤標記,甚至作為潛在的敗血性休克、缺血性腦損傷和阿茲海默病的治療 [Articles:14962363, 18840018, 20151259, 17278152, 9605379, 11048840, 17928358, 20731659, 14714878, 20575634, 20959759] (Moldenhauer Brooks, 1936, The Scientific Monthly, 43:585-586)。作為光動力療法,它可用於治療牛皮癬、西尼羅病毒感染、AIDS-相關的卡波西肉瘤、抗生素耐藥性細菌株,以及在輸血前對血液進行去污 [Articles:19180895, 16118025, 16942436, 19193212, 22232515, 14714878]。Methylene Blue 也為藥物開發做出了貢獻,作為其他治療藥物的化學基礎,包括抗瘧藥氯喹、抗組胺藥普羅美嗪和抗精神病藥氯丙嗪 [Article:14714878]。
高鐵血紅蛋白症
高鐵血紅蛋白症是紅血球中高鐵血紅蛋白(MetHb)含量增加的情況 (RBCs) [Articles:22024786, 7073040]。高鐵血紅蛋白(MetHb)是在血紅蛋白中的血基因鐵原子被氧化後形成的,這使其無法再結合氧氣或二氧化碳 [Articles:22024786, 8416301, 7073040, 15862084, 10533013]。正常的MetHb水平在循環紅血球中 (RBCs) 約為1% - 當這些水平增加時,就會發生高鐵血紅蛋白症,這可能是由於遺傳因素(遺傳性)或由外源性氧化劑如治療藥物引起(獲得性) [Articles:22024786, 7073040]。當MetHb達到約15%時會出現青紫症,隨著水平進一步上升,可能會出現組織缺氧 - MetHb水平達到70%或以上可能是致命的 [Article:7073040]。
途徑 描述
Methylene Blue 途徑 專注於血紅蛋白氧化為MetHb的機制,以及保護這一過程或將MetHb還原回血紅蛋白的機制。血紅蛋白在 RBCs 中具有可互換的結構形式,使其能夠在肺部吸收氧氣並釋放二氧化碳,並在組織中釋放氧氣和吸收二氧化碳(在 [Article:9435331] 中有廣泛的回顧)。去氧血紅蛋白是緊張的構象 - 當氧氣結合到一個血基因組時,結構放鬆,對氧氣的親和力增加,使氧氣分子能夠迅速結合剩餘的三個血基因組(氧合血紅蛋白) [Articles:9435331, 8416301]。MetHb是通過將去氧血紅蛋白中的一個或多個血基因鐵原子從亞鐵狀態氧化為鐵三價狀態(Fe2+到Fe3+)而形成的,這一過程由氫過氧化物 (H2O2) 和超氧化物(O2-)等化合物促進 [Articles:22024786, 8416301, 7073040, 15862084, 10533013]。
為了防止MetHb的形成,RBCs 具有幾種不同的機制,這些機制通過還原細胞中的 ROS 來防止MetHb的形成(包括在 氧化壓力調節 途徑 中描述的機制),或通過還原將鐵三價還原回鐵二價 [Articles:7073040, 15862084, 22024786]。主要的 RBC 酶在 in vivo 中還原MetHb的是可溶性細胞色素b5還原酶 (CYB5R3,也稱為 NADH-依賴的MetHb還原酶或二氫酶-1),利用電子供體 NADH 來還原細胞色素b5 (CYB5A),然後再還原MetHb [Articles:22024786, 8416301, 7073040, 18318771, 10533013]。在 CYB5R3 基因中已經發現超過四十種遺傳變異與隱性先天性高鐵血紅蛋白症相關 [Article:18318771]。在乳糖脫氫酶存在的情況下,細胞外 NADH 可以增強人類紅血球中MetHb還原的速率 [Article:15833275]。
第二種酶,黃素還原酶 (NADPH)(也稱為 BLVRB,膽紅素還原酶B,NADPH-MetHb還原酶,NADPH-MetHb-二氫酶)在正常情況下在 RBCs 中進行約5%的這一活動,需要 NADPH 和電子受體輔因子 [Articles:22024786, 7073040, 10533013, 8687377]。riboflavin, FAD 和 FMN 都可以作為電子受體來還原MetHb [Articles:869945, 7400118, 698125]。
藥效學 的 Methylene Blue
另一種對於 BLVRB 的輔因子,能顯著加速MetHb還原的是 Methylene Blue [Articles:22024786, 7073040, 10533013]。Methylene Blue 被 BLVRB 還原為白色 Methylene Blue,接受來自 NADPH 的電子 [Article:7073040]。白色 Methylene Blue 作為電子供體還原MetHb為血紅蛋白,並在循環氧化還原反應中轉換回 Methylene Blue [Articles:7073040, 10533013]。相反,由於 Methylene Blue 是一種氧化劑,在高濃度下,它可能通過氧化血紅蛋白而導致高鐵血紅蛋白症 [Articles:7073040, 10533013]。Methylene Blue 治療的療效可能受到多種因素的影響,例如,苯胺中間體可能會阻止 RBC 吸收 Methylene Blue [Article:12845393]。
藥物基因體學
估計有近3.3億人缺乏 G6PD 酶,最高的發病率出現在非洲、中東和亞洲 [Article:19233695。G6PD 缺乏 個體對於 RBC 由外源性因素如治療藥物引起的氧化壓力更為敏感,因為 NADPH 的產生無法滿足調節機制所需的需求(另見 五碳磷酸 途徑 和 氧化壓力 途徑]) [Articles:7949118, 4154443, 2633878。已識別的 G6PD 基因中的變異(目前 >180)被歸類為 CATegorized 為 WHO 類別 (I-V),根據酶缺乏的程度和它們所引起的臨床表現(另見 G6PD VIP 摘要]) [Articles:22237549, 22293322, 6075369, 5316621, 2633878]。
Methylene Blue 是減少MetHb的有效治療,但在葡萄糖-6-磷酸脫氫酶 (G6PD) 缺乏 個體中與不良反應相關(表1)。藥物 仿單 對於 Methylene Blue 禁忌或建議在 G6PD 缺乏 個體中使用時要謹慎,因為有溶血性貧血和/或高鐵血紅蛋白症的風險。早期 in vitro 研究顯示,與正常 RBCs 相比,與 Methylene Blue 和葡萄糖共同培養的 G6PD 缺乏 RBCs 中MetHb還原的速率顯著降低 [Article:14056871]。然而,這可以通過將 G6PD 缺乏 和“正常” RBCs 一起培養來增加 - 可能是由於白色 Methylene Blue 擴散到 G6PD 缺乏 RBCs [Article:14056871]。
由於依賴於 NADPH,Methylene Blue 治療在 G6PD 缺乏 患者中通常無法有效改善高鐵血紅蛋白症 [Articles:5091568, 9590495, 17444323, 15587250, 18561168, 11418378],並可能在 G6PD 缺乏的個體中加重病情和/或誘導溶血(見表1) [Articles:16493607, 15842651, 5091568, 11048840, 15787927, 22015451, 17444323, 11418378, 15587250, 11824767] [Article:22024786]。事實上,Methylene Blue 無法還原高鐵血紅蛋白的失敗已被開發為 G6PD 缺乏的測試 [Articles:13804322, 13872968]。
表1:在 Methylene Blue 治療後報告的不良反應案例 G6PD 缺乏 個體 | 研究詳情 | 報告的高鐵血紅蛋白症觸發因素 | 隨後 Methylene Blue 治療的後果 | G6PD 缺乏?是否進行測試? | 參考文獻 | | 案例研究,男性成人(菲律賓)患有轉移性腎細胞癌 | Triapine| 出現黃疸、血紅蛋白尿、溶血 | G6PD 缺乏,酶活性測定 | [Articles:16493607, 15842651] | | 案例研究,男性成人(墨西哥裔美國人) | 含有苯胺和甲苯的清潔液 | MetHb水平無變化,第二天出現溶血,可能是由苯胺、甲苯、Methylene Blue(或隨後的維生素C治療)觸發 | G6PD 缺乏 A- 變異,定量和定性酶活性測定 | [Article:5091568] | |報告三名早產新生兒 WHO 在產前接觸 Methylene Blue(兩名男性,一名女性) | 不適用 | 出現嚴重溶血,導致高膽紅素血症,所有人都需要進行換血 | G6PD 缺乏在三例中確認,酶活性測定 | [Article:11048840] | | 案例研究,26個月大的男性 | 指甲去除液(含有硝基乙烷) | MetHb水平僅暫時降低,且 ROS,但通過 RBC 換血得到解決。 | G6PD 缺乏,酶活性,53% HbA,41% HbS 鐮刀型特徵。 | [Article:9590495] | | 案例研究,23歲女性(印度) | 苯胺,還給予維生素C | 無改善。出現溶血並需要輸血。 | G6PD 缺乏,高鐵血紅蛋白還原方法 | [Article:17444323] | | 一名3個月大的 WHO 進行了心臟手術 | 無法確定,但作者討論可能是心肺旁路對酶活性的影響,或甘油三硝酸酯治療,或其他心臟或呼吸原因。 | 給予低劑量 Methylene Blue,持續10分鐘,MetHb水平降低。出現黃疸和輕度血尿,歸因於溶血。 | 先前對部分 G6PD 缺乏的了解 | [Article:15787927] | | 一例案例研究(n=1),40歲男性 | 含有銅-8-羥基喹啉的殺真菌劑。他最初接受了維生素C治療。出現高鐵血紅蛋白症和溶血。 | 給予 Methylene Blue,並持續給予維生素C治療。治療無效,溶血變得更嚴重。 | 潛在的 G6PD 缺乏,以及銅對 G6PD 活性的抑制。活性測定。 | [Article:15587250] | | 一例案例研究,成人,在80名患者的試驗中(未招募已知 G6PD 缺乏的患者) | Rasburicase | MetHb水平降低,但溶血惡化 | 先前未知的 G6PD 缺乏,未報告測試。 | [Article:22015451] | | 一例案例研究,12歲男性(老撾人) | Rasburicase | 治療無效 | G6PD 缺乏,酶活性測試。| [Article:18561168] | | 一例案例研究,一名男性患者(約旦)患有慢性腎衰竭 | 美克洛普拉米德(腎功能受損和細胞色素b5還原酶缺乏也有貢獻) | 也給予維生素C。治療無效,病情惡化,可能出現溶血。患者死亡。 | CYB5R3 缺乏,定量測定,和 G6PD 缺乏,酶活性測定。 | [Article:11418378] | | 一例案例研究,25歲男性 | 苯胺 | 症狀減輕,MetHb水平降低,但幾天後出現溶血性貧血。 | G6PD 缺乏,測定。 | [Article:11824767] | | 一例案例研究,23歲女性進行了lapaROS拷貝 | Methylene Blue(通過子宮頸給予以可視化輸卵管) | 青紫症用維生素C治療,而不是 Methylene Blue | G6PD 缺乏,酶水平 | [Article:9605379] | | n=409名兒童進行基因分型,n=88為 G6PD 缺乏。劑量尋找研究 - 使用氯喹和不同劑量的 Methylene Blue 治療。布基納法索 | 不適用 | 在一名兒童中,血紅蛋白在第5天降至5g/dl以下,在7名兒童中,血紅蛋白值下降 >3g/dl | 在案例中 <5g/dl = G6PD 缺乏 半合子男性。7名中有3名兒童血紅蛋白下降 >3g/dl 為 G6PD 缺乏。基因分型方法或變異未描述 | [Article:17026773] | | 四項隨機對照試驗的合併分析(n=1005名兒童)(包括 PMID: 16179085, 17026773 以上,18286187 和未發表的數據)。一名21個月大的女孩和一名28個月大的男孩,均患有瘧疾 | 不適用 | n=844名兒童接受了 Methylene Blue 與其他抗瘧藥的聯合治療。在這兩名患者中,血紅蛋白水平降至等於或低於5g/dl(indiCATing 嚴重貧血) | 女性為 異型合子(Heterozygous) 的 G6PD A-,男性為半合子(可能是上述 PMID: 17026773 中描述的)。未提供基因分型的具體信息 | [Article:23135803] |
__注意 - 應注意,高濃度的維生素C(抗壞血酸)也與在 G6PD 缺乏 個體中誘導溶血有關 [Articles:1138591, 1976956],但在 治療劑量 中被認為對於 WHO 不具有 WHO I類變異的患者是安全的 [Articles:7949118, 20701405]。
在 Methylene Blue G6PD 缺乏 個體中是否安全?
最近的一項基於證據的回顧得出結論,應避免在 G6PD 缺乏的患者中使用 Methylene Blue 治療,因為有溶血的風險 [Article:20701405],這一結論得到了其他回顧的支持 [Articles:20350285, 7949118, 19769422,意大利 G6PD 缺乏協會,以及 藥物 仿單 。高鐵血紅蛋白症的替代治療包括維生素C,這是一種電子供體,可以還原 ROS,從而抑制MetHb的產生 (氧化壓力調節 途徑]) [Articles:12569111, 22024786, 5091568, 9605379]。然而,Methylene Blue 是比其他選擇(如 riboflavin)更強效且快速的MetHb還原劑 [Article:10809266],而且維生素C治療並不總是有效 [Articles:17444323, 15587250, 11418378],並且需要幾種 NADPH- 依賴的機制來回收氧化的維生素C [Articles:10657232, 9667500, 9405334]。
幾項研究顯示,Methylene Blue誘導的溶血風險與 G6PD 缺乏之間沒有關聯。在一項針對未合併的瘧疾感染使用 Methylene Blue 和氯喹的研究中,24名 G6PD 缺乏的兒童中未觀察到嚴重溶血的案例,這一藥物組合在74名健康的 G6PD 缺乏 男性中也被認為是安全的 [Articles:16179085, 15655011]。這兩項研究均在西非進行,該地區 G6PD 類別 III 變異普遍 [Articles:16179085, 15655011, 16225660]。
因此,是否在 G6PD 缺乏 個體中使用 Methylene Blue 是安全的問題仍然存在爭議。答案可能取決於缺乏的類型,因為 WHO 類別 III G6PD 變異被認為會導致較輕的缺乏,與I類或II類相比 [Articles:22149420, 6075369, 5316621, 2633878, 16179085, 15655011]。然而,反對在這一患者群體中使用 Methylene Blue 的一個論點是,世界上大多數情況下,G6PD 缺乏的測試仍然基於酶活性,而不是基因分型或對潛在變異的特徵描述,因此應對已知 G6PD 缺乏的患者極為謹慎地給予 [Articles:22149420, 19233695。在這裡進行的廣泛文獻回顧中識別的案例研究(表1)中,只有兩篇公開的 CAT 描述了 G6PD 電泳變異(A-)的特徵,而特定的基因變異的基因分型並不總是報告(見 G6PD A- 單倍型]) [Articles:5091568, 23135803]。另一個論點是,儘管先前的看法,G6PD A- 不應被臨床視為“輕微”,因為患者在面對強效藥物時仍然面臨致命的急性溶血性貧血風險 [Article:22993389],並且對於 WHO II類和 III G6PD 變異之間的區分不再具有臨床意義(Luzzatto & Poggi, 2009, Glucose-6-Phosphate Dehydrogenase Deficiency chapter, in Nathan and Oski's Hematology of Infancy and Childhood, 7th Edition)。舉例來說,最近對四項隨機對照試驗的綜合分析觀察到,在半合子/同型合子(Homozygous) 兒童中,與野生型或雜合子相比,血紅蛋白水平顯著但輕微下降(表1) [Article:23135803。這一影響被描述為臨床意義有限(844名兒童中僅有兩名顯示出嚴重貧血,一名 [[P0_6f3a57c]],一名半合子),但建議對 G6PD 患者的不良血液學事件進行監測 [Article:23135803]。
由於白色 Methylene Blue 可能擴散到 G6PD 缺乏 RBCs [Article:14056871],異型合子(Heterozygous) 女性可能在 Methylene Blue誘導的溶血風險中較低,但據我們所知,這一機制尚未被檢查。
其他遺傳因素可能會增加風險 - 例如,缺乏 CYB5R3、CAT 或 GSH 合成酶的個體可能更容易出現藥物誘導的高鐵血紅蛋白症和溶血性貧血 [Articles:11418378, 31928, 6765904, 1999334, 6620333, 5686480, 11167850]。新生兒特別容易出現高鐵血紅蛋白症,因為其 CYB5R3 水平低,CAT 和 GPX1 活性降低 [Articles:8416301, 3780953, 7073040]。其他因素,包括基線血紅蛋白,與寄生蟲水平相關,也可能影響風險 [Article:23135803]。類似於 G6PD,己糖激酶能在氧化壓力條件下(例如治療 Methylene Blue)提高 PPP 的速率,這一點通過在抑制己糖激酶時細胞中未增強的 PPP 速率得以證明 [Article:3415698],而缺乏己糖激酶的患者則表現出非球狀性溶血性貧血 [Article:10474511]。 BLVRB 缺乏在一名 WHO 擁有足夠 G6PD 活性但異常 Methylene Blue 篩查測試的個體中被描述 [Article:4383300]。由於 BLVRB 在 藥效學 中的作用,BLVRB 缺乏 患者的美克洛普拉米德治療可能會失敗,這在 EU藥物 仿單中被禁忌在這些個體中使用 [Articles:7582412, 17122537]。
疾病背景也可能起到作用 - 患有高鐵血紅蛋白症的患者已經在其 RBC 中顯示出氧化壓力的臨床跡象,因此可能更容易出現溶血。作為氧化劑,給予的 Methylene Blue 劑量也應考慮 [Articles:7073040, 10533013]。其他因素,例如瘧疾感染患者的基線血紅蛋白,與寄生蟲水平相關,也可能影響風險 [Article:23135803]。
Methylene Blue 是否會在 G6PD 缺乏 個體中引起溶血,還是引發高鐵血紅蛋白症的藥物?
幾種已知會引發獲得性高鐵血紅蛋白症的藥物也被認為會在 G6PD 缺乏 個體中引起溶血性貧血,例如奎寧、乙醯苯胺和甲苯 [Articles:7073040, 7949118]。因此,很難確定 Methylene Blue 是否是正在接受獲得性高鐵血紅蛋白症治療的 G6PD 缺乏 個體中溶血的原因,而不是前驅藥物,儘管 Methylene Blue 被列為既能引起 G6PD 缺乏 個體的溶血性貧血的藥物,也能引起獲得性高鐵血紅蛋白症 [Articles:7073040, 7949118]。在我們的文獻回顧中,有一項研究顯示在一名 G6PD 缺乏 患者中發展出高鐵血紅蛋白症與 Methylene Blue 相關(表1) [Article:9605379]。
G6PD 缺乏 個體是否也更容易面臨高鐵血紅蛋白症的風險?
G6PD 缺乏 個體可能更容易出現獲得性高鐵血紅蛋白症,儘管在已發表的文獻中這一直接關聯尚不明確。高鐵血紅蛋白症的發展與 G6PD 缺乏有關 [Article:8785565]。Rasburicase(在 G6PD 缺乏 患者中禁忌)在幾例報告的 G6PD 缺乏患者中與高鐵血紅蛋白症和溶血性貧血相關 [Articles:22015451, 18561168, 22190578, 16204390, 22573495, 17387701, 12942574]。G6PD 的缺乏可能通過減少可用的 NADPH 在 RBCs 中來促進獲得性高鐵血紅蛋白症的加重,如上所述,儘管 NADH- 依賴的 CYB5R3 途徑 主導了MetHb的還原 [Articles:7073040, 22024786]。
Oxidative Stress Regulatory 途徑 (紅血球)
概括
一個簡化的圖示,顯示幾種防止紅血球氧化壓力的調控機制,其中許多機制需要來自於 Pentose Phosphate 途徑 的 NADPH。
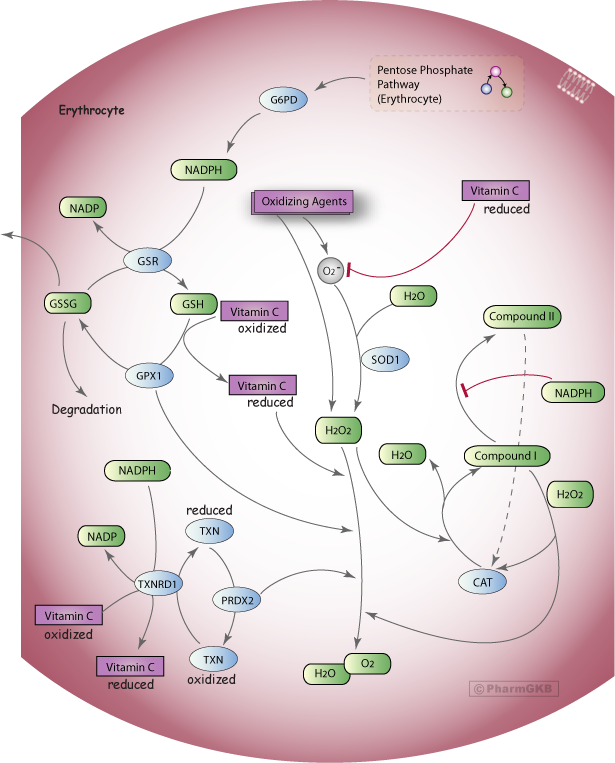
描述
反應性氧物種的釋放 (ROS),例如超氧化物 (O2-) 和/或過氧化物(例如氫過氧化物,H2O2),可以被外源性氧化劑如藥物或其代謝物所觸發 [Articles:2633878, 10533013]。例如,H2O2 是藥物 rasburicase 將尿酸轉化為尿囊素的副產物 [Articles:12646938, 16597166]。紅血球 (RBCs, erythrocytes) 不斷受到氧化壓力的影響,這是由於它們作為氧運輸者的角色以及在循環中接觸外源性物質 [Articles:15862084, 10533013]。Oxidative Stress Regulatory 途徑 專注於一些需要 NADPH 來中和 ROS 的機制,例如 O2- 和 H2O2。
O2- 可以通過超氧化物歧化酶 (SOD1) 轉化為 H2O2 [Articles:20350285, 2633878]。谷胱甘肽還原酶 (GSR) 利用 NADPH 將氧化型谷胱甘肽 (GSSG) 轉化為還原型谷胱甘肽 (GSH) [Articles:18177777, 16204390, 21376665, 17611006, 10657232]。然後,GSH 被谷胱甘肽過氧化酶 (GPX1) 氧化回 GSSG,這是一個循環反應,用於將 2H2O2 中和為 2H20 和 O2 [Articles:18177777, 16204390, 21376665, 17611006, 2633878]。GSH 也通過防止和逆轉氧化來保護血紅蛋白,這種氧化會導致球蛋白鏈之間的二硫化物交聯,並扭曲血紅蛋白結構,可能導致“海因茲小體”的沉澱 [Article:15862084]。具有正常 G6PD 酶活性的 RBCs 其 PPP 活性和 GSH 水準較高,與 G6PD 缺乏 RBCs 相比,然而 缺乏 細胞在正常條件下可以應對低水平的可用 NADPH [Articles:4154443, 2633878]。當氧化壓力發生時,G6PD “正常” RBCs 通過增強 PPP 活性來維持 GSH 水準,而在 G6PD 缺乏 細胞中,PPP 保持在最低容量,GSH 水準下降 [Article:4154443]。由於 PPP 在 G6PD 缺乏 RBCs 中已接近正常條件下可獲得的最大活性速率,因此它們無法應對氧化壓力,並且更容易受到氧化壓力觸發的溶解,這可能導致溶血性貧血 [Articles:4154443, 2633878]。
另一個需要 NADPH 的關鍵系統涉及氧化型硫氧還蛋白 (TXN) 轉化為還原型,這一過程由硫氧還蛋白還原酶 (TXNRD1) 催化,還原的 TXN 隨後被酶過氧化物還原酶用作電子供體,以中和 H2O2 [Articles:18479207, 17611006, 10657232]。在 RBCs 中,過氧化物還原酶 2 (Prx 2, PRDX2) 是最豐富的同種型,並且通過與血紅蛋白結合和穩定血紅蛋白發揮保護作用 [Articles:18479207, 22960070]。PRDX2 的重要性在於缺失小鼠中顯示出形態學 RBC 缺陷,例如海因茲小體,並且在接觸 H2O2 血液樣本時,缺失小鼠的樣本相比於野生型樣本顯示出增強的 MetHb 形成 [Article:12586629]。
GSH 和 TXNRD1 都可以將完全氧化的 vitamin c(去氫抗壞血酸)轉化為其還原型(抗壞血酸),這可以進一步向 O2-、H2O2 和氧自由基捐贈電子和氫 [Articles:10657232, 9667500, 9405334, 11687303]。由於人類無法合成 vitamin c,因此從氧化狀態回收它對於維持 RBC 和抗氧化形式的血漿水準至關重要 [Articles:10657232, 9667500, 9405334]。
CAT酶 (CAT) 也中和 H2O2,涉及形成不同狀態的酶的反應步驟 - NADPH 不是 CAT酶功能活性所必需的,而是防止形成酶的非活性狀態 [Article:17158050]。靜止的 CAT酶(鐵CAT酶)與 H2O2 的第一次反應形成化合物 I 和 H2O,然後與進一步的 H2O2 分子反應使 CAT酶返回靜止狀態並釋放 H2O 和 O2 [Articles:17158050, 22516655]。化合物 I 的還原也可以形成非活性的化合物 II 狀態,該狀態會慢慢自發地恢復為 CAT酶 [Articles:17158050, 22516655。化合物 II 的形成可以通過 NADPH 的產生來防止,該產物由 G6PD 從葡萄糖-6-磷酸生成(見 五碳磷酸 途徑(紅血球)] [Articles:3805001, 8704218, 17158050]。證據表明,NADPH 也可能在延長此狀態的 CAT酶的條件下,將化合物 I 還原回 CAT酶 [Article:17158050]。