CPIC 指南註解:tacrolimus 與 CYP3A5 基因
摘要
CPIC 對於 tacrolimus 的劑量指引建議,對於 CYP3A5 中間型或 廣泛代謝型(Extensive metabolizer) 的患者,起始劑量應增加至建議起始劑量的 1.5 到 2 倍,但總起始劑量不應超過 0.3 mg/kg/day。治療藥物監測(TDM) 也應用於指導劑量調整。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC® 關於 tacrolimus 和 CYP3A5 的指導方針。
2015年7月
2015年3月在線提前發表
-
關於在 tacrolimus 劑量中使用藥物基因組學測試的指導方針已由臨床藥物基因體學實施聯盟(CPIC)於《Clinical Pharmacology and Therapeutics》期刊發表
。 -
這些指導方針適用於:
- 接受腎臟、心臟、肺或造血幹細胞移植的患者。
- 接受肝臟移植且供體和受體CYP3A5基因型相同的患者。
- 兒童:「...對於至少有一個 CYP3A5*1 等位基因的兒童和青少年,建議劑量增加1.5到2倍,隨後進行成人推薦的治療藥物監測(TDM)。」
-
2015年 tacrolimus 劑量指導方針摘錄:
- 「tacrolimus 的血藥濃度強烈建議受CYP3A5基因型的影響,已有大量證據將CYP3A5基因型與表型變異性聯繫起來...在腎臟、心臟和肺移植患者中,超過50項研究發現,具有CYP3A5*1/*1或CYP3A5*1/*3基因型的個體相比於CYP3A5*3/*3基因型的個體,劑量調整後的 tacrolimus 濃度顯著降低...」
- 「那些具有廣泛或中間代謝型(Intermediate metabolizer) 表現型的受體通常需要增加 tacrolimus 劑量以達到治療藥物濃度。我們建議劑量比標準劑量高1.5 - 2倍,但不超過0.3 mg/kg/天,隨後進行[治療藥物監測(TDM)],因為超治療性 tacrolimus 濃度可能會導致動脈血管收縮、高血壓和腎毒性風險。」
-
下載並閱讀:
表1:基於 CYP3A5 表現型的 tacrolimus 劑量建議:
改編自2015年指導方針手稿的表1和表2。
| 可能的表現型 a | 基因型 | 雙倍型的示例b | 對 tacrolimus 藥理學措施的影響 | 治療建議 c | 建議等級 e |
|---|---|---|---|---|---|
| 廣泛代謝型(Extensive metabolizer) (CYP3A5 表達者) | 攜帶兩個功能性等位基因的個體 | *1/*1 | 劑量調整後的 tacrolimus 濃度較低,達到目標 tacrolimus 濃度的機會減少 | 起始劑量增加1.5到2倍於推薦起始劑量d。總起始劑量不應超過0.3mg/kg/天。使用治療藥物監測(TDM)指導劑量調整 | 強烈建議 |
| 中間代謝型(Intermediate metabolizer) (CYP3A5 表達者) | 攜帶一個功能性等位基因和一個非功能性等位基因的個體 | *1/*3, *1/*6, *1/*7 | 劑量調整後的 tacrolimus 濃度較低,達到目標 tacrolimus 濃度的機會減少 | 起始劑量增加1.5到2倍於推薦起始劑量d。總起始劑量不應超過0.3mg/kg/天。使用治療藥物監測(TDM)指導劑量調整 | 強烈建議 |
| 弱代謝型(Poor metabolizer) (CYP3A5 非表達者) | 攜帶兩個非功能性等位基因的個體 | *3/*3, *6/*6, *7/*7, *3/*6, *3/*7, *6/*7 | 較高(“正常”)劑量調整後的 tacrolimus 濃度,達到目標 tacrolimus 濃度的機會增加 | 以標準推薦劑量開始治療。使用治療藥物監測(TDM)指導劑量調整 | 強烈建議 |
a 通常對於其他 CYP 酶,廣泛代謝型(Extensive metabolizer)會被分類為“正常”代謝者,因此,藥物劑量不會根據患者的基因型改變。然而,在 CYP3A5 和 tacrolimus 的情況下,CYP3A5 表達者(即 CYP3A5 廣泛代謝型(Extensive metabolizer) 或 中間代謝型(Intermediate metabolizer))需要更高的推薦起始劑量,而 CYP3A5 非表達者(即 弱代謝型(Poor metabolizer))需要標準推薦起始劑量。
b 可能發現其他罕見變異如CYP3A5*2, *8和*9,這些變異具有功能未知意義。然而,如果存在拷貝的*1,預期表現型將為中間代謝型(Intermediate metabolizer)。
c 此建議包括在腎臟、心臟、肺和造血幹細胞移植患者中使用 tacrolimus,以及供體和受體基因型相同的肝臟移植患者。
d 由於其他臨床因素(例如,藥物相互作用或肝功能),可能需要進一步的劑量調整或選擇替代療法
e 評分方案在2015年補充資料中描述。
Tacrolimus/Cyclosporine 途徑, 藥效學
概括
風格化細胞描繪了tacrolimus和cyclosporine的作用機制,以及被認為與這兩種藥物相互作用的候選基因。
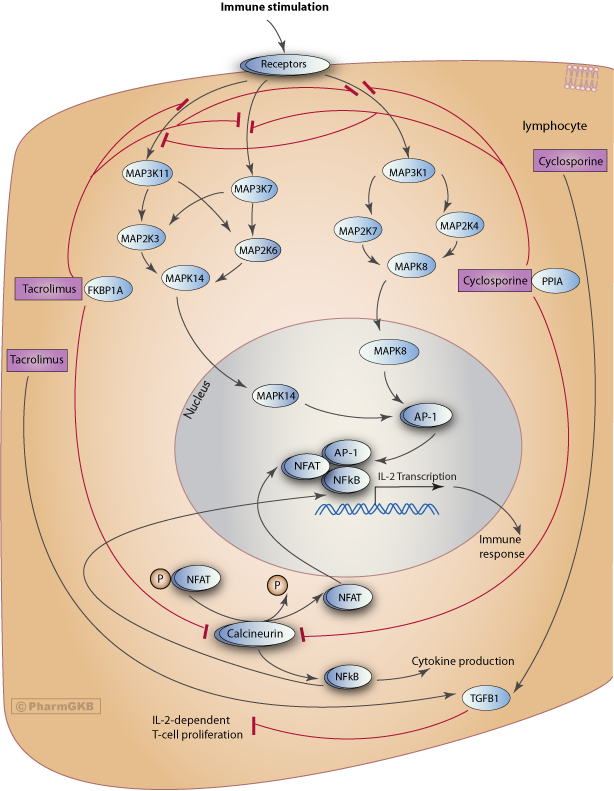
描述
背景
tacrolimus (FK506) 和 cyclosporine (cyclosPORin A, CsA) 是用於固體器官移植受者的基石免疫抑制劑,旨在預防和治療移植物排斥反應。1970年代發現的 cyclosporine 及其在1980年代初進入免疫抑制劑的行列,標誌著醫學上的重大突破。cyclosporine 迄今為止是最成功的抗排斥藥物,顯著提高了移植受者的生存機會。1994年,食品藥品監督管理局 (FDA) 批准了 tacrolimus,這是一種有效的替代藥物,取代了 cyclosporine [Article:15041303。自那時以來,tacrolimus 和 cyclosporine 已成為固體器官移植的主要免疫抑制藥物。根據美國器官採購與移植網絡和科學移植受者登記處的數據顯示,2011年,接受腎臟移植的16,055名患者中,有86%在出院時被處方tacrolimus,而2.4%則被處方cyclosporine。移植一年後,84%和4%的患者分別接受tacrolimus和cyclosporine治療。tacrolimus和cyclosporine的使用在全球範圍內存在差異:2008年來自澳大利亞和新西蘭透析與移植登記處]的數據顯示,391名接受已故腎臟捐贈者移植的澳大利亞患者中,有61%被處方tacrolimus,35%被處方cyclosporine。在移植一年後,這些數字分別變為55%和33%對於tacrolimus和cyclosporine。tacrolimus和cyclosporine也被處方給肝臟、腸道、肺和心臟移植受者,並可用於管理嚴重的自體免疫疾病,如特應性皮炎[Articles:15175770、14522634]和類風濕性關節炎[Articles:15187241,8448639]。
tacrolimus 和 cyclosporine 在化學結構上有所不同:cyclosporine 是一種環狀十一肽[Article:8513650],而 tacrolimus 是一種大環內酯[Article:8588225]。然而,它們的作用方式相似。兩者都是鈣調素抑制劑,其主要作用機制涉及抑制這種重要的磷酸酶[Article:15041303]。tacrolimus 的效果與cyclosporine相似,但濃度低100倍[Article:2445722]。儘管在效能上存在差異,tacrolimus 和 cyclosporine 在多項比較研究中均顯示出優異的移植物存活率(Maes等人的綜述[Article:15041305])。然而,幾項研究顯示,使用tacrolimus與cyclosporine相比,與較低的移植物排斥率相關[Articles:16686762、15741208、16157605]。
藥效學
在淋巴細胞內,tacrolimus 和 cyclosporine 通過多種途徑發揮免疫抑制作用,包括抑制鈣調素和c-JUN N端激酶 (JNK) 和p38 途徑,並誘導轉化生長因子-ß1 (TGF-ß1) 的表達增加。大多數關於tacrolimus和cyclosporine的藥效學研究集中於它們在T細胞中的作用。自然殺手細胞(NK細胞)在移植排斥中的參與尚不明確,但研究發現這兩種藥物以劑量依賴的方式抑制自然殺手細胞的去顆粒化[Article:20967261]。
對鈣調素和NFAT
進入T細胞後,cyclosporine 和 tacrolimus 以高親和力與稱為免疫親和素的蛋白質結合。cyclosporine 主要與環素A(由PPIA基因編碼)結合,這是T細胞內主要的環素,而tacrolimus則與FK-結合,特別是FKBP12(由FKBP1A基因編碼)。這兩種免疫親和素在沒有任何配體的情況下與鈣調素相互作用。然而,藥物結合後,免疫親和素對鈣調素的親和力增強,導致該蛋白質活性的抑制[Article:7529175]。鈣調素是一種鈣調蛋白依賴性磷酸酶,在T細胞激活過程中通過一系列涉及鈣和鈣調蛋白的事件被刺激[Articles:11015619、1377362]。一旦被激活,它會與活化的T細胞核因子(NFAT)家族成員結合並去磷酸化,從而激活這些蛋白質[Articles:10878286、7479966]。激活後,NFAT 蛋白質轉位到細胞核[Article:7479966],與其他轉錄因子(如活化蛋白-1 (AP-1) 家族成員)結合,並與DNA結合以促進白介素-2 (IL-2) 的轉錄[Article:10970869]。它還與多種其他細胞因子基因的啟動子位點結合,包括白介素-4 (IL-4), 白介素-10 (IL-10) 和白介素-17 (IL-17) [Article:20103781]。因此,鈣調素的抑制阻止了其去磷酸化和激活NFAT的能力,影響了在免疫反應中至關重要的細胞因子的轉錄。藥物對IL-2轉錄的影響可能是最明確的機制,這種細胞因子在免疫反應中扮演著重要角色,包括調節性T細胞的維持以及CD4+ 和 CD8+ T細胞的分化和存活[Article:22343569]。
除了NFAT和AP-1家族成員外,活化B細胞的核因子kappa輕鏈增強子(NF-κB)也參與了IL-2轉錄的誘導[Articles:2497518、7546397、20103781]。NF-κB是指一組二聚體轉錄因子,這些因子以同源或異源二聚體的形式結合,對基因轉錄施加正面和負面的影響[Article:22302935]。一般來說,NF-κB對T細胞的發展、穩態、生存和功能有很大影響[Article:21199863。它在T細胞內有多種靶基因,除了[[KEEP_37FDAb36]]外,還參與調節細胞因子,如腫瘤壞死因子-β (TNFβ) [Article:2104232]和干擾素-γ (IFNγ) [Article:9374532]。鈣調素也參與NF-κB的激活。它間接誘導一種稱為IκB的化合物的降解,該化合物與不活化的NF-κB結合並作為抑制蛋白,防止NF-κB與其核靶基因結合。兩種藥物對鈣調素活性的阻斷因此影響了NF-κB對免疫系統基因的作用[Articles:8112299、21199863]。
對JNK和p38 途徑
雖然tacrolimus和cyclosporine對鈣調素的影響可能是研究最深入的機制,但這兩種藥物也被認為參與抑制有絲分裂原活化蛋白激酶(MAPK)途徑。MAPK 途徑是一個信號傳導級聯,涉及多種過程,特別是在免疫系統細胞內[Article:17473844]。它由三種蛋白激酶組成:MAPK、MAPKK和MAPKK-K。MAPKK-K 磷酸化並激活MAPKK,後者又磷酸化並激活MAPK [Article:11274345]。有三個不同的MAPK亞群 - ERK、JNK和p38 [Article:17473844]。cyclosporine和tacrolimus(與其免疫親和素複合)已被證明能抑制JNK (MAPK8) 和p38 (MAPK14) 途徑,但不抑制ERK 途徑。在Jurkat T淋巴細胞中的一項研究顯示,在給予cyclosporine或tacrolimus後,JNK和p38蛋白的水平降低。JNK和p38通過T細胞和CD28共刺激受體的MAPK信號傳導級聯被激活[Article:9575191],並在激活後轉位到細胞核,在那裡它們可以履行各自的角色[Article:12077368]。這包括調節AP-1成員的活性[Article:7622446],這些成員參與促進IL-2 [Article:10970869]和其他細胞因子的轉錄[Article:9468273]。事實上,對p38和JNK 途徑的阻斷已被證明能防止IL-2基因的表達[Article:9575191]。途徑的JNK和p38激活通過各種激酶的作用可以在圖中看到,這兩種藥物被認為抑制途徑在MAPKK-K水平的上游,因為cyclosporine和tacrolimus都被觀察到抑制一種名為MAP3K1的MAPKK-K的激活[Article:11258483]。目前尚不認為鈣調素參與此機制,因為鈣調素的抑制劑已被觀察到阻止NFAT的激活,但不影響JNK或p38 途徑在T細胞內的活化[Article:11258483]。
對TGF-ß1
TGF-ß1是一種對免疫系統細胞調節至關重要的細胞因子。它是TGF-ß家族的一員,該家族還包括TGF-ß2和TGF-ß3。TGF-ß已被證明能抑制IL-2-依賴的T細胞增殖[Article:8423782],並在T細胞內發揮多種其他免疫抑制作用[Article:11905837]。在體內的研究顯示,接受移植的末期腎病患者在接受cyclosporine治療後,TGF-beta1 mRNA和蛋白質表達增加[Article:10071036],而在T細胞中的體外研究也顯示,在給藥後mRNA和蛋白質水平顯著增加[Article:9484745]。然而,這些藥物影響TGF-ß1水平的機制仍需進一步闡明。還需要注意的是,一些研究發現,無論是tacrolimus還是cyclosporine在能成功抑制IL-2產生的濃度下,都無法影響TGF-ß1蛋白或mRNA水平[Articles:12588317、15716327]。因此,目前無法明確指出這兩種藥物是否影響TGF-ß1水平。然而,值得注意的是,除了參與免疫系統外,TGF-ß1還具有纖維生成特性,可能導致腎毒性的發展[Article:19218475]。在腎臟移植患者中的一項研究發現,腎活檢中TGF-ß1 mRNA的表達在存在tacrolimus或cyclosporine腎毒性的患者中增加,與那些出現急性排斥反應的患者相比。這表明,該蛋白質的增加可能導致這些藥物常見的腎毒性[Article:12427154]。
藥物基因體學
大多數藥物基因體學關於tacrolimus和cyclosporine的研究集中於CYP3A4、CYP3A5和ABCB1基因中變異的影響,因為這些基因編碼的酶和轉運蛋白在tacrolimus和cyclosporine的處置中扮演著核心角色。然而,少數研究考察了孕烯X受體基因中的單核苷酸多態性(SNPs)(NR1I2),該受體調節多個基因的表達,包括CYP3A和ABCB1 [Article:23095803]。此外,還有幾項研究考察了POR基因中的SNPs,該基因編碼CYP450氧化還原酶,這是一種負責將電子從NADPH轉移到CYP450酶的蛋白質,使其能夠發揮活性[Article:11371558。幾項研究還考察了TGF-ß1基因(TGFB1)、環素A基因(PPIA)和CYP2C8基因的變異;CYP2C8參與將花生四烯酸(AAs)代謝為環氧二十碳三烯酸(EETs),這些代謝物與維持正常腎功能有關。儘管有這些眾多研究,只有*3 等位基因 (rs776746])在CYP3A5基因中顯示出強烈建議的關聯性tacrolimus 藥物動力學。對於影響tacrolimus 藥效學或cyclosporine 藥物動力學和藥效學的因素,幾乎沒有一致的證據出現。這些研究的整體不一致性可能與種族變異、小樣本量、非特異性藥物代謝動力學測定、結果測量時間的變化以及供體基因型的影響有關,特別是在腎移植患者的腎毒性研究或肝移植患者的藥物代謝動力學研究中。更大規模的研究和綜合分析(Meta-analysis)考慮到種族和供體基因型,可能有助於解決這些變異性問題。
Tacrolimus/Cyclosporine 途徑, 藥物動力學
概括
tacrolimus 和 cyclosporine 代謝的示意圖。
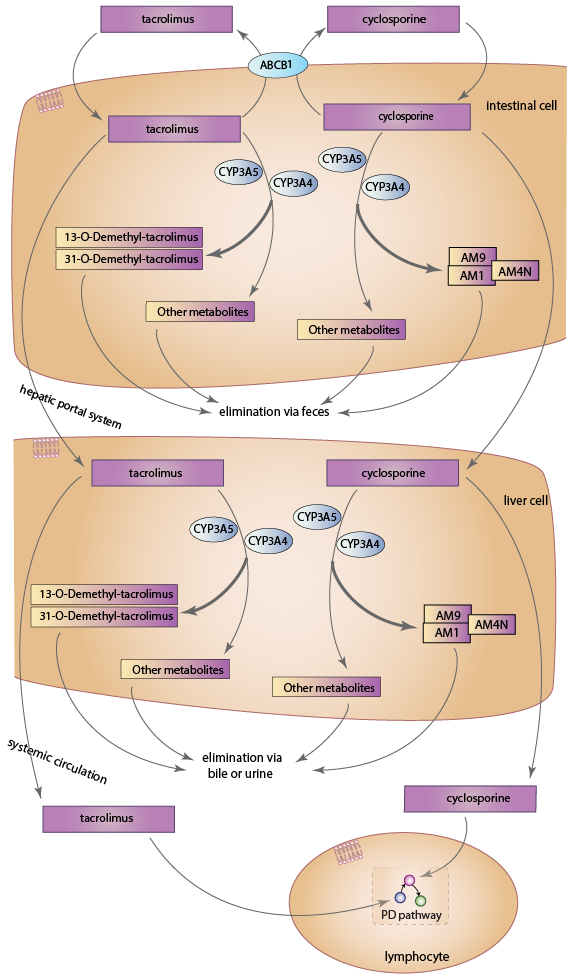
描述
背景
tacrolimus (FK506) 和 cyclosporine (cyclosPORin A, CsA) 是用於固體器官移植受者的基石免疫抑制劑,旨在預防和治療移植物排斥反應。1970年代發現的 cyclosporine 及其在1980年代初進入免疫抑制劑的行列,標誌著醫學上的重大突破。cyclosporine 迄今為止是最成功的抗排斥藥物,顯著提高了移植受者的生存機會。1994年,美國食品藥品監督管理局 (FDA) 批准了 tacrolimus,這是一種有效的替代 cyclosporine [Article:15041303。自那時以來,tacrolimus 和 cyclosporine 已成為固體器官移植的主要免疫抑制藥物。根據美國器官採購與移植網絡和移植受者科學登記處]的數據顯示,2011年,16,055名接受腎臟移植的患者中,有86%在出院時被處方 tacrolimus,而2.4%被處方 cyclosporine。移植一年後,84%和4%的患者分別接受 tacrolimus 和 cyclosporine 治療。全球在 tacrolimus 和 cyclosporine 的使用上存在差異:2008年來自澳大利亞和新西蘭透析與移植登記處的數據顯示,391名接受已故腎臟捐贈者移植的澳大利亞患者中,有61%被處方 tacrolimus,35%被處方 cyclosporine。在移植一年後,這些數字分別變為55%和33%對於 tacrolimus 和 cyclosporine。tacrolimus 和 cyclosporine 也被處方給肝臟、腸道、肺和心臟移植受者,並可用於管理嚴重的自體免疫疾病,如特應性皮炎 [Articles:15175770、14522634] 和類風濕性關節炎 [Articles:15187241、8448639]。
tacrolimus 和 cyclosporine 在化學結構上有所不同:cyclosporine 是一種環狀十一肽 [Article:8513650],而 tacrolimus 是一種大環內酯 [Article:8588225]。然而,它們的作用方式相似。兩者均為鈣調素抑制劑,其主要作用機制涉及抑制這種重要的磷酸酶 [Article:15041303]。tacrolimus 表現出與 cyclosporine 相似的效果,但濃度低100倍 [Article:2445722]。儘管在效能上存在差異,tacrolimus 和 cyclosporine 在多項比較研究中均顯示出優異的移植物生存率(詳見 Maes 等人 [Article:15041305])。然而,幾項研究顯示,使用 tacrolimus 與 cyclosporine 相比,與較低的移植物排斥率相關 [Articles:16686762、15741208、16157605]。
藥物動力學
進入腸上皮細胞後,兩種藥物均由腸道 CYP3A 同工酶代謝,主要是 CYP3A4 和 CYP3A5 [Articles:18978522、22871995]。研究顯示 CYP3A5 是 tacrolimus 代謝的主要酶,CYP3A4 也有貢獻,但其催化效率較低 [Articles:16501005、15951320]。相對而言,cyclosporine 主要由 CYP3A4 代謝 [Article:15450954]。CYP3A 酶家族還包括 CYP3A7 和 CYP3A43 [Article:12406645]。然而,CYP3A7 在 cyclosporine 代謝中的作用尚不清楚 [Article:18978522],且其對 tacrolimus 的親和力和能力較低,這表明它在 tacrolimus 代謝中可能起到的作用有限 [Article:15951320]。同樣,沒有證據支持 CYP3A43 在 cyclosporine 代謝中的參與 [Article:18978522],且其在 tacrolimus 代謝中的作用(如果有的話)尚待闡明 [Article:15244495]。逃避腸道代謝的母藥進入肝臟 POR 系統和肝臟,在那裡 CYP3A4 和 CYP3A5 代謝 tacrolimus 和 cyclosporine [Articles:8689938、1683920]。進入全身循環後,兩種藥物均廣泛結合於紅血球 [Articles:15041303、6129301],只有未結合的藥物能夠進入淋巴細胞並發揮其主要的免疫抑制作用。
最多可形成十五種 tacrolimus 的代謝物 [Article:17965516],其中最常見的是 13-O-Demethyl-tacrolimus [Articles:7507815,15244495]。這種代謝物的活性約為 tacrolimus 的十分之一,而一種次要代謝物 31-O-Demethyl-tacrolimus 被發現具有與 tacrolimus 相當的免疫抑制活性 [Articles:7507815、17965516]。其餘的代謝物均被發現具有弱或微不足道的藥理活性 [Articles:7536652、17965516]。對於 cyclosporine,約形成25種代謝物 [Article:22210099]。血液中發現的主要代謝物為 AM1 和 AM9,這些是羥基化產物,以及 AM4N,這是N-去甲基化的 [Article:22210099]。CYP3A4 能夠將 cyclosporine 轉化為 AM1、AM9 和 AM4N,而 CYP3A5 只將藥物轉化為 AM9 [Article:15450954]。這些代謝物的免疫抑制活性在不同研究中有所變化,但迄今為止所有研究的代謝物活性均低於 cyclosporine [Articles:2137384、1521927]。AM1 具有最高的免疫抑制活性,一些研究發現其活性接近於原始 cyclosporine 的20% [Article:1521927],而其他研究則發現其活性高達80% [Article:2137384]。
tacrolimus 和 cyclosporine 均被廣泛代謝,母藥在尿液和糞便中未改變的比例分別少於0.5% 和1% [Articles:10348790、21151751]。約95%的 tacrolimus 代謝物通過膽道排泄,尿液排泄約占2% [Article:10348790]。同樣,cyclosporine 代謝物主要通過膽道排泄,只有約3%的藥物經腎臟排泄 [Articles:21151751、2587622]。
除了 CYP3A4 和 CYP3A5,外排轉運蛋白 P-糖蛋白也在 藥物動力學 中發揮重要作用 tacrolimus 和 cyclosporine [Article:10837558]。該蛋白由 ABCB1 基因編碼,能將外源性物質從細胞質泵送到細胞外 [Article:9333100]。它存在於細胞的頂面,並已知能轉運 tacrolimus 和 cyclosporine [Article:7681059]。研究發現 P-糖蛋白在小腸絨毛尖端的腸上皮細胞中濃度很高 [Article:10518631],並通過將兩種藥物泵出腸上皮細胞進入腸腔來降低細胞內濃度 [Article:9333100]。除了腸上皮細胞,ABCB1 也在肝細胞內轉運藥物 [Article:16377077] 和腎細胞 [Articles:18518969、9375821]。它還參與淋巴細胞內的藥物轉運 [Articles:1071649917606483],因此,這些細胞內 cyclosporine 和 tacrolimus 的實際濃度可能受到細胞 P-糖蛋白含量的影響。然而,P-糖蛋白在腸上皮細胞中的作用已被更好地表徵,因此僅顯示其在腸道藥物轉運中的參與。腸道 P-糖蛋白的變異約占 cyclosporine 口服清除率變異的17%,其中 P-糖蛋白水平較高的患者觀察到藥物清除率較高。事實上,同一研究得出的結論是,75%的患者間變異可由肝臟中 CYP3A4 活性和腸上皮細胞中 P-糖蛋白的表達變異解釋 [Article:9333100]。對於 tacrolimus,在一項研究中,肝移植後的前7天內,tacrolimus 的濃度/劑量比與腸道 mRNA 水平的 ABCB1 之間存在反比相關 [Article:15919446],而在另一項研究中,肝移植後的前4天內也觀察到了類似的結果 [Article:16413244]。
許多藥物已被報導與 tacrolimus 和 cyclosporine 互動。詳細的清單可參見 van Gelder [Article:12167066]、Christians 等人 [Article:12190331] 和 Campana 等人 [Article:8906896] 的綜述。藥物相互作用主要發生在 tacrolimus 或 cyclosporine 與細胞色素 P450 3A (CYP3A) 或 P-糖蛋白的抑制劑或誘導劑共同給藥時 [Article:12190331],這兩種蛋白在底物特異性上有顯著重疊 [Article:7619215]。
藥物基因體學
大多數關於 tacrolimus 和 cyclosporine 的 藥物基因體學 研究集中於 CYP3A4、CYP3A5 和 ABCB1 基因中變異的影響,因為這些基因編碼的酶和轉運蛋白在 tacrolimus 和 cyclosporine 的處置中扮演著核心角色。然而,少數研究已檢查了編碼孕烯 X 受體的基因中的單核苷酸多態性 (SNPs) 的影響 (NR1I2),該受體調節多個基因的表達,包括 CYP3A 和 ABCB1 [Article:23095803]。此外,還有幾項研究檢查了編碼 CYP450 氧化還原酶的基因中的 SNPs,該酶負責將電子從 NADPH 轉移到 CYP450 酶,從而使其活性得以發揮 [Article:11371558。幾項研究還考察了 TGF-ß1 基因 (TGFB1)、環孢素 A 基因 (PPIA) 和 CYP2C8 基因的變異;CYP2C8 參與將花生四烯酸 (AAs) 代謝為環氧二十烷三烯酸 (EETs),這些代謝物與維持正常腎功能有關。儘管有這麼多研究,只有 *3 等位基因 (rs776746]) 在 CYP3A5 基因中顯示出與 tacrolimus 藥物動力學 的相關性。對於影響 tacrolimus 藥效學 或 cyclosporine 藥物動力學 和 藥效學 的因素,幾乎沒有一致的證據出現。這些研究的整體不一致性可能與種族變異、患者數量少、非特異性藥物動力學測定、結果測量時間的變化以及供體基因型的影響有關,特別是在腎移植患者的腎毒性研究或肝移植患者的藥物動力學研究中。更大規模的研究和 綜合分析(Meta-analysis) 考慮到種族和供體基因型的因素,可能有助於解決這些變異性問題。