CPIC 指南註解:citalopram、escitalopram 與 CYP2C19 基因
摘要
CPIC 劑量指引針對 選擇性血清素再回收抑制劑(SSRI)s citalopram 和 escitalopram 建議,對於 CYP2C19 超快速代謝者、可能的低代謝者和 弱代謝型(Poor metabolizer)s,應考慮選擇一種臨床上適合且不主要由 CYP2C19 代謝的抗抑鬱藥。若 citalopram 或 escitalopram 在臨床上適合,則建議調整劑量。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC® 指南,針對CYP2D6、CYP2C19、CYP2B6、SLC6A4和HTR2A基因型與血清素再攝取抑制劑抗抑鬱藥。這是對先前CPIC® 指南的更新,涉及選擇性血清素再回收抑制劑(SSRI)和CYP2D6及CYP2C19。
2023年2月
- 2015年CPIC® 指南針對選擇性血清素再回收抑制劑(SSRI)和CYP2D6及CYP2C19已更新,納入了更多基因和藥物。現在稱為CPIC® 指南,針對CYP2D6、CYP2C19、CYP2B6、SLC6A4和HTR2A基因型與血清素再攝取抑制劑抗抑鬱藥。2015年1月至2022年6月間發表的有關es-/citalopram和CYP2C19及CYP2D6的文獻已被審查,並更新了建議和補充信息。
- 指南摘錄:
- 「目前數據不足以計算CYP2C19 UMs的初始citalopram或escitalopram劑量,且UMs比NMs有更高的停藥或換藥率(見表S1)。因此,建議CYP2C19 UMs使用不經CYP2C19廣泛代謝的其他臨床適用抗抑鬱藥。」
- 「越來越多的文獻顯示CYP2C19 PMs有較差的臨床結果,包括增加的藥物停用或更換及增加的副作用(見表S1)。為了減少citalopram、escitalopram或sertraline的不良臨床結果,建議CYP2C19 PMs使用不經CYP2C19廣泛代謝的其他臨床適用抗抑鬱藥,或考慮調整劑量。」
- 此指南適用於:
- 成人患者
- 兒科患者
- 下載並閱讀:
表1:基於CYP2C19 表現型的citalopram和escitalopram劑量建議
改編自指南的表1和表3a。
| 表現型 | 基因型 | 例子 | 影響 | 治療 建議 |
建議的 分類 a |
考量 |
|---|---|---|---|---|---|---|
| 超快速代謝型(Ultrarapid metabolizer) | 攜帶兩個功能增強 等位基因的個體。 | *17/*17 | 與CYP2C19快速和正常代謝型(Normal metabolizer)相比,citalopram和escitalopram代謝增加為活性較低的化合物。較低的血漿濃度降低了臨床效益的可能性。 | 考慮使用不經CYP2C19主要代謝的其他臨床適用抗抑鬱藥。如果citalopram或escitalopram臨床適用,且在標準維持nan劑量下未達到足夠的療效,考慮調整至更高的維持劑量。 | 強烈建議 | 藥物交互作用及其他患者特徵(如年齡、腎功能、肝功能)應在調整劑量或選擇替代療法時考慮。 |
| 快速代謝型(Rapid metabolizer) | 攜帶一個功能正常 等位基因和一個功能增強 等位基因的個體。 | *1/*17 | 與CYP2C19 正常代謝型(Normal metabolizer)相比,citalopram和escitalopram代謝增加為活性較低的化合物。較低的血漿濃度降低了臨床效益的可能性。 | 以建議的起始劑量開始治療。如果患者對建議的維持nan劑量反應不佳,考慮調整至更高的維持劑量或轉換至不經CYP2C19主要代謝的其他臨床適用抗抑鬱藥。 | 可選建議 | 藥物交互作用及其他患者特徵(如年齡、腎功能、肝功能)應在調整劑量或選擇替代療法時考慮。 |
| 正常代謝型(Normal metabolizer) | 攜帶兩個功能正常 等位基因的個體。 | *1/*1 | 正常代謝 | 以建議的起始劑量開始治療。 | 強烈建議 | |
| 可能為中間代謝型(Likely intermediate metabolizer) | 攜帶一個功能正常 等位基因和一個降低b功能等位基因或一個功能增強 等位基因和一個降低b功能等位基因或兩個降低b功能等位基因的個體。 | *1/*9, *9/*17, *9/*9 | 與CYP2C19 正常代謝型(Normal metabolizer)相比,代謝減少。較高的血漿濃度可能增加副作用的可能性。 | 以建議的起始劑量開始治療。考慮較慢的劑量調整計劃和較低的維持劑量,與正常代謝型(Normal metabolizer)相比。 | 中等建議 | 藥物交互作用及其他患者特徵(如年齡、腎功能、肝功能)應在調整劑量時考慮。 |
| 中間代謝型(Intermediate metabolizer) | 攜帶一個功能正常 等位基因和一個功能缺失 等位基因或一個功能增強 等位基因和一個功能缺失 等位基因的個體。 | *1/*2, *1/*3, *2/*17, *3/*17 | 與CYP2C19 正常代謝型(Normal metabolizer)相比,代謝減少。較高的血漿濃度可能增加副作用的可能性。 | 以建議的起始劑量開始治療。考慮較慢的劑量調整計劃和較低的維持劑量,與正常代謝型(Normal metabolizer)相比。 | 中等建議 | 藥物交互作用及其他患者特徵(如年齡、腎功能、肝功能)應在調整劑量時考慮。 |
| 可能為弱代謝型(Likely poor metabolizer) | 攜帶一個降低b功能等位基因和一個功能缺失 等位基因的個體。 | *2/*9, *3/*9 | 與CYP2C19正常和中間代謝型(Intermediate metabolizer)相比,citalopram和escitalopram代謝減少為活性較低的化合物。較高的血漿濃度可能增加副作用的可能性。 | 考慮使用不經CYP2C19主要代謝的其他臨床適用抗抑鬱藥。如果citalopram或escitalopram臨床適用,考慮較低的起始劑量、較慢的劑量調整計劃和標準維持劑量的50%減少,與正常代謝型(Normal metabolizer)相比。 | 強烈建議 | 根據FDA警告,CYP2C19 弱代謝型(Poor metabolizer)的citalopram最大建議劑量為20 mg/天,因QT延長風險。FDA產品仿單還警告citalopram劑量應限制在20 mg/天,適用於肝功能不全患者、服用CYP2C19抑制劑的患者和年齡超過60歲的患者。 |
| 弱代謝型(Poor metabolizer) | 攜帶兩個功能缺失 等位基因的個體。 | *2/*2, *2/*3, *3/*3 | 與CYP2C19正常和中間代謝型(Intermediate metabolizer)相比,citalopram和escitalopram代謝減少為活性較低的化合物。較高的血漿濃度可能增加副作用的可能性。 | 考慮使用不經CYP2C19主要代謝的其他臨床適用抗抑鬱藥。如果citalopram或escitalopram臨床適用,考慮較低的起始劑量、較慢的劑量調整計劃和標準維持劑量的50%減少,與正常代謝型(Normal metabolizer)相比。 | 強烈建議 | 根據FDA警告,CYP2C19 弱代謝型(Poor metabolizer)的citalopram最大建議劑量為20 mg/天,因QT延長風險。FDA產品仿單還警告citalopram劑量應限制在20 mg/天,適用於肝功能不全患者、服用CYP2C19抑制劑的患者和年齡超過60歲的患者。 |
| 無法判定 | 攜帶一個或兩個功能尚未確定 等位基因的個體。 | *1/*12, *2/*12, *12/*14 | 無建議 | 無建議 |
a 評分方案描述於補充資料中。 b 有限數據可用於描述功能減弱 等位基因的功能。
2015年8月
2015年5月在線發表
- 關於選擇性血清素再回收抑制劑(SSRI)劑量中使用藥物基因組學測試的指南已由臨床藥物基因體學實施聯盟(CPIC)於《Clinical Pharmacology and Therapeutics》期刊發表。
- 2015年選擇性血清素再回收抑制劑(SSRI)劑量指南摘錄(針對citalopram/escitalopram和CYP2C19):
- 「CYP2C19 超快速代謝型(Ultrarapid metabolizer)與廣泛代謝型(Extensive metabolizer)相比,對這些藥物的暴露顯著降低,因此可能增加治療失敗的可能性。由於數據不足以計算CYP2C19 超快速代謝型(Ultrarapid metabolizer)的初始citalopram或escitalopram劑量,如果考慮其他藥物和臨床因素,可能選擇不經CYP2C19廣泛代謝的替代SSRI。」
- 「在弱代謝型(Poor metabolizer)中觀察到這些藥物的濃度升高,可能增加不良藥物反應的風險。為了可能預防不良反應,應考慮不經CYP2C19廣泛代謝的替代SSRI。如果需要citalopram或escitalopram,應考慮初始劑量減少50%。對於citalopram,FDA建議對CYP2C19 弱代謝型(Poor metabolizer)劑量減少50%(或成人最大劑量為20 mg/天),因QT延長風險(FDA建議不適用於escitalopram)。」
- 「指南中的建議主要適用於基於基因測試的行動;藥物相互作用和其他臨床因素對SSRI的處方決策有重大影響,應在開始藥物治療前考慮。」
- 「描述CYP2D6或CYP2C19基因型與SSRI系統暴露或穩定狀態(Steady state)血漿濃度之間關係的數據在兒科患者中稀少...CYP2C19活性在兒童中可能相對於成人增加;因此,這些建議在兒童中應謹慎使用,並伴隨密切監測。」
- 下載並閱讀:
表1:基於CYP2C19 表現型的citalopram和escitalopram劑量建議:
改編自2015年指南手稿的表1和表3a。
| 可能表現型 | 基因型 | CYP2C19 雙倍型的例子 | 對citalopram/escitalopram代謝的影響 | 治療建議 | 建議等級 a |
|---|---|---|---|---|---|
| 超快速代謝型(Ultrarapid metabolizer)(約5-30%的患者)b | 攜帶兩個功能增強 等位基因或一個功能正常 等位基因和一個功能增強 等位基因的個體 | *17/*17, *1/*17 | 與廣泛代謝型(Extensive metabolizer)相比,代謝增加。較低的血漿濃度將增加藥物治療失敗的可能性。 | 考慮使用不經CYP2C19主要代謝的替代藥物。c | 中等建議 |
| 廣泛代謝型(Extensive metabolizer)(約35-50%的患者) | 攜帶兩個功能正常 等位基因的個體 | *1/*1 | 正常代謝 | 以建議的起始劑量開始治療。 | 強烈建議 |
| 中間代謝型(Intermediate metabolizer)(約18-45%的患者) | 攜帶一個功能正常 等位基因或一個功能增強 等位基因和一個功能缺失 等位基因的個體 | *1/*2, *1/*3, *2/*17 d | 與廣泛代謝型(Extensive metabolizer)相比,代謝減少。 | 以建議的起始劑量開始治療。 | 強烈建議 |
| 弱代謝型(Poor metabolizer)(約2-15%的患者) | 攜帶兩個功能缺失 等位基因的個體 | *2/*2, *2/*3, *3/*3 | 與廣泛代謝型(Extensive metabolizer)相比,代謝大幅減少。較高的血漿濃度可能增加副作用的可能性。 | 考慮減少50%e,f的建議起始劑量並根據反應調整劑量,或選擇不經CYP2C19主要代謝的替代藥物。c | 中等建議 |
a 評分方案描述於補充資料中。
b CYP2C19代謝者狀態頻率基於平均多族裔頻率。
c 藥物交互作用及其他患者特徵(如年齡、腎功能、肝功能)應在選擇替代療法時考慮。
d *2/*17基因型的預測代謝者表現型為臨時分類。目前可用的證據顯示CYP2C19*17 功能增強 等位基因無法完全補償功能缺失 CYP2C19*2。參見補充材料以獲取更全面的預測代謝者表現型列表。
e 根據FDA警告,CYP2C19 弱代謝型(Poor metabolizer)的citalopram最大建議劑量為20 mg/天,因QT延長風險。FDA產品仿單還警告citalopram劑量應限制在20 mg/天,適用於肝功能不全患者、服用CYP2C19抑制劑的患者和年齡超過60歲的患者。
f Stingl等人計算/估算的口服清除率差異百分比對應的劑量調整百分比。[文章:22565785].
Citalopram and Escitalopram 途徑, 藥物動力學
概括
藥物動力學 的 選擇性血清素再回收抑制劑(SSRI) citalopram。
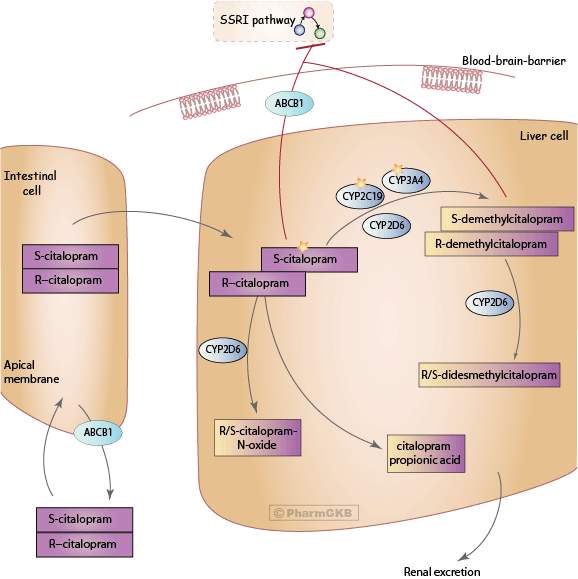
描述
抑鬱症、焦慮症及與癡呆相關的行為障礙已被連結至血清素神經傳導功能的失調 [Article:11336616].
citalopram 是一種 選擇性血清素再回收抑制劑(SSRI) (SSRI)。 SSRI 的分子靶點是 SLC6A4,這導致血清素在突觸間隙的再攝取受到抑制,如同在 SSRI 途徑 中所見。
經口給藥後,citalopram 迅速被吸收,約在 1-4 小時後達到峰值血漿濃度,且給藥後的血漿半衰期約為 35 小時 [Articles:729609, 6939299, 17722014]。 作為一種取代的鄰苯二甲酸酯衍生物,citalopram 是一種高度脂溶性的化合物,並具有一個手性中心 [Article:10507507]。 由於其高脂溶性,citalopram 在經口給藥後的生物利用度約為 80% [Article:17722014]。 約 12% 至 23% 的經口劑量 citalopram 以未改變的 citalopram 形式排泄於尿液中,約 10% 則以糞便排泄 [Article:8732438].
citalopram 及其 N-去甲基化代謝物以外消旋化合物的形式存在。體外及體內測試顯示,citalopram 和 N-demethylcitalopram 的效果主要或完全是由 S-對映體引起的:S-citalopram 和 S-demethylcitalopram [Article:1632943]。 在其體外對血清素攝取的抑制中,S-citalopram 和 S-demethylcitalopram 分別比 R-對映體強效 167 倍和 6.6 倍 [Article:1632943]。 與 citalopram 相比,demethylcitalopram 穿越血腦屏障的能力較差 [Article:9571301].
S-citalopram 是 escitalopram 的活性成分,這是另一種可用的 SSRI [Article:17426664]。 在某種程度上,R-citalopram 抵消了 S-citalopram 對映體的增強血清素作用 [Article:16918708]。 因此,escitalopram 是比 citalopram 更有效的抗抑鬱劑,因為後者是 S-citalopram 和 R-citalopram 的混合物。
citalopram 的兩個對映體均由肝臟細胞色素 P450 系統代謝。R/S-demethylcitalopram 的形成由同工酶 CYP2C19, CYP3A4, 和 CYP2D6 催化 [Articles:10507506, 10494454]。 隨後的 N-去甲基化至 R/S-didesmethylcitalopram 是由 CYP2D6 媒介 [Articles:9110356, 10575324, 7581865]。 R/S-citalopram 的清除是立體特異性的 擇期 [Articles:8986013, 17722014, 9366029]。 在人類肝臟微粒體的體外研究中,CYP2C19, CYP3A4, 和 CYP2D6 都促進生物活性 S-對映體的轉化 [Articles:10575324, 17722014]。 給予外消旋化合物會產生 R- 和 S-立體異構體的不同 穩態濃度(Css)。此外,還觀察到 N-氧化和去胺反應,分別導致 R/S-citalopram N-氧化物和 citalopram propionic acid 代謝物 [Articles:16470634, 9698084]。 N-氧化步驟也由 CYP2D6 媒介 [Article:10575324].
根據體外和體內研究,Citalopram and Escitalopram 對主要 CYP 酶的影響最小 [Articles:10507506, 12387707] citalopram 是一種弱 CYP2D6 抑制劑,對 CYP1A2, CYP2C19, 和 CYP3A4 的影響微弱或無影響 [Article:18691982]。 demethylcitalopram 是 CYP2D6 的抑制劑,其效能比 citalopram 高一個數量級,並可能介導該藥物與其他由此同工酶代謝的藥物之間的輕微相互作用 [Article:9571301].
幾篇出版物顯示,citalopram 的血漿濃度受到 CYP2C19 變異體的影響。弱代謝型(Poor metabolizer) 的 CYP2C19 具有降低 citalopram 的清除率 [Articles:16418702, 17625515, 12968986, 8451774, 12975335, 16855453]。 具有超快速 CYP2C19 等位基因 的患者 S-citalopram 的血清濃度較低 [Article:17625515]。 有證據顯示,CYP2D6 弱代謝型(Poor metabolizer) 基因型與 CYP2C19 弱代謝型(Poor metabolizer) 基因型的組合可以增加 citalopram 的半衰期;在一名患者中,這導致了嚴重的不良反應 [Article:2968986]。 在另一項研究中,7 名對 citalopram 無反應的患者中有 6 名被基因分型為 廣泛代謝型(Extensive metabolizer) 的 CYP2D6 和 CYP2C19 [Article:8986013]。 正如這些研究明確指出的,藥物動力學 的 citalopram 受到 CYP2D6 和 CYP2C19 基因型的影響,但臨床相關的效果在不同研究之間變化很大 [Articles:16855453, 18382661].
citalopram 是 ABCB1 的底物,並由該蛋白質從大腦中主動運輸。citalopram 在擁有 2677TT (rs2032583) 基因型的 ABCB1 人群中的療效可能會降低 [Articles:18215618, 18940259],儘管另一項研究未確認此結果 [Article:18382661].
選擇性血清素再回收抑制劑(SSRI) 途徑, 藥效學
概括
參與血清素合成、釋放、再攝取及介導抗憂鬱劑 選擇性血清素再回收抑制劑(SSRI)在人類大腦中作用的基因。
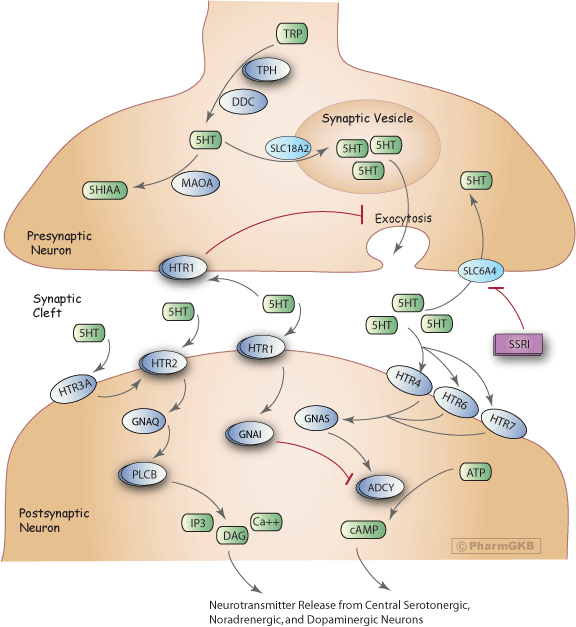
描述
血清素(5-羥色胺,5-HT)是一種神經傳導物質,影響多個過程,包括自主功能、運動活動、荷爾蒙分泌、認知以及與情感、情緒和獎勵相關的複雜過程[Article:17046718]。
在血清素能神經元的末端軸突中,自由色氨酸(TRP)被轉化為5-HT[Article:11590474]。5-HT的合成是一個由色氨酸羥化酶(TPH)和芳香族脫羧酶(DDC)催化的兩步驟過程。TPH是限速酶,存在兩種同工型TPH1和TPH2。在神經組織中,TPH2同工型是主要形式[Articles:12511643, 16581041]。5-HT的攝取進入突觸前儲存囊泡是由囊泡單胺轉運蛋白(SLC18A2)介導的。該轉運蛋白利用囊泡膜上的質子梯度將血清素積累到突觸囊泡中[Article:9665836]。未儲存於囊泡中的5-HT則被單胺氧化酶A(MAOA)降解為5-羥基吲哚乙酸(5-HIAA)。
動作電位刺激突觸前囊泡中血清素的鈣依賴性外排,釋放至突觸間隙,並與突觸後和突觸前受體相互作用。在突觸前側,5-HT激活5-羥色胺(血清素)受體1A(HTR1A)、B(HTR1B)和D(HTR1D),導致5-HT外排的減弱[Article:11590474]。這一反饋迴路調節突觸間隙中的5-HT濃度,因此影響突觸後膜上各種HTR受體亞類的刺激程度[Article:8480026]。長期使用選擇性血清素再回收抑制劑(SSRI)會使這些反饋迴路失去敏感性,從而削弱其對血清素能神經傳導的調節作用[Article:8221701]。突觸後HTR1受體(HTR1A、HTR1B、HTR1D、HTR1E、HTR1F)與HTR2受體亞型(HTR2A、HTR2C)共同作用,通過激活第二信使級聯來介導效應信號[Article:11590474]。在突觸後,訊息傳遞途徑對HTR1受體亞型的主要信號鏈接是通過Gi/o蛋白α亞單位(GNAI)的耦合來實現的。這一相互作用通過抑制腺苷酸環化酶(ADCY)來降低環狀AMP的形成[Article:16896947]。在與5-HT相互作用後,HTR2受體亞群的主要信號鏈接是通過耦合Gq/11蛋白α(GNAQ)來激活磷脂酶C(PLCB)[Article:16896947]。PLCB催化肌醇-1, 4, 5-三磷酸(IP3)和二酸甘油(DAG)的形成[Article:11916537]。突觸後的離子型HTR3受體是一種陽離子特異性配體門控離子通道,並不激活第二信使系統[Article:18466097]。5-HT與此受體的結合通過鈉的內流和鉀的外流使突觸後膜去極化,這被認為會影響HTR2受體的激活[Article:11590474]。HTR4、HTR6和HTR7主要耦合Gs蛋白α(GNAS),導致腺苷酸環化酶的激活,從而增加環狀AMP的水平[Article:11916537]。進一步的操作多樣性得益於多種HTR的剪接和編輯變異的存在、輔助蛋白和伴護蛋白的可能調節,以及它們在GPCR和配體門控通道層面形成同源或異源聚合物的潛力[Article:18571247]。
所有這些第二信使信號在進一步下游反應中的放大導致通過調節鉀通道、幾種蛋白激酶和其他鈣依賴性信號來介導來自中樞血清素能、去甲腎上腺素能和多巴胺能神經元的神經傳導物質釋放。
慢性使用抗抑鬱劑治療已被報導通常會增加腦源性神經生長因子(BDNF)的表達,這是一種依賴於活動的分泌蛋白,對神經網絡的組織和突觸可塑性至關重要[Articles:18433734, 19403460]。
溶質運輸蛋白家族6(神經傳導物質轉運蛋白,血清素),成員4(SLC6A4)負責終止突觸間隙中5-HT的作用。釋放的血清素通過這種整合膜蛋白被運輸回突觸前末端。SLC6A4是Na+/Cl--依賴性轉運蛋白家族的成員[Article:14642278]。
目前存在四大類抗抑鬱藥物:單胺氧化酶抑制劑、選擇性血清素再回收抑制劑(SSRI)、三環化合物和非典型抗抑鬱藥[Article:8221701]。迄今為止,尚未建立針對這些療法的全面假說來解釋其抗抑鬱作用[Article:12726882]。儘管如此,這些藥物都有一個或多個主要的分子靶點以發揮作用。SSRI的分子靶點是SLC6A4,導致抑制突觸前從突觸間隙中5-HT的再攝取。五種SSRI(fluoxetine、fluvoxamine、paroxetine、sertraline和citalopram)在其藥理特徵上有所不同,導致對特定患者的療效或副作用特徵的差異[Articles:10674711, 19370626, 18308785]。SSRI對5-HT再攝取轉運蛋白具有高親和力,對去甲腎上腺素再攝取轉運蛋白具有低親和力,對神經傳導物質受體則具有非常低的親和力。
目前的抗抑鬱療法需要持續治療2-4週才能有效的觀察結果,這表明血清素能和去甲腎上腺素能神經傳導及下游神經適應(例如BDNF受體訊息傳遞途徑)的適應性變化,而不僅僅是突觸單胺水平的升高,才是其治療效果的原因[PMID:19522734, 19481572]。
幾種基因多態性已與治療SSRI反應及不良反應相關,包括SLC6A4、HTR1A、HTR2A、HTR3B、TPH、BDNF和G蛋白β3亞單位的基因變異[Articles:18466097, 19403460, 15111987, 19558256]。