CPIC 指南註解:voriconazole 與 CYP2C19 基因
摘要
CPIC 對於 voriconazole 的劑量指引建議,在 CYP2C19 超快速代謝型(Ultrarapid metabolizer)、快速代謝型(Rapid metabolizer) 或 弱代謝型(Poor metabolizer) 的成人中,應選擇不依賴 CYP2C19 代謝的替代藥物。在兒科患者中,對於 超快速代謝型(Ultrarapid metabolizer) 或 弱代謝型(Poor metabolizer) 的患者,應使用替代藥物。在兒科 快速代謝型(Rapid metabolizer) 中,治療應以建議的標準劑量開始,然後應使用治療劑量監測來調整劑量以達到治療 血清谷濃度(Ctrough)。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC® 指南,針對voriconazole和CYP2C19。
2016年12月
-
關於在voriconazole劑量中使用藥物基因組學測試的指南已由《Clinical Pharmacology and Therapeutics》期刊中的藥物基因體學臨床應用聯盟(CPIC)發佈。
-
這些指南適用於:
- 成人患者(見下表1)
- 兒科患者(見下表2)
-
下載並閱讀:
表1:基於CYP2C19 表現型的成人患者voriconazole治療劑量建議
改編自2016年指南手稿的表1和表2。
| 可能的表現型 | 基因型b | 雙倍型的例子 | 對藥理措施的影響 | 治療建議 | 建議等級e |
|---|---|---|---|---|---|
| 超快速代謝型(Ultrarapid metabolizer)(約2-5%的患者)a | 攜帶兩個功能增強 等位基因的個體 | *17/*17 | 對於識別出超快速代謝型(Ultrarapid metabolizer)基因型的患者,使用標準劑量達到治療性voriconazole濃度的可能性很小。 | 選擇不依賴CYP2C19代謝的替代藥物作為主要治療,而不是voriconazole。此類藥物包括isavuconazole、脂質體兩性黴素B和posaconazole。f | 中等建議g |
| 快速代謝型(Rapid metabolizer)(約2-30%的患者)a | 攜帶一個功能正常 等位基因和一個功能增強 等位基因的個體 | *1/*17 | 對於識別出快速代謝型(Rapid metabolizer)基因型的患者,使用標準劑量達到治療性濃度的可能性適中。 | 選擇不依賴CYP2C19代謝的替代藥物作為主要治療,而不是voriconazole。此類藥物包括isavuconazole、脂質體兩性黴素B和posaconazole。f | 中等建議 |
| 正常代謝型(Normal metabolizer)(約35-50%的患者)ca | 攜帶兩個功能正常 等位基因的個體 | *1/*1 | 正常的voriconazole代謝 | 以推薦的標準護理劑量開始治療。f | 強烈建議 |
| 中間代謝型(Intermediate metabolizer)(約18-45%的患者)a | 攜帶一個功能正常 等位基因和一個功能缺失 等位基因或一個功能缺失 等位基因和一個功能增強 等位基因的個體 | *1/*2, *1/*3, *2/*17d | 與正常代謝型(Normal metabolizer)相比,voriconazole的劑量調整後血清谷濃度(Ctrough)較高。 | 以推薦的標準護理劑量開始治療。f | 中等建議 |
| 弱代謝型(Poor metabolizer)(約2-15%的患者)a | 攜帶兩個功能缺失 等位基因的個體 | *2/*2, *2/*3, *3/*3 | 與血清谷濃度(Ctrough)相比,voriconazole的劑量調整後血清谷濃度(Ctrough)較高,且可能增加不良事件的概率。 | 選擇不依賴CYP2C19代謝的替代藥物作為主要治療,而不是voriconazole。此類藥物包括isavuconazole、脂質體兩性黴素B和posaconazole。f 如果根據臨床建議,voriconazole被認為是最合適的藥物,對於具有弱代謝型(Poor metabolizer)基因型的患者,應以低於標準劑量的劑量謹慎給予voriconazole。治療藥物監測(TDM)。 | 中等建議 |
a 參見CYP2C19頻率表,了解特定種族的等位基因和表現型頻率。
b 等位基因功能的分配,參見CYP2C19 等位基因功能表。
c 根據CPIC術語標準化項目,在所有新的和更新的CPIC指南中,將使用術語"正常代謝型(Normal metabolizer)"代替術語"廣泛代謝型(Extensive metabolizer)"。
d 對於*2/*17基因型的預測代謝者表現型是一個臨時分類。目前可用的證據表明,CYP2C19*17 功能增強 等位基因無法完全補償功能缺失 CYP2C19*2(Sibbing 等,2010)。有關預測代謝者表現型的更全面列表,請參見2016年補充文件。
e 評分方案在2016年補充文件中描述
f 由於其他臨床因素,如藥物相互作用、肝功能、腎功能、物種、感染部位、TDM和合併症,可能需要進一步調整劑量或選擇替代療法。
g 建議基於從CYP2C19*1/*17基因型患者中推斷的數據
表2:基於CYP2C19 表現型的兒科患者voriconazole治療劑量建議
改編自2016年指南手稿的表1和表3。
| 可能的表現型 | 基因型b | 雙倍型的例子 | 對藥理措施的影響 | 治療建議 | 建議等級e |
|---|---|---|---|---|---|
| 超快速代謝型(Ultrarapid metabolizer)(約2-5%的患者)a | 攜帶兩個功能增強 等位基因的個體 | *17/*17 | 對於識別出超快速代謝型(Ultrarapid metabolizer)基因型的患者,達到治療性voriconazole濃度的可能性很小。 | 選擇不依賴CYP2C19代謝的替代藥物作為主要治療,而不是voriconazole。此類藥物包括脂質體兩性黴素B和posaconazole。f,g | 中等建議 |
| 快速代謝型(Rapid metabolizer)(約2-30%的患者)a | 攜帶一個功能正常 等位基因和一個功能增強 等位基因的個體 | *1/*17 | 對於識別出快速代謝型(Rapid metabolizer)基因型的患者,達到治療性濃度的可能性可變型(Variable)。 | 以推薦的標準案例劑量開始治療。f 使用治療劑量監測來調整劑量以達到治療性血清谷濃度(Ctrough)。g,h | 中等建議 |
| 正常代謝型(Normal metabolizer)c(約35-50%的患者)a | 攜帶兩個功能正常 等位基因的個體 | *1/*1 | 正常的voriconazole代謝 | 以推薦的標準護理劑量開始治療。f | 強烈建議 |
| 中間代謝型(Intermediate metabolizer)(約18-45%的患者)a | 攜帶一個功能正常 等位基因和一個功能缺失 等位基因或一個功能缺失 等位基因和一個功能增強 等位基因的個體 | *1/*2, *1/*3, *2/*17d | 與正常代謝型(Normal metabolizer)相比,voriconazole的劑量調整後血清谷濃度(Ctrough)較高。 | 以推薦的標準護理劑量開始治療。f | 中等建議 |
| 弱代謝型(Poor metabolizer)(約2-15%的患者)a | 攜帶兩個功能缺失 等位基因的個體 | *2/*2, *2/*3, *3/*3 | 與血清谷濃度(Ctrough)相比,voriconazole的劑量調整後血清谷濃度(Ctrough)較高,且可能增加不良事件的概率。 | 選擇不依賴CYP2C19代謝的替代藥物作為主要治療,而不是voriconazole。此類藥物包括脂質體兩性黴素B和posaconazolef,i。如果根據臨床建議,voriconazole被認為是最合適的藥物,對於具有弱代謝型(Poor metabolizer)基因型的患者,應以低於標準劑量的劑量謹慎給予voriconazole。治療藥物監測(TDM)。 | 中等建議i |
a 參見CYP2C19頻率表,了解特定種族的等位基因和表現型頻率。
b 等位基因功能的分配,參見(CYP2C19 等位基因功能表)。
c 根據CPIC術語標準化項目,在所有新的和更新的CPIC指南中,將使用術語"正常代謝型(Normal metabolizer)"代替術語"廣泛代謝型(Extensive metabolizer)"。
d 對於*2/*17基因型的預測代謝者表現型是一個臨時分類。目前可用的證據表明,CYP2C19*17 功能增強 等位基因無法完全補償功能缺失 CYP2C19*2(Sibbing 等,2010)。有關預測代謝者表現型的更全面列表,請參見2016年補充文件。
e 評分方案在2016年補充文件中描述
f 由於其他臨床因素,如藥物相互作用、肝功能、腎功能、物種、感染部位、TDM和合併症,可能需要進一步調整劑量或選擇替代療法。
g 在兒科人群中,對於超快速和快速代謝型(Rapid metabolizer) 表現型,及時達到voriconazole治療濃度是困難的。由於達到治療濃度可能會失去關鍵時間,建議使用替代抗真菌藥物,以便兒童能夠盡快接受有效的抗真菌治療。
h 對快速代謝型(Rapid metabolizer)進行細緻的治療藥物監測(TDM)是至關重要的。由於血清谷濃度(Ctrough)的變異性很大,目前尚無足夠證據區分CYP2C19*1/*17和*1/*1的兒科患者。
i 建議基於從成人中推斷的數據。
Voriconazole 途徑, 藥物動力學
概括
途徑 描述了 Voriconazole 的代謝過程。
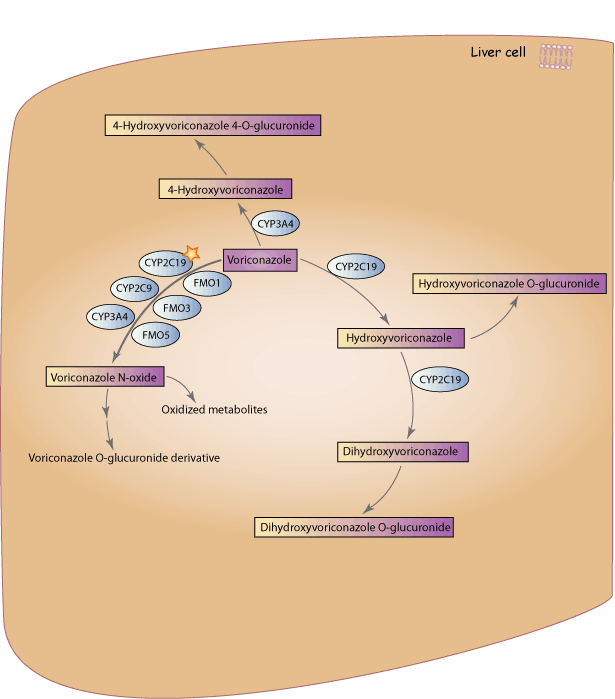
描述
引言
Voriconazole是一種三唑類抗真菌劑,對多種真菌和霉菌具有活性,如Candida、Aspergillus、Fusarium、Scedosporium和Cryptococcus。它特別推薦用於肺部侵襲性曲霉病,這種感染主要發生在免疫功能低下的患者中,例如接受器官移植或有自體免疫疾病的患者[Articles:22141384、21881144]。Voriconazole和其他三唑類抗真菌劑的作用機制是通過干擾真菌細胞膜中一種名為麥角固醇的化合物的合成。麥角固醇合成的干擾導致真菌細胞膜受損,最終導致真菌細胞死亡或抑制真菌細胞生長[Article:18447660]。雖然Voriconazole通常耐受性良好且有效,但其治療範圍較窄。藥物濃度過低會降低療效,而濃度過高則可能影響耐受性和安全性[Articles:22141384、18171251]。與Voriconazole使用相關的嚴重不良事件包括肝毒性和中樞神經系統影響;視覺障礙也很常見,尤其是在藥物濃度較高時[Article:24510446]。Voriconazole的代謝和清除,以及因此在體內的藥物濃度,受到CYP2C19基因型的影響。影響Voriconazole濃度的非遺傳因素包括患者年齡、性別、肝病和同時使用的藥物[Article:23442261。仿單對於Voriconazole的藥物已獲得美國食品藥品監督管理局(FDA)和加拿大衛生部]的批准,指出那些是CYP2C19 弱代謝型(Poor metabolizer)的個體,其藥物暴露平均比正常(廣泛)代謝者高出4倍。然而,支持CYP2C19與毒性或療效之間直接關聯的證據有限。本綜述將提供有關藥物動力學和藥物基因體學的Voriconazole文獻概述,特別強調藥物基因體學,因為該領域的發展可能提供優化劑量的方法。
]藥物動力學
上述圖中提供了Voriconazole在體內的分佈的示意圖。Voriconazole被廣泛代謝,原始劑量中未變化的形式排泄少於2%[Article:16802848]。主要的循環代謝物是voriconazole n-oxide,該代謝物沒有抗真菌活性[Articles:16802848、12695341]。CYP2C19是將Voriconazole代謝為voriconazole n-oxide的主要酶,雖然CYP3A4、CYP2C9和含黃素的單氧化酶(FMO)家族的成員也有貢獻[Articles:16802848、12695341、18362161、17433262];估計約75%的Voriconazole代謝是通過CYP酶介導的,而FMO家族介導剩餘的25%[Article:18362161]。voriconazole n-oxide也可以進一步代謝為各種較少見的代謝物[Article:12756205]。Voriconazole具有作為CYP2C19、CYP3A4和CYP2C9酶的底物和抑制劑的潛力[Article:16802848]。
Voriconazole有兩條主要的代謝途徑:一是甲基基團的羥基化,另一是氟嘧啶環的羥基化[Articles:12756205、18362161]。下圖顯示了這兩種羥基化代謝物的化學結構,以及voriconazole n-oxide的結構。氟嘧啶環的羥基化被認為是通過CYP2C19的作用發生的,而甲基基團的羥基化則被認為是通過CYP3A4的作用發生的[Articles:18362161、17433262、20002085]。羥基化後,這兩種代謝物形成葡萄糖醛酸化代謝物。此外,hydroxyvoriconazole代謝物可以通過CYP2C19再次羥基化形成二羥基-Voriconazole;這種二羥基代謝物隨後可以進行葡萄糖醛酸化[Articles:12756205、20002085]。Bourcier等人發現UGT1A4是參與Voriconazole葡萄糖醛酸化的主要酶,但對於其在Voriconazole代謝物的葡萄糖醛酸化中的作用沒有可用的信息[Article:20304965]。
![]()
圖1. 主要Voriconazole代謝物的化學結構。Voriconazole代謝的三條主要途徑是氟嘧啶環的羥基化、甲基基團的羥基化和N-氧化[Article:12756205]。在“氟嘧啶環的羥基化”代謝物中,與OH基團相關的符號表示OH基團的附著位置是可變的——OH與環相連,但在環的某個未指定或未知的原子上。
藥物基因體學
對Voriconazole的藥物基因體學研究已在健康成人和免疫功能低下的患者中進行。對健康成人的研究測量了不同CYP2C19基因型之間的各種藥代動力學參數的差異,如清除率、血漿濃度-時間曲線下面積(AUC)、中位停留時間(MRT)、最大血漿濃度(Cmax)、血清谷濃度(Ctrough)和消除半衰期(T1/2)[Articles:16890574、20002085、18982321]。為了本綜述的目的,我們將偶爾將這些參數歸類在一起,並稱之為影響CYP2C19基因型的“代謝”。在免疫功能低下的患者中的研究則專注於Voriconazole的谷值或劑量調整的血清谷濃度(Ctrough)[Articles:25084200、26775563、24403552]。Voriconazole 藥物基因體學研究的一個主要限制是小樣本量——在對弱代謝型(Poor metabolizer)(PMs)、中間代謝型(Intermediate metabolizer)(IMs)和超快速代謝型(Ultrarapid metabolizer)(UMs)的研究中,約一半的研究樣本少於30人,大多數少於50人,只有兩項研究的樣本超過100人[Articles:25239277、26982740]。一項綜合分析檢查了CYP2C19變異與Voriconazole 血清谷濃度(Ctrough)和臨床結果之間的關聯:Li等人發現PMs的血清谷濃度(Ctrough)較NMs(NMs)和IMs在6項研究中均有所增加,IMs的血清谷濃度(Ctrough)較NMs在7項研究中有所增加。他們還發現PMs的治療成功率較NMs(在4項研究中)有所增加;然而,PMs、IMs、NMs和UMs之間並未觀察到與不良反應的顯著關聯[Article:27388292]。有關其他參與Voriconazole代謝或濃度的基因變異(如CYP3A4和CYP2C9)的文獻證據非常有限。一項最近的研究發現,根據CYP2C19基因型進行劑量調整的Voriconazole可更快達到目標濃度,這表明預防性CYP2C19基因分型在臨床上可能是有用的[Article:26616742]。
CYP2C19
由於CYP2C19是Voriconazole代謝的主要酶,幾乎所有關於該藥物的藥物基因體學研究都集中在CYP2C19基因型或由此產生的代謝表現型上。CYP2C19基因具有高度多態性,已知有超過30種變異等位基因(http://www.CYP等位基因.ki.se/CYP2C19.htm)。然而,大多數個體將攜帶*1、*2、*3或*17 等位基因。CYP2C19*1 等位基因與正常功能的CYP2C19酶相關,而CYP2C19*2(rs4244285;19154G>A)和*3(rs4986893;17948G>A)是與酶功能缺失最常見的等位基因[Article:22027650]。*2在不同人群中的頻率變化,CAUCasians約15%、非裔美國人約18%和亞洲人約29-34%。*3的頻率則較低,CAUCasians約0.6%、非裔美國人約0.3%和亞洲人約2-9%。其他等位基因也與顯著降低或功能缺失相關(例如 *4-*10),但它們非常罕見,通常在各族群中的頻率低於1%[Articles:25974703、22027650]。此外,對於它們在Voriconazole方面的功能狀態尚未進行研究。CYP2C19*17 等位基因(rs12248560;-806C>T)導致酶活性增加,CAUCasians約22%、非裔美國人約19%、東亞人約2%和南亞或中亞人約17%[Article:22027650。有關CYP2C19 等位基因的更多信息,包括它們的功能性和人群頻率,請參考基因特定信息表頁面CYP2C19]。
根據這些等位基因的存在,個體可以被分類為CYP2C19 超快速代謝型(Ultrarapid metabolizer)(UM)、正常代謝型(Normal metabolizer)(NM)、中間代謝型(Intermediate metabolizer)(IM;也稱為異型合子(Heterozygous) 廣泛代謝型(Extensive metabolizer) (HEM))或弱代謝型(Poor metabolizer)(PM)。NMs的同型合子(Homozygous)為CYP2C19*1 等位基因,並且擁有正常功能的酶。IMs攜帶一個*1 等位基因和一個功能缺失等位基因(例如*1/*2),這會產生一種功能降低的酶。PMs攜帶兩個功能缺失等位基因(例如*2/*2),導致低或缺乏 CYP2C19酶活性。UMs攜帶*17 等位基因,而沒有功能缺失等位基因(即 *1/*17或*17/*17),導致CYP2C19酶活性增加[Article:22027650]。雖然大多數研究將*1/*17歸類為超快速代謝型(Ultrarapid metabolizer) [Articles:26239729,25239277],但有時也將其歸入正常代謝型(Normal metabolizer) 表現型 [Article:24475354]。攜帶功能缺失等位基因和功能增強的等位基因(例如e.g. *2/*17)的個體通常被歸類為IMs [Articles:25974703、23698643]。
弱代謝型(Poor metabolizer)
在17項研究和一項綜合分析中,弱代謝型(Poor metabolizer)被一致發現具有降低的代謝,導致Voriconazole濃度增加,相較於NMs[Articles:15179414、16890574、19033450、18982321、19299322、20002085、20669013、21383338、25999694、21615537、23400848、24403552];一項研究和一項綜合分析發現PMs的代謝較IMs降低[Articles:20669013、27388292]。然而,對於PM基因型對臨床結果的影響,幾乎沒有證據。一項病例報告提到一名*2/*2基因型的患者因藥物濃度過高而停止使用Voriconazole[Article:21615537]。另一項病例報告提到一名*2/*2基因型的個體,由於藥物在毒性水平時出現QTc延長而停止使用該藥物。然而,該研究指出QTc延長可能是由於其他原因引起的,例如電解質異常[Article:23400848]。一項針對兒科患者的大型研究報告了一名PM患者,其Voriconazole濃度過高,發展為不適當抗利尿激素分泌綜合徵(SIADH),並停止使用該藥物[Article:23588332]。幾項研究發現PMs與其他代謝者之間的藥物毒性(例如肝毒性、胃腸道影響、光敏感性)發生率沒有統計學上的顯著差異表現型 [Articles:24475354、19261446、17827141],包括上述討論的綜合分析[Article:27388292]。
中間代謝型(Intermediate metabolizer)
九項研究報告了中間代謝型(Intermediate metabolizer)與Voriconazole的代謝和濃度之間的關聯[Articles:20002085、21383338、23588332、25084200、21038076、26775563],儘管幾項並未進行統計分析[Articles:25999694、25558073、25155930]。然而,幾乎每項研究都發現IMs的Voriconazole代謝降低,濃度增加,相較於NMs。兩個例外是Shi等人的一項研究,發現IMs與NMs之間的AUC、半衰期或清除率沒有顯著差異[Article:20669013],以及Wang等人的一項研究,發現IMs與NMs之間的血清谷濃度(Ctrough)沒有顯著差異,儘管他們確實發現IMs的Voriconazole 血清谷濃度(Ctrough)與voriconazole n-oxide濃度的比率顯著增加[Article:25239277];這些研究中並未提供對矛盾結果的解釋。與PMs一樣,對於IM基因型對臨床結果的影響幾乎沒有證據。一項病例報告提到一名*1/*2基因型的個體,由於血清谷濃度(Ctrough)過高而需要減少劑量[Article:25155930],另一項病例報告提到一名*1/*2基因型的個體,其濃度升高伴隨著幻覺和異常的肝功能檢查。後者患者的不良反應在停止Voriconazole治療後消失,並且在以較低劑量重新引入時未出現問題[Article:21507170]。一項針對兒科患者的研究報告了一名IM患者,其肝功能異常需要減少劑量[Article:23588332]。如前所述,在弱代謝型(Poor metabolizer)部分中,沒有其他研究報告CYP2C19基因變異與Voriconazole相關不良事件之間的統計顯著關聯。迄今為止,大多數報告都是單一患者或病例報告。
超快速代謝型(Ultrarapid metabolizer)
十項研究探討了UM基因型對Voriconazole的代謝和血漿濃度的影響[Articles:18982321、25239277、25084200、26775563、25558073、26239729、23215888、25986028、25120580、22122271],其中五項專注於*1/*17基因型[Articles:18982321]。一項研究發現,擁有*1/*17基因型的個體,其清除率與NMs相比顯著增加[Article:18982321]。另外兩項研究也發現,擁有*1/*17基因型的個體,其Voriconazole濃度較NMs或PMs降低,但均未進行統計分析[Articles:25239277、26239719]。此外,兩項病例報告提到擁有*1/*17基因型的個體,其藥物濃度低於治療範圍或不可檢測[Articles:23215888、25120580]。然而,在這些報告中,一名慢性肉芽腫病患者的結果複雜。該患者在初次評估時的Voriconazole濃度異常高,但隨後的Voriconazole濃度低到不可檢測;作者建議這可能是由於炎症導致的CYP450酶下調[Article:23215888]。與這些報告相反,Hicks等人在兒科患者中的一項研究發現,Voriconazole劑量調整的血清谷濃度(Ctrough)在擁有*1/*17基因型的患者與擁有*1/*1基因型的患者之間沒有統計學上的顯著差異[Article:25084200]。
有關*17/*17基因型對Voriconazole濃度的影響的文獻證據稀少。然而,Hicks等人在兒科研究中發現,擁有*17/*17基因型的患者,其血清谷濃度(Ctrough)的劑量調整Voriconazole顯著低於擁有*1/*1基因型的患者(該研究中有四名擁有此基因型的患者)[Article:25084200]。兩項病例報告支持這一關聯,一項描述了一名藥物濃度不可檢測的個體,促使停止Voriconazole並轉用其他藥物[Article:22122271],另一項描述了一名急性白血病患者,未能達到治療濃度,促使停止使用並轉用卡泊芬淨[Article:26138512]。然而,在前一病例研究中,作者指出該患者同時使用了已知的CYP2C19誘導劑卡馬西平,因此基因型和同時用藥的個別貢獻無法區分[Article:22122271]。在後一研究中,作者表示同時用藥和疾病引起的CYP2C19和CYP3A4的調節不能排除,作為低Voriconazole濃度的解釋[Article:26138512]。
此外,一項針對肺移植患者的研究發現,擁有*1/*17或*17/*17基因型的患者在接受Voriconazole時,發生鱗狀細胞癌(SCC)的風險顯著增加[Article:26982740]。SCC可能導致多種皮膚病變,可能需要手術,並且在某些情況下可能致命;Voriconazole的使用與肺移植受者的疾病風險增加73%相關[Article:26372838]。有關CYP2C19 UMs和SCC的研究作者建議,SCC的增加風險可能與voriconazole n-oxide代謝物和DNA損傷之間的聯繫有關[Article:26982740]。
基因型導向的Voriconazole
Lamoureux等人試圖確定CYP2C19基因型對於在35名患者中達到治療Voriconazole血漿濃度所需劑量的影響。他們發現NMs與IMs或PMs之間的劑量需求沒有差異。然而,UMs的劑量需求顯著高於NMs,並且與IMs或PMs相比,劑量需求約高出1.5倍(UMs:4.76±0.47 mg/kg每日兩次 vs. IMs/PMs:3.03±0.36 mg/kg每日兩次)[Article:26775563]。Teusink等人最近的一項研究比較了Voriconazole的標準劑量與基因型導向劑量[Article:26616742]。一項先導研究跟蹤了25名接受HEM造血幹細胞移植的個體,這些患者接受了5 mg/kg每日兩次的初始劑量,無論基因型如何。然後根據他們的劑量進行調整,直到達到1 - 5.5 ug/L的目標治療範圍。隨後的研究在給予Voriconazole之前對20名個體進行了CYP2C19 *2、*3和*17的基因分型,並根據他們的基因型調整初始Voriconazole劑量如下:IMs或未知代謝者每12小時接受6 mg/kg/劑量,NMs或UMs每12小時接受7 mg/kg/劑量。基因型導向劑量組中沒有PMs,只有一名UM(*1/*17)。然後,劑量如先導研究中所述進行調整,直到達到目標範圍。基因型導向劑量組與標準劑量組的比較顯示,基因型導向劑量組的患者達到目標治療範圍的中位時間為6.5天,而標準劑量組的患者則為29天,這是一個統計學上顯著的差異[Article:26616742]。
其他基因
雖然CYP3A4、CYP2C9和FMO家族的成員都對Voriconazole的代謝有貢獻,但在編碼這些酶的基因變異與Voriconazole的濃度或藥代動力學參數之間的關聯證據非常有限。一項研究發現,擁有CYP3A4基因中rs4646437的AG基因型的個體,其Voriconazole濃度顯著高於擁有GG基因型的個體[Article:25515945]。rs4646437SNP的功能角色尚待確定,但在涉及他克莫司、環孢素和非那雄胺的研究中報告了相反的結果——擁有GG基因型的個體被觀察到具有最高的這些藥物濃度,其次是AG基因型,然後是AA基因型[Articles:24465960、25955319]。CYP2C9也在Voriconazole的代謝中發揮作用,但對於一名*2/*2(弱代謝型(Poor metabolizer))基因型的個體的單一病例報告發現,與擁有*1/*1基因型的健康志願者相比,藥代動力學參數相似[Article:16940139]。迄今為止,尚無研究調查FMO家族變異對Voriconazole代謝或反應的影響。
結論
雖然有相當多的文獻證據支持CYP2C19基因型與Voriconazole暴露之間的關聯,但這些支持性研究大多數樣本量不足。可能需要更大規模的研究來確定基因與藥物之間的更明確聯繫。然而,這類大型研究的可行性可能受到尋找足夠的PMs、IMs或UMs患者的困難影響;國際合作可能有助於招募具有多樣化CYP2C19 表現型的患者。此外,將CYP2C19多態性與Voriconazole臨床結果和不良事件的聯繫結果並不一致。因此,需要更多研究來解決這一潛在關聯。雖然一項研究確實前瞻性地對CYP2C19進行了基因分型,並顯示更快達到目標Voriconazole濃度,但由於該研究的樣本量小、缺乏PMs,且在基因型導向劑量組中僅有一名UM參與者,這一結論受到限制[Article:26616742]。目前文獻中的這些問題需要進一步研究,因為在免疫功能低下患者中,抗真菌治療失敗的高發病率和死亡率令人擔憂。最近由藥物基因體學臨床應用聯盟(CPIC)發布的指南[Article:27981572]提供了基於CYP2C19基因型的治療建議,可能有助於臨床醫生提供更準確的劑量,從而可能防止治療優化的延遲或不必要的不良事件。