CPIC 指南註解:atomoxetine 與 CYP2D6 基因
摘要
CPIC 對於 atomoxetine 的劑量指引提供了 治療建議,適用於 CYP2D6 超快速代謝型、正常代謝型、中間代謝型和 弱代謝型(Poor metabolizer),其中包括血漿藥物濃度測試的指導,作為在治療2週後無臨床反應且無不良事件時估算 atomoxetine 暴露量的方法。該指引自原始發表後已更新。請參閱指引註釋以獲取更多信息。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC® 指南,針對 atomoxetine 和 CYP2D6。
2019年10月更新
CYP2D6 基因型到表現型翻譯變更:截至2019年8月,CYP2D6 基因型到表現型翻譯在指南(如CPIC和DPWG)和臨床基因檢測實驗室之間存在一些不一致。CPIC最近進行了一項修改的德爾菲項目,以獲得國際CYP2D6專家小組對統一系統的共識,用於翻譯CYP2D6基因型到表現型 更多信息。對CPIC先前系統的修改包括將CYP2D6*10 等位基因的活性分數計算值從0.5降至0.25,並將活性分數為1的表現型分配從正常代謝型(Normal metabolizer)更改為中間代謝型(Intermediate metabolizer)(所有先前和新表現型分組的表格)。
因此,CYP2D6 等位基因功能表、CYP2D6基因型到表現型表、Atomoxetine測試前後警報和流程圖中已進行以下更改(請參閱下表):
- 活性分數為1的從CYP2D6 正常代謝型(Normal metabolizer)更改為CYP2D6 中間代謝型(Intermediate metabolizer)。
- 對本指南建議的影響:當前指南對AS為1(無CYP2D6*10 等位基因存在)有具體建議;因此,當前已發表的正常和中間代謝型(Intermediate metabolizer)建議將保持不變。
- 所有包含CYP2D6*10 等位基因的雙倍型的活性分數已相應更新(活性分數更改以反映CYP2D6*10的較低活性值0.25)。請參閱所有先前和新表現型分組的表格。
- 對本指南建議的影響:對於超快速和正常代謝型(Normal metabolizer)的建議相同,因此此更改不影響推薦的處方建議。對於活性分數為1(存在CYP2D6*10 等位基因)和0.5的建議相同,因此當前已發表的此雙倍型建議將保持不變。
2018年2月
2019年2月在線提前發表
- 關於在atomoxetine劑量中使用藥物基因組學測試的CPIC指南已發表在《Clinical Pharmacology and Therapeutics》期刊由藥物基因體學臨床應用聯盟(CPIC)。
- 這些指南適用於:
- 兒科患者
- 成人患者
- 2019年劑量指南摘錄:
- 「CYP2D6基因變異對atomoxetine 藥物動力學有深遠影響。.... CYP2D6 PMs的atomoxetine暴露(AUC)平均比非PMs高10倍。.... 與至少有一個功能正常 等位基因的個體相比,具有兩個CYP2D6*10 等位基因的個體具有更高的atomoxetine暴露(高5倍最高血中濃度(Cmax))。」
- 「atomoxetine最廣泛研究的藥代動力學參數是將近似於母化合物Cmax的血漿藥物濃度與ADHD症狀的減少相關聯。鑑於此證據,每個CYP2D6 表現型類別的治療建議還包括血漿藥物濃度測試的指導,作為估計atomoxetine暴露(即暴露檢查)的一種方法。這些目標參考值來自神經精神藥理學治療藥物監測(TDM)共識指南[文章:29493375],旨在指導臨床醫生在患者對atomoxetine反應不足的情況下。」
- 「來自體外和體內研究的數據(補充表1),以及共識建議被用於制定指導。」
- 下載並閱讀:
表1:根據CYP2D6基因型/表現型為兒童推薦的atomoxetine劑量
改編自2019年指南手稿的表1和表2
| 表現型a | 活性分數 | 基因型 | 基因型示例b | 影響 | 治療建議 | 建議等級c |
|---|---|---|---|---|---|---|
| CYP2D6 超快速代謝型(Ultrarapid metabolizer) | >2 | 攜帶功能性等位基因重複的個體 | *1/*1xN, *1/*2xN, *2/*2xNd | 基於CYP2D6 超快速代謝型(Ultrarapid metabolizer)服用atomoxetine的非常有限的數據,標準劑量下不太可能超快速代謝型(Ultrarapid metabolizer)達到預期效果的足夠血清濃度 | 以0.5 mg/kg/天的劑量開始,3天後增加至1.2 mg/kg/天。如果2週後無臨床反應且無不良事件,考慮獲得峰值血漿濃度(給藥後1至2小時)。如果<200 ng/ml,考慮按比例增加劑量以接近400 ng/mle,f | 中等建議 |
| CYP2D6 正常代謝型(Normal metabolizer) | 1.5和2 | 攜帶兩個功能正常 等位基因或一個功能正常和一個功能減弱 等位基因的個體 | *1/*1, *1/*2, *1/*9, *1/*41, *2/*2 | atomoxetine的正常代謝型(Normal metabolizer)反應可能性較低,與弱代謝型(Poor metabolizer)相比。這與因缺乏療效而增加的停藥率相關,與弱代謝型(Poor metabolizer)相比 | 以0.5 mg/kg的劑量開始,3天後增加至1.2 mg/kg/天。如果2週後無臨床反應且無不良事件,考慮獲得峰值血漿濃度(給藥後1至2小時)。如果<200 ng/ml,考慮按比例增加劑量以接近400 ng/mle,f | 中等建議 |
| CYP2D6 正常代謝型(Normal metabolizer)或中間代謝型(Intermediate metabolizer)(仍有爭議)g | 1(無*10 等位基因存在)h | 攜帶兩個功能減弱 等位基因或一個功能正常和一個功能缺失 等位基因的個體。活性分數(AS)為1.0與AS為1.5或2的個體相比,與atomoxetine代謝減少相關 | *1/*4, *1/*5, *41/*41 | 可能比正常代謝型(Normal metabolizer)具有更高的atomoxetine濃度,但臨床意義可疑。正常代謝型(Normal metabolizer)可能比弱代謝型(Poor metabolizer)有更高的停藥風險 | 以0.5 mg/kg的劑量開始,3天後增加至1.2 mg/kg/天。如果2週後無臨床反應且無不良事件,考慮獲得峰值血漿濃度(給藥後1至2小時)。如果<200 ng/ml,考慮按比例增加劑量以接近400 ng/mle,f | 中等建議 |
| CYP2D6 正常代謝型(Normal metabolizer)或中間代謝型(Intermediate metabolizer)(仍有爭議)g | 1(*10 等位基因存在)h | 攜帶兩個功能減弱 等位基因或一個功能正常和一個功能缺失 等位基因的個體。活性分數(AS)為1.0與AS為1.5或2的個體相比,與atomoxetine代謝減少相關 | *10/*10, *10/*41 | 與正常代謝型(Normal metabolizer)相比,atomoxetine代謝減少且atomoxetine濃度較高。具有CYP2D6*10的活性分數為1.0的個體可能比弱代謝型(Poor metabolizer)有更高的停藥風險 | 以0.5 mg/kg/天的劑量開始,如果2週後無臨床反應且無不良事件,考慮在給藥後2-4小時獲得血漿濃度。如果反應不足且濃度<200 ng/ml,考慮按比例增加劑量以達到接近400 ng/ml的濃度e,f如果在任何時候出現不可接受的副作用,考慮減少劑量 | 中等建議 |
| CYP2D6 中間代謝型(Intermediate metabolizer) | 0.5 | 攜帶一個功能減弱和一個功能缺失 等位基因的個體 | *4/*10,*4/*41, *5/*9 | 與正常代謝型(Normal metabolizer)相比,atomoxetine代謝減少且atomoxetine濃度較高。中間代謝型(Intermediate metabolizer)可能比弱代謝型(Poor metabolizer)有更高的停藥風險 | 以0.5 mg/kg/天的劑量開始,如果2週後無臨床反應且無不良事件,考慮在給藥後2-4小時獲得血漿濃度。如果反應不足且濃度<200 ng/ml,考慮按比例增加劑量以達到接近400 ng/ml的濃度e,f如果在任何時候出現不可接受的副作用,考慮減少劑量 | 中等建議 |
| CYP2D6 弱代謝型(Poor metabolizer) | 0 | 僅攜帶功能缺失al 等位基因的個體 | *3/*4,*4/*4, *5/*5, *5/*6 | atomoxetine代謝顯著減少可能導致濃度較高,與非弱代謝型(Poor metabolizer)相比。這可能增加治療出現的副作用,但在能夠耐受治療的患者中,與非弱代謝型(Poor metabolizer)相比,ADHD症狀的改善更大。弱代謝型(Poor metabolizer)狀態與較低的最終劑量需求相關,與非弱代謝型(Poor metabolizer)相比 | 以0.5 mg/kg/天的劑量開始,如果2週後無臨床反應且無不良事件,考慮在給藥後4小時獲得血漿濃度。如果反應不足且濃度<200 ng/ml,考慮按比例增加劑量以達到接近400 ng/ml的濃度e,f如果在任何時候出現不可接受的副作用,考慮減少劑量 | 強烈建議 |
a請參閱CYP2D6頻率表以獲取種族特定的等位基因和表現型頻率CYP2D6表。
b 等位基因功能的分配和等位基因功能的引用可以在CYP2D6 等位基因定義表和CYP2D6 等位基因功能表中找到。要獲取CYP2D6 雙倍型和結果表現型的完整列表,請參閱CYP2D6基因型到表現型表CYP2D6表。請注意,活性分數為1的基因型在在線CYP2D6基因型到表現型表中被分類為NMs
。
c補充中描述的評分方案
。
d其中xN代表CYP2D6基因拷貝數。對於具有CYP2D6重複或多重的個體,請參閱補充數據以獲取有關如何將雙倍型轉換為表現型的其他信息
。
e已提出200至1000 ng/ml的治療範圍[文章:29493375]。
f有關atomoxetine血漿濃度與臨床反應之間關係的數據有限。可用信息表明,PMs的臨床反應比非PMs更大,這可能與PMs在給藥後1至1.5小時的血漿濃度較高有關,與非PMs給予相似劑量相比。此外,在最高血中濃度(Cmax)大於400 ng/ml時,觀察到ADHD-RS的減少定義的反應適度改善
。
g某些參考實驗室可能將活性分數為1.0的患者分類為中間代謝型(Intermediate metabolizer)。一組CYP2D6專家目前正在努力標準化CYP2D6基因型到表現型翻譯系統。CPIC將相應更新CPIC網站
。
h CPIC通常將活性分數為1的患者分類為“正常代謝型(Normal metabolizer)”。然而,在atomoxetine的情況下,對於AS為1.0的患者的處方建議是基於CYP2D6*10 等位基因的存在而等位基因依賴的
表2:根據CYP2D6基因型/表現型為成人推薦的atomoxetine劑量
改編自2019年指南手稿的表1和表3
| 表現型a | 活性分數 | 基因型 | 基因型示例b | 影響 | 治療建議 | 建議等級c |
|---|---|---|---|---|---|---|
| CYP2D6 超快速代謝型(Ultrarapid metabolizer) | >2 | 攜帶功能性等位基因重複的個體 | *1/*1xN, *1/*2xN, *2/*2xNd | 基於CYP2D6 超快速代謝型(Ultrarapid metabolizer)服用atomoxetine的非常有限的數據,標準劑量下不太可能超快速代謝型(Ultrarapid metabolizer)達到預期效果的足夠血清濃度 | 以40 mg/天的劑量開始,3天後增加至80 mg/天。如果2週後無臨床反應且無不良事件,考慮增加劑量至100 mg/天。如果2週後無臨床反應,考慮獲得峰值血漿濃度(給藥後1至2小時)。如果<200 ng/ml,考慮按比例增加劑量以接近400 ng/mle,f可能需要超過100 mg/天的劑量以達到目標濃度g | 中等建議 |
| CYP2D6 正常代謝型(Normal metabolizer) | 1.5和2 | 攜帶兩個功能正常 等位基因或一個功能正常和一個功能減弱 等位基因的個體 | *1/*1, *1/*2, *1/*9, *1/*41, *2/*2 | atomoxetine的正常代謝型(Normal metabolizer)反應可能性較低,與弱代謝型(Poor metabolizer)相比。這與因缺乏療效而增加的停藥率相關,與弱代謝型(Poor metabolizer)相比 | 以40 mg/天的劑量開始,3天後增加至80 mg/天。如果2週後無臨床反應且無不良事件,考慮增加劑量至100 mg/天。如果2週後無臨床反應,考慮獲得峰值血漿濃度(給藥後1至2小時)。如果<200 ng/ml,考慮按比例增加劑量以接近400 ng/mle,f可能需要超過100 mg/天的劑量以達到目標濃度g | 中等建議 |
| CYP2D6 正常代謝型(Normal metabolizer)或中間代謝型(Intermediate metabolizer)(仍有爭議)h | 1(無*10 等位基因存在)i | 攜帶兩個功能減弱 等位基因或一個功能正常和一個功能缺失 等位基因的個體。活性分數(AS)為1.0與AS為1.5或2的個體相比,與atomoxetine代謝減少相關 | *1/*4, *1/*5, *41/*41 | 可能比正常代謝型(Normal metabolizer)具有更高的atomoxetine濃度,但臨床意義可疑。正常代謝型(Normal metabolizer)可能比弱代謝型(Poor metabolizer)有更高的停藥風險 | 以40 mg/天的劑量開始,3天後增加至80 mg/天。如果2週後無臨床反應且無不良事件,考慮增加劑量至100 mg/天。如果2週後無臨床反應,考慮獲得峰值血漿濃度(給藥後1至2小時)。如果<200 ng/ml,考慮按比例增加劑量以接近400 ng/mle,f可能需要超過100 mg/天的劑量以達到目標濃度g | 中等建議 |
| CYP2D6 正常代謝型(Normal metabolizer)或中間代謝型(Intermediate metabolizer)(仍有爭議)h | 1(*10 等位基因存在)i | 攜帶兩個功能減弱 等位基因或一個功能正常和一個功能缺失 等位基因的個體。活性分數(AS)為1.0與AS為1.5或2的個體相比,與atomoxetine代謝減少相關 | *10/*10, *10/*41 | 與正常代謝型(Normal metabolizer)相比,atomoxetine代謝減少且atomoxetine濃度較高。具有CYP2D6*10的活性分數為1.0的個體可能比弱代謝型(Poor metabolizer)有更高的停藥風險 | 以40 mg/天的劑量開始,如果2週後無臨床反應且無不良事件,增加劑量至80 mg/天。如果2週後反應不足,考慮在給藥後2-4小時獲得血漿濃度。如果濃度<200 ng/ml,考慮按比例增加劑量以達到接近400 ng/ml的濃度e,f如果在任何時候出現不可接受的副作用,考慮減少劑量 | 中等建議 |
| CYP2D6 中間代謝型(Intermediate metabolizer) | 0.5 | 攜帶一個功能減弱和一個功能缺失 等位基因的個體 | *4/*10,*4/*41, *5/*9 | 與正常代謝型(Normal metabolizer)相比,atomoxetine代謝減少且atomoxetine濃度較高。中間代謝型(Intermediate metabolizer)可能比弱代謝型(Poor metabolizer)有更高的停藥風險 | 以40 mg/天的劑量開始,如果2週後無臨床反應且無不良事件,增加劑量至80 mg/天。如果2週後反應不足,考慮在給藥後2-4小時獲得血漿濃度。如果濃度<200 ng/ml,考慮按比例增加劑量以達到接近400 ng/ml的濃度e,f如果在任何時候出現不可接受的副作用,考慮減少劑量 | 中等建議 |
| CYP2D6 弱代謝型(Poor metabolizer) | 0 | 僅攜帶功能缺失al 等位基因的個體 | *3/*4,*4/*4, *5/*5, *5/*6 | atomoxetine代謝顯著減少可能導致濃度較高,與非弱代謝型(Poor metabolizer)相比。這可能增加治療出現的副作用,但在能夠耐受治療的患者中,與非弱代謝型(Poor metabolizer)相比,ADHD症狀的改善更大。弱代謝型(Poor metabolizer)狀態與較低的最終劑量需求相關,與非弱代謝型(Poor metabolizer)相比 | 以40 mg/天的劑量開始,如果2週後無臨床反應且無不良事件,增加劑量至80 mg/天。如果2週後反應不足,考慮在給藥後2-4小時獲得血漿濃度。如果濃度<200 ng/ml,考慮按比例增加劑量以達到接近400 ng/ml的濃度e,f如果在任何時候出現不可接受的副作用,考慮減少劑量 | 中等建議 |
a請參閱CYP2D6頻率表以獲取種族特定的等位基因和表現型頻率CYP2D6表。
b 等位基因功能的分配和等位基因功能的引用可以在CYP2D6 等位基因定義表和CYP2D6 等位基因功能表中找到。要獲取CYP2D6 雙倍型和結果表現型的完整列表,請參閱CYP2D6基因型到表現型表CYP2D6表。請注意,活性分數為1的基因型在在線CYP2D6基因型到表現型表中被分類為NMs
。
c補充中描述的評分方案
。
d其中xN代表CYP2D6基因拷貝數。對於具有CYP2D6重複或多重的個體,請參閱補充數據以獲取有關如何將雙倍型轉換為表現型的其他信息
。
e已提出200至1000 ng/ml的治療範圍[文章:29493375]。
f有關atomoxetine血漿濃度與臨床反應之間關係的數據有限。可用信息表明,PMs的臨床反應比非PMs更大,這可能與PMs在給藥後1至1.5小時的血漿濃度較高有關,與非PMs給予相似劑量相比。此外,在最高血中濃度(Cmax)大於400 ng/ml時,觀察到ADHD-RS的減少定義的反應適度改善
。
g劑量超過120 mg/天尚未評估
。
h某些參考實驗室可能將活性分數為1.0的患者分類為中間代謝型(Intermediate metabolizer)。一組CYP2D6專家目前正在努力標準化CYP2D6基因型到表現型翻譯系統。CPIC將相應更新CPIC網站
。
i CPIC通常將活性分數為1的患者分類為“正常代謝型(Normal metabolizer)”。然而,在atomoxetine的情況下,對於AS為1.0的患者的處方建議是基於CYP2D6*10 等位基因的存在而等位基因依賴的
atomoxetine 途徑, 藥物動力學
概括
參與 atomoxetine 代謝之候選基因示意圖
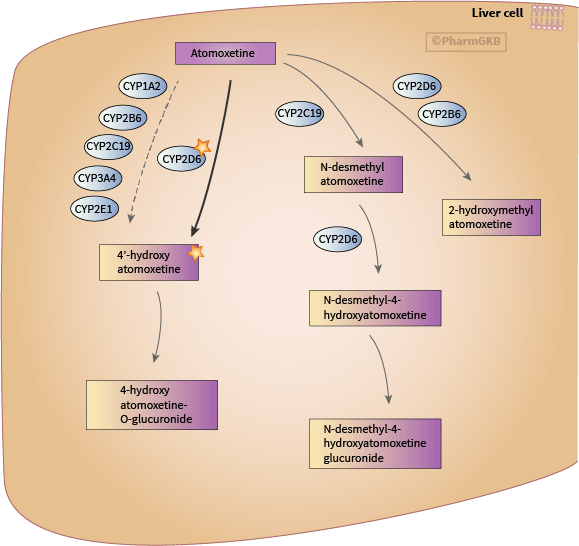
描述
atomoxetine (ATX) 是一種去甲腎上腺素再攝取抑制劑,用於治療注意力不足過動症 (ADHD)。ATX 透過抑制突觸前神經元中的去甲腎上腺素運輸蛋白 (SLC6A2) 來影響去甲腎上腺素 途徑,然而其完整的作用機制尚未完全了解 [Articles:8233054, 25637266]。與三環類藥物相比,其對其他神經元運輸蛋白和神經傳遞物質受體的親和力相對較低 [Article:6123593]。ATX 的血腦屏障運輸似乎主要是被動的 [Article:18936112],而 ATX 不太可能是 ABCB1 的底物 [Article:17963743]。
藥物動力學
藥物動力學 在健康個體中的研究表明,具有多態性變異的酶參與了 ATX 的清除,因為 11 名參與者中有 2 名顯示出延長的半衰期和隨後的 ATX 累積 [Article:4008676]。 4-羥基atomoxetine (4-OH ATX) 是 ATX 的主要且具有藥理活性的代謝物,迅速被葡萄糖醛酸化為無活性的 4-羥基atomoxetine 葡萄糖醛酸酯 (4-OH ATX 葡萄糖醛酸酯) [Article:12485958]。 使用人類肝微粒體的研究顯示,4-OH ATX 的形成與 CYP2D6 活性相關 [Articles:11854152, 27052878]。多種 CYP (CYP1A2, CYP2B6, CYP2C19, CYP3A4, CYP2E1) 在 CYP2D6 的微粒體中顯示能夠形成 4-OH ATX。然而,其效率降低,且代謝物的量少於由 CYP2D6 媒介的量 [Article:11854152]。相反地,篩選幾種異源表達的 CYP 450 酶僅識別 CYP2J2 作為 4-OH ATX 形成的次要酶 (比 CYP2D6 低 100 倍) [Article:27052878]。然而,在同一研究中,對於在池化的人類肝微粒體中 4-OH ATX 形成的抑制劑的識別僅顯示奎寧 (CYP2D6) 以劑量依賴的方式作出貢獻。此外,酮康唑 (CYP3A) 在一名無 CYP2D6 活性的受試者的肝微粒體中抑制了 4-OH ATX 的形成 [Article:27052878]。 ATX 的另一條不太顯著的排除途徑是轉化為無活性的 N-去甲基atomoxetine (N-desmethyl ATX; noratomoxetine),由 CYP2C19 進一步形成 N-desmethyl-4-hydroxyatomoxetine,推測是通過 CYP2D6 [Articles:12485958, 11854152, 26660002]。N-desmethyl ATX 也由 CYP1A1, CYP2B6, CYP2D6, CYP2J2, CYP3A4 生成,且在使用異源表達的細胞色素 P450 的實驗中,CYP2C18 生成的量最大 [Article:27052878]。 此外,2-羥基甲基atomoxetine (2-CH2-OH-ATX) 和 2-羥基甲基atomoxetine 衍生的代謝物以小量被檢測到 [Articles:12485958, 26660002]。對於 ATX 轉化為 2-CH2-OH-ATX,CYP2D6 和 CYP2B6 可能參與 [Article:27052878]。
藥物基因體學
放射性標記的 ATX 從腸胃道良好吸收,且無個體間差異。在完全 CYP2D6 代謝的受試者中,大部分放射性劑量在 24 小時內排出 (ATX t1/2=5h),而在 CYP2D6 缺乏的受試者中,排出時間增加至 72 小時 (ATX t1/2=20h) [Article:12485958]。4-OH ATX 葡萄糖醛酸酯在功能性 CYP2D6 的受試者尿液樣本中約占總放射性活性的 84%,在血漿樣本中占 67%,這些受試者在第 5 天接受了兩次 20mg ATX 的劑量,並在第 6 天接受了一次 14C-ATX 的劑量 [Article:12485958]。在 CYP2D6 弱代謝型(Poor metabolizer) (PM) 受試者中,尿液中的量減少 (31%),但 4-OH ATX 葡萄糖醛酸酯仍然是尿液中主要的 ATX- 衍生代謝物,於給藥後 120-264 小時內。PM 受試者的血漿樣本中,ATX 和 N-desmethyl ATX 的濃度是最豐富的代謝物 [Article:12485958]。由於 CYP2D6 在 N-desmethyl ATX 的清除中起作用,因此在 CYP2D6 PM 中該代謝物的較高量被認為是由於清除速度較慢而導致的累積,而非產生增強。研究發現,與 CYP2D6 正常代謝型(Normal metabolizer) (NM; 前 廣泛代謝型(Extensive metabolizer)) 相比,CYP2D6 PM 受試者的次要 (次要) 轉化途徑中的代謝物增加 (佔 ATX 劑量的 22%) [Article:12485958]。 在 23 名兒童的單次 ATX 劑量研究中,確認 4-OH ATX 是主要的代謝物,主要以葡萄糖醛酸化形式存在,與 CYP2D6 基因型無關。N-去甲基化途徑在 ATX 代謝中僅貢獻微量,但在 PM 受試者中 N-desmethyl ATX 的比例較高,且 PM 中次要途徑的代謝物增加也與成人的研究結果一致 [Article:26660002]。
目前發表的大多數 ATX 藥物基因體學 研究調查了 CYP2D6 變異的影響。表 1 總結了研究,這些研究比較了按兩個 功能缺失 CYP2D6 等位基因 (PM) 與其餘受試者分組的兒童和青少年患者的療效和副作用。確定了 功能缺失 等位基因 *3, *4, *5, *6, *7, *8。同型合子(Homozygous) 和 複合異形合子(Compound heterozygous) 這些 等位基因 的攜帶者被歸類為 PM,而 異型合子(Heterozygous) 和非攜帶者則被分為 NM。PM 的平均峰值血漿濃度是 ATX 的 NM 的 2 到 5 倍 [Articles:12562062, 17242628]。在至少 1.2mg/kg/day 的劑量下,1290 名 NM 與 67 名 PM 或 1239 名 NM 與 87 名 PM 之間的治療中止沒有差異 [Articles:12562062, 17698328]。然而,對幾個綜合研究的不同分析指出,PM 的研究持續率較高 (2563 NM 對 171 PM, p=0.032, Fisher 精確檢驗)。有人認為這是由於基於注意力不足過動症評分量表 (ADHDRS) 的改善更好而驅動的 [Article:17242628],而另一項研究未能顯示兩組之間的反應差異 [Article:17698328]。CYP2D6 PM 的脈搏率略有增加,且體重減輕的情況比 NM 更明顯 [Articles:12562062, 17242628, 17698328]。在 CYP2D6 NM 和 PM 兒童及青少年患者之間未觀察到 QT 間期的差異 [Articles:17242628, 17698328]。
除了上述較大研究外,還有其他 藥物基因體學 研究關於 CYP2D6 變異對 atomoxetine 藥物動力學參數和結果/ADR 的影響,總結於表 2。僅使用 CYP2D6 PM (未報告特定變異),健康成人受試者接受安慰劑、40 和 120mg/day ATX (按體重調整的最大批准劑量) 的劑量顯示,隨著血漿濃度的增加,QTc 之心率校正間期顯著增加 [Article:22803597]。然而,作者得出結論,ATX 與 QTc 的臨床顯著變化無關 [Article:22803597]。在接受 ATX 80-100 mg/day 治療的成人中,與非 PM 相比,報告了更高頻率的口乾、男性勃起功能障礙、多汗、失眠和尿潴留 [Article:25919121]。雖然在兒童的研究中僅調查了 功能缺失 等位基因,但在成人的後續研究中進一步考察了其他代謝者 表現型,並未在 NM/超快速代謝型(Ultrarapid metabolizer) (UM) 和 中間代謝型(Intermediate metabolizer) (IM) 之間建立治療出現不良事件的差異 (見表 2) [Article:25919121]。然而,IM 組涵蓋了廣泛的功能性,將具有一個正常和一個減少或 功能缺失 等位基因、兩個減少功能 等位基因 和一個減少和一個 功能缺失 等位基因 的患者進行分組。
最近一項對 0.5 mg/kg ATX 的單次劑量研究將受試者分為 NMs,具有一個或兩個 功能正常 或兩個 功能減弱 等位基因,IM (攜帶一個減少和一個 功能缺失 等位基因) 和 PM (兩個 功能缺失 等位基因) [Article:26660002]。PM 和 NM 受試者之間的 ATX 和 4-OH ATX 的血漿濃度以及 ATX 的口服清除顯著不同,但 IM 值在某些但不是所有評估的參數中與 PM 沒有顯著差異。劑量校正的 ATX 系統性暴露在 23 名兒童中變化了 29.6 倍,並且依賴於基因型,在 NMs 中為 4.4±2.7 µM*h,對於具有兩個 等位基因 的 NMs 為 5.8±1.7 µM*h,16.3±2.9 µM*h 和 50.2±7.3 µM*h,分別為 IM 和 PM (p<0.0001) [Article:26660002]。 在亞洲人群中的研究顯示,ATX 的藥物動力學參數如 Cmax、AUC 和清除率在 *1/*1、*1/*10 和 *10/*10 攜帶者之間存在差異 (表 2) [Articles:17610534, 21543662, 26254792],但這種變異的臨床意義尚未調查。在兩項小型研究中,未發現 ATX 的耐受性差異 [Articles:17610534, 21543662]。
除了 CYP2D6 的變異外,與 CYP2D6 抑制劑的共同用藥可能會影響 ATX 藥物動力學。帕羅西汀在一項對 22 名健康個體的研究中,將 20mg/day ATX 與額外的 20mg/day 帕羅西汀共同給藥,分別增加了 C(ss,max)、AUC0-12 和 atomoxetine 的 t1/2 約 3.5 倍、6.5 倍和 2.5 倍。在與帕羅西汀共同給藥後,觀察到 N-desmethyl ATX 的增加和 4-OH ATX 濃度的減少 [Article:12412820]。同樣,Kim 等報告了帕羅西汀共同給藥對 ATX 藥物動力學參數的影響 [Article:27673638]。此外,一項案例研究報告了通過提高 ATX 濃度來改善症狀,這是由於帕羅西汀共同給藥 [Article:18215333]。
多個機構的產品 仿單 包含有關 CYP2D6 和 atomoxetine 的信息,並在 ATX 藥物 仿單 頁面上進行總結。
儘管大多數 藥物基因體學 研究存在於 CYP2D6 變異與 ATX 治療的療效和副作用風險的關聯,但已發表的有關 CYP2C19 和 SLC6A2 變異的研究不多。一項對 40 名健康韓國受試者的研究顯示,在單次 40 mg 劑量後,ATX 的藥物動力學參數存在差異。ATX 的血漿濃度 (Cmax 和 AUC) 在 PM (攜帶 *2/ *2、*2/ *3、*3/ *3) 中較高,清除率 (CL/F) 較低,半衰期較長,與 IM (*1/ *2、*1/ *3) 和 NM (*1/ *1) 相比 [Article:24346747]。N-desmethyl ATX 的血漿濃度 (Cmax 和 AUC) 較低。所有患者均為 CYP2D6 *1/*10 [Article:24346747]。
研究 ATX 的目標,Ramoz 等使用了兩個不同的隊列 (N=160 和 N=105) 的兒童 ADHD [Article:19387424]。第一個隊列的患者治療開始劑量為 0.5 mg/kg/day,並可調整至最大劑量 1.8 mg/kg 每天,持續最多 10 週的急性、開放性治療。第二個較小的隊列使用急性、隨機、雙盲治療,劑量為 0.8–1.8 mg/kg 每天,持續 6 週。在最初研究的 108 SNV 中,265 名患者的綜合隊列中有 14 名名義上顯著。然而,這 14 個變異在所有分析中均未顯示與 6 週治療後的反應有關聯,包括隊列 1、隊列 2、綜合隊列和僅 CAUC 亞洲受試者。通過綜合注意力不足過動症評分量表 (ADHDRS) 和臨床全球印象-疾病嚴重程度量表 (CGI-S) 分數測量的反應與 rs3785152 的 T 等位基因 之間的關聯被檢測到 (p<0.01,對於綜合隊列的比值比 (OR) 2.2;p<0.01 OR 3.1 對於隊列 1;p<0.01 OR 2.7 僅對 CAUC 亞洲人;p=0.15 OR 2.1 對於隊列 2) [Article:19387424]。Yang 等發現 rs3785143 T 等位基因 與在一個 111 名中國兒童的隊列中為非反應者的關聯,這些兒童接受了劑量調整至 1.2-1.4 mg/kg 每天並維持 4 週 (p=0.0416,OR 2.66,經多重檢驗修正) [Article:23266789]。在這項研究中,使用注意力不足過動症評分量表版本 4 (ADHDRS-IV) 作為主要療效指標,並定義反應者為分數減少 25%。SLC6A2 rs3785143 的結果無法複製,且未顯示反應者與非反應者之間的差異 [Article:23266789]。
結論
ATX 由高度變異的 CYP2D6 廣泛代謝。這導致在建議劑量下藥物暴露的顯著變異性。
表 1
在兒童和青少年患者 (混合族裔) 中的療效和副作用,按兩個 功能缺失 CYP2D6 等位基因 (弱代謝型(Poor metabolizer); PM; 例如 *4/*5) 與 正常代謝型(Normal metabolizer) (NM; 例如 *1/*4, *1/*1) 分組。這些隊列的基因型為 *3, *4, *5, *6, *7, *8,功能減弱 等位基因 未包含。
| 發表的研究/綜合分析(Meta-analysis) | 原始研究 | 樣本大小 | 劑量 (給藥) | 劑量 (最終) | 反應 (ADHDRS-IV-Parent:Inv 分數) | 中止 | ADR 一般 | 體重和脈搏 | QT 間期 |
|---|---|---|---|---|---|---|---|---|---|
| 12562062 | Allen AJ et al 2001 (無 PMID) | 1290NM; 67 PM | 至少 1.2 mg/kg/day | 無差異 | 無差異 | PM 比 NM 的脈搏率和體重減輕更高 (無統計學意義) | |||
| 17242628 | 11694667; 12411225; 12523874 | 559 NM; 30 PM | 按體重調整的最大每日劑量為 1.8 mg/kg | PM: 平均最終劑量 1.28 (0.36) mg/kg/day NM: 1.37 (0.33) mg/kg/day (p = 0.12) | PM 與 NM 的平均最終 ADHDRS 總分數相比,改善更大 (p=0.002) 和反應者的比率更高 (p=0.033) | ||||
| 17242628 | 未報告 | 2563 NM; 171 PM | 接受劑量 >1.2 mg/kg/day | PM: 平均最終劑量為 1.51 (0.30) mg/kg/day NM: 1.55 (0.29) mg/kg/day | 治療中止 (p=0.032) 歸因於療效不足 (p=0.004) 的情況下,PM 與 NM 的中止率顯著較低,無差異於 ADR | 無差異,除了 PM 與 EM 之間報告的磨損 (p=0.013) 和顫抖 (p<0.001) 的發生率較高 | PM 與 NM 相比,脈搏 (p<0.001) 和舒張壓 (p<0.012) 增加更大,體重增加較少 (p=0.088) | 無差異 | |
| 17698328 | Allen AJ et al 2001 (無 PMID); Wernicke et al 2002 (無 PMID) | 1239 NM; 87 PM | 以 0.5 mg/kg/day 開始,並在試驗期間增加至 1.8 mg/kg/day,目標是達到 CGI-ADHD-S 分數低於 3 | 最終劑量 (在終點) 的平均值為 NM: 1.50 mg/kg/d (SD = 0.36) 和 PM: 1.35 mg/kg/d (SD = 0.43) p=0.004 | PM 的總分數減少無顯著性 (p=0.07),反應者率無差異 (p=0.56) | 無中止的差異 (p=0.33);PM 中由於任何不良事件的中止率較高的趨勢 (NM: 30/1239,或 2.4%;PM: 5/87,或 5.8%,p=0.08) | PM 中的體重差異 (p<0.001),且 PM 的脈搏增加比 NM 更大 (p<0.005) | 無差異 |
ADHDRS-IV-Parent:Inv: 注意力不足過動症評分量表-IV-家長版本: 研究者管理和評分; CGI-S: 臨床全球印象-疾病嚴重程度量表; CGI-ADHD-S: 臨床全球印象-ADHD-嚴重程度; 反應者: 定義為從基線減少 25% 的 ADHDRS-IV-Parent:Inv 總分; NM: 正常 (前廣泛) 代謝者; PM: 弱代謝型(Poor metabolizer)
表 2
基因變異對 CYP2D6 的影響 atomoxetine 代謝和藥物反應。
12485958| 參考 | CYP2D6 表現型 | CYP2D6 Diplotype | 研究大小 | 國家/族裔 | 劑量 | 主要發現 | |||
|---|---|---|---|---|---|---|---|---|---|
| 11694667 | 280 NM, 17PM | NA (PM 等位基因 基因型) | 297 名兒童和青少年 ADHD | USA | 安慰劑; 0.5; 1.2; 1.8 mg/kg/day | 療效使用 ADHD RS 量表分數進行測量。ATX 在 1.2 和 1.8 mg/kg/day 劑量下在所有患者中優於安慰劑。對於 PM 患者,這些劑量的效果幅度較 NM 更大 (p<0.05) | |||
| 11854152 | NA | NA | A) 2 個人類微粒體樣本包含完整的 CYP; B) 2 個人類微粒體樣本 CYP2D6-缺乏 | 體外 | NA | 4-OH ATX 形成的酶動力學分析:A) CLint (Vmax/Km) 為 50 和 155 B) CLint (Vmax/Km) 為 0.1 和 0.3 | |||
| 4 NM; 3 PM | NA (PM 等位基因 基因型) | 7 | USA | 每日兩次 20mg 持續 5 天 | PM 中 4-OH ATX 形成的速率降低,且平均 ATX 清除率較慢 (為 NM 的 25%) | ||||
| 17242628 | 559 NM; 30 PM | NA (*3, *4, *5, *6, *7, *8) 被基因型並且患者被分組 PM 為其中之一或兩個 同型合子(Homozygous) 的組合;所有其他患者分組為 NM) | 589 名兒童和青少年 ADHD | 非洲裔 (14.8%)、亞洲裔 (0.7%)、白人 (69.8%)、西班牙裔 (10.1%)、其他 | NM: 平均劑量 1.37 mg/kg/day; PM: 平均劑量 1.28 mg/kg/day (允許最大每日劑量為 1.8mg/kg) | PM 與 NM 患者相比,改善更大; ADHDRS p=0.002, CGI-S p=0.052, 反應者的百分比 (定義為基線減少超過 25%) p=0.033 | |||
| 17242628 | 2563 NM; 171 PM | NA (*3, *4, *5, *6, *7, *8 被基因型並且患者被分組 PM 為其中之一或兩個 同型合子(Homozygous) 的組合;所有其他患者分組為 NM) | 2734 名兒童和青少年 ADHD,所有研究合併 (不清楚每個研究的生命體徵數量) | 非洲裔、亞洲裔、白人、西班牙裔、其他 | ATX 劑量 >1.2 mg/kg/day | PM 與 NM 相比,脈搏 (p<0.001) 和舒張壓 (p=0.012) 增加更大,對 NM 相比,體重增加無顯著差異 (p=0.088),對 QT 間期的影響無差異 | |||
| 17242628 | 313NM; 25 PM | NA (*3, *4, *5, *6, *7, *8 被基因型並且患者被分組 PM 為其中之一或兩個 同型合子(Homozygous) 的組合;所有其他患者分組為 NM) | 338 名兒童和青少年 ADHD | 非洲裔、亞洲裔、白人、西班牙裔、其他 | 1.0 mg/kg/day (分為每日兩次) | PM 的 最高血中濃度(Cmax) 平均值比 NM 高 5 倍 | |||
| 20691935 | NA | *1/ *4, *5/ *41 | 100 名兒童 ADHD | 荷蘭 | 0.6 至 1.8 mg/kg/day 根據反應 | 從 100 名患者中,有 10 名符合晚期效果的標準 (>9 週) 或 ADR,並被基因型檢測 CYP2D6 (*2, *3, *4, *5, *6, *9, *10, *41) 和 CYP2C19*2。攜帶 *1/ *4 (3) 和 *5/ *41 (1) 的患者因在 40mg 和 80mg 的 ADR 而中止治療。攜帶 *1/ *4 (1)、*2/*4、*2/*10 (1) 和 *1/*9 (1) 的患者在劑量從 60 降至 40 mg (*1/*4、*2/*4 和 *2/*10) 或從 40 降至 25 mg (*1/*9) 後顯示良好反應和耐受性 | |||
| 19387424 | NA | NA (*3, *4, *5, *6, *7, *8 被基因型並且患者被分組 PM 為其中之一或兩個 同型合子(Homozygous) 的組合;所有其他患者分組為 NM) | 兩項試驗 160 和 105 名兒童 ADHD,分別進行單獨和合併分析 | 混合和子分析僅在 CAUC 亞洲人中 | 0.5 mg/kg/day 至 1.8 mg/kg 每天 | 在使用 ADHDRS 終點值 (p>0.05) 測量的治療效果中,未發現顯著差異,經過 6 週的治療使用 ADHDRS 和 CGI-S 分數來確定反應 | |||
| 25919121 | UMs (>2 功能性 等位基因) n=67, NM (2 功能正常 等位基因) n=972, IM (正常 + 減少 n=79,正常 + 無 n=670,兩個減少 n=6),PM (兩個 功能缺失 等位基因) n=117 | *1/*1xN, *1/*1, *1/*10, *1/*17, *1/*3, *1/*4, *1/*5, *1/*6, *1/*7, *10/*10, *10/*17, *17/*17, *3/*3, *3/*4, *3/*5, *3/*6, *4/*4, *4/*4xN, *4/*5, *4/*6, *5/*5, *4xN/*5 | 1967 名成人 ADHD | 混合 | 40 mg/day 持續 2 週,然後增加至 80mg/day | 安全性和耐受性通過報告的治療出現 ADR 的頻率進行評估。與非 PM 相比,PM 的口乾、勃起功能障礙、多汗、失眠和尿潴留的頻率顯著較高。對於治療出現的不良事件,正常/超快速和 中間代謝型(Intermediate metabolizer) 之間未發現顯著差異。 | |||
| 26660002 | NM2 兩個 功能正常 等位基因 n=8,NM1 一個 功能正常 等位基因 n=8,IM n=3,PM n=4 | *1/*2xN, *1/*1, *1/*2, *2/*4, *1/*3, *1/*4, *2/*5, *2/*4, *9/*29, *10/*41, *5/*17, *4/*4, *4/*4xN, *4/*9 | 23 名兒童和青少年 ADHD | 混合 | 單次劑量研究,平均劑量為 0.43 +/-0.07 mg/kg | 劑量校正的 ATX 系統性暴露在受試者之間變化了 29.6 倍,範圍從 NM2 的 4.4±2.7 µM*h 到 EM1 的 5.8±1.7 µM*h、16.3±2.9 µM*h 和 50.2±7.3 µM*h,分別為 IM 和 PM (p<0.0001)。在代謝者組之間未見脈搏增加的差異。 | |||
| 17470523 | NA | *10, *17 | 體外 | NA | NA | 從昆蟲細胞中表達的重組 CYP2D6 的微粒體準備 | NA | NA | *2 + *10 + *87 + *88 + *90 + *91 + *93 + *95 + *97 與野生型相比,顯示出 ATX 的內源性清除率降低,*92 和 *96 的活性太弱,無法產生可測量的 4-OH ATX 形成。研究未報告創建星號 等位基因 的確切變異;例如 *2[] |
ADHD: 注意力不足 – 過動症; ADHDRS: 注意力不足 – 過動症評分量表; ATX: atomoxetine; AUC: 血漿濃度-時間曲線下面積 NM: 正常 (前廣泛) 代謝者; PM: 弱代謝型(Poor metabolizer); NA: 不可用 (未報告)