CPIC 指南註解:efavirenz 與 CYP2B6 基因
摘要
考慮對於 CYP2B6 弱代謝型(Poor metabolizer)的患者,以減少劑量的 efavirenz 400 或 200 mg/天開始治療。考慮對於 CYP2B6 中間代謝型(Intermediate metabolizer)的患者,以減少劑量的 efavirenz 400 mg/天開始治療。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC®關於efavirenz和CYP2B6的指引。
2019年4月
2019年4月線上提前發表。
-
關於含efavirenz的抗逆轉錄病毒療法在CYP2B6基因型下的CPIC指引已發表於《Clinical Pharmacology and Therapeutics》期刊。
-
這些指引適用於:
-
兒科患者
-
成人患者
-
-
2019年efavirenz劑量指引摘錄:
-
「大量證據顯示CYP2B6基因型與血漿中efavirenz濃度的變異性及不良反應有關。大多數研究已檢驗CYP2B6 c.516G>T和c.983T>C的影響;因此,這些變異提供了我們臨床建議的基礎。」
-
「多項研究顯示,CYP2B6 弱代謝型(Poor metabolizer)基因型,特別是由CYP2B6 c.516G>T和/或c.983T>C的同型合子或複合異型合子所定義,與efavirenz清除率降低及efavirenz毒性(特別是中樞神經系統毒性、肝損傷和QTc延長)及/或治療中止的風險增加有關,儘管有些研究未顯示此關聯。」
-
「根據目前的證據,CYP2B6 正常代謝型(Normal metabolizer, NMs)預期具有正常的efavirenz代謝,並以標準劑量(600 mg/天)達到治療性efavirenz濃度。CYP2B6 中間代謝型(Intermediate metabolizer, IMs)可能會經歷較高的劑量調整血清谷濃度(Ctrough),與NMs相比,這可能使這些患者的副作用風險增加至1.3倍。對於這些患者,有「中等建議」建議考慮以減少劑量400 mg/天開始efavirenz。CYP2B6 弱代謝型(Poor metabolizer, PMs)與NMs和IMs相比,具有最高的劑量調整血清谷濃度(Ctrough)風險,並且總體血漿efavirenz暴露更大,這使這些患者的副作用和治療中止風險增加至4.8倍。對於這些患者,有「中等建議」建議考慮以減少劑量400或200 mg/天開始efavirenz。」
-
「CYP2B6 RMs和UMs可能會經歷與正常代謝型(Normal metabolizer)相比略低的劑量調整血清谷濃度(Ctrough),這對efavirenz可能具有臨床重要性。然而,根據目前的證據,功能增強 等位基因 CYP2B6*4和*22的影響似乎是適度的。因此,目前的數據不足以建議改變正常處方,RM或UM 表現型的患者應接受標準efavirenz劑量。」
-
「兒科: Efavirenz已獲FDA批准用於3個月及以上年齡且體重≥3.5 kg的兒童作為抗逆轉錄病毒療法的一部分。在美國,efavirenz有膠囊(50或200 mg);片劑(600 mg);固定劑量組合包含efavirenz 600 mg、emtricitabine 200 mg和tenofovir disoproxil fumarate 300 mg;以及最近為體重≥35 kg的兒童提供的固定劑量組合Symfi Lo®(efavirenz 400 mg、lamivudine 300 mg和tenofovir disoproxil fumarate 300 mg)。美國衛生與公共服務部(DHHS)關於兒童HIV感染中抗逆轉錄病毒藥物使用的指引建議efavirenz與兩種核苷類逆轉錄酶抑制劑(NRTIs)聯合使用作為初始治療HIV的替代非核苷類逆轉錄酶抑制劑(NNRTI)方案。」
-
「年齡<3歲的兒童。類似於DHHS指引,我們不建議在3個月至<3歲的嬰兒和兒童中使用efavirenz,除非在特殊情況下如結核病合併感染。如果臨床情況需要在此年齡組中使用efavirenz,CYP2B6測試可能提供信息,並且劑量可以根據當前DHHS指引進行指導,這些指引由IMPAACT研究P1070(36)提供信息。指引建議根據體重組對CYP2B6差(c.516T/T)代謝者進行efavirenz劑量減少:5 kg至<7 kg:50 mg;7 kg至<14 kg:100 mg;14 kg至<17 kg:150 mg;和≥17 kg:150 mg。正常(c.516G/G)代謝者和中間(c.516G/T)代謝者的劑量如下:5 kg至<7 kg:300 mg;7 kg至<14 kg:400 mg;14 kg至<17 kg:500 mg;和≥17 kg:600 mg。儘管當前DHHS兒科efavirenz劑量指引未考慮c.983T>C,我們建議c.516T/T的劑量建議也適用於c.516T/c.983C和c.983C/C。我們還建議在開始治療兩週後測量血漿efavirenz濃度。從成人臨床監測數據中得出的1至4 mg/L的中劑量血漿efavirenz濃度目標通常也適用於兒科患者的血清谷濃度(Ctrough)。」
-
「年齡>3歲且體重<40 kg的兒童。雖然已證明CYP2B6基因型對efavirenz暴露的影響在體重小於40 kg的三歲以上兒童中,但支持CYP2B6基因型指導劑量的具體臨床數據有限。因此,儘管我們無法對此年齡和體重組基於CYP2B6基因型的劑量調整做出明確建議,但CYP2B6基因型幾乎肯定會影響這些兒童的efavirenz暴露,因此對CYP2B6 弱代謝型(Poor metabolizer)的efavirenz劑量減少也是合理的。治療藥物監測(TDM),如果可用且可獲得,可能有助於在此年齡/體重組中指導劑量調整,特別是在潛在藥物相關毒性、病毒反彈或依從患者缺乏反應的情況下。對於體重40 kg或以上的兒科患者,適用成人劑量(見表2)。」
-
-
下載並閱讀:
表1:根據CYP2B6 表現型推薦的Efavirenz劑量
改編自2019年指引的表1和表2。
| CYP2B6 表現型 | 基因型 | 雙倍型的例子 | 影響 | 劑量建議 | 建議等級 |
|---|---|---|---|---|---|
| 超快速代謝型(Rapid metabolizer) | 攜帶兩個功能增強 等位基因s的個體 | *4/*4, *22/*22, *4/*22 | 與正常代謝型(Normal metabolizer)相比,efavirenz的劑量調整血清谷濃度(Ctrough)略低 | 以標準劑量(600 mg/天)開始efavirenz | 強烈建議 |
| 快速代謝型(Rapid metabolizer) | 攜帶一個功能正常 等位基因和一個功能增強 等位基因的個體 | *1/*4, *1/*22 | 與正常代謝型(Normal metabolizer)相比,efavirenz的劑量調整血清谷濃度(Ctrough)略低 | 以標準劑量(600 mg/天)開始efavirenz | 強烈建議 |
| 正常代謝型(Normal metabolizer) | 攜帶兩個功能正常 等位基因的個體 | *1/*1 | 正常的efavirenz代謝 | 以標準劑量(600 mg/天)開始efavirenz | 強烈建議c |
| 中間代謝型(Intermediate metabolizer) | 攜帶一個功能正常 等位基因和一個功能減弱 等位基因或一個功能正常 等位基因和一個功能缺失 等位基因或一個功能增強 等位基因和一個功能減弱 等位基因或一個功能增強 等位基因和一個功能缺失 等位基因的個體 | *1/*6, *1/*18, *4/*6, *4/*18, *6/*22, *18/*22 | 與正常代謝型(Normal metabolizer)相比,efavirenz的劑量調整血清谷濃度(Ctrough)較高;中樞神經系統不良事件的風險增加。 | 考慮以減少劑量400 mg/天開始efavirenza,b。 | 中等建議 |
| 弱代謝型(Poor metabolizer) | 攜帶兩個功能減弱 等位基因s或兩個功能缺失 等位基因s或一個功能減弱 等位基因和一個功能缺失 等位基因的個體 | *6/*6, *18/*18, *6/*18 | 與正常代謝型(Normal metabolizer)相比,efavirenz的劑量調整血清谷濃度(Ctrough)較高;中樞神經系統不良事件和治療中止的風險顯著增加 | 考慮以減少劑量400或200 mg/天開始efavirenza,b。 | 中等建議 |
| a如果治療藥物監測(TDM)可用且開出減少的efavirenz劑量,考慮獲取穩定狀態的血漿efavirenz濃度以確保濃度在建議的治療範圍內(約1至4 µg/mL)。 | |||||
| b在多藥方案中以減少的劑量400 mg/天或200 mg/天開出efavirenz可能需要每天服用多於一顆藥丸。如果是這樣,提供者應權衡減少劑量的潛在益處與增加藥丸數量的潛在不利影響。 | |||||
| cENCORE研究顯示,在隨機開始efavirenz為基礎的方案(與tenofovir和emtricitabine聯合)的初治患者中,400 mg/天在CYP2B6基因型無論如何均不劣於600 mg/天。 |
Efavirenz 途徑, 藥物動力學
概括
Efavirenz 的代謝及其對 [[KEEP_6350687]] 的作用機制的示意圖。
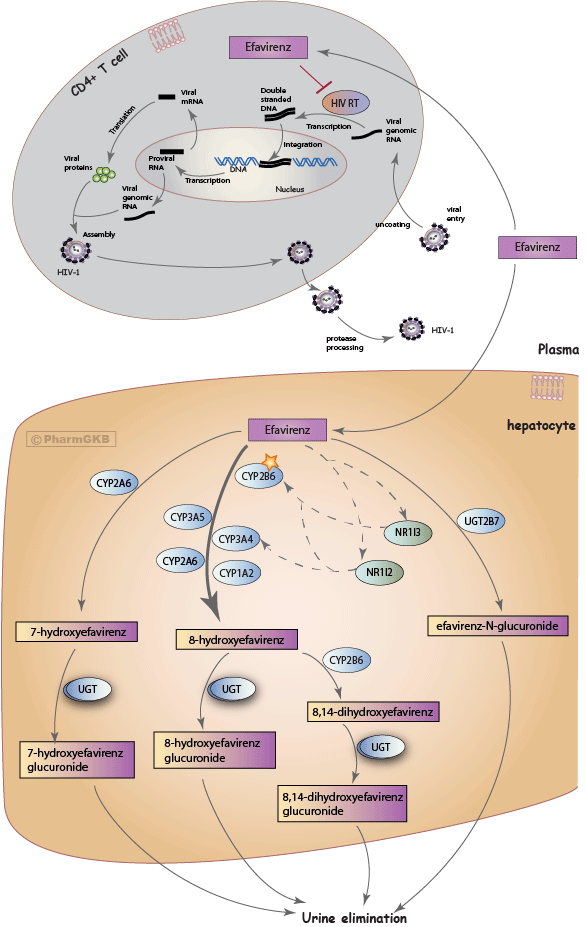
描述
背景
efavirenz (EFV) 被用作高效抗逆轉錄病毒療法 (ART) 方案 (HAART) 的 pART,以對抗 HIV-1 感染 [Articles:22474613, 24390631]。正確的抗病毒藥物劑量至關重要:血漿中 EFV 的濃度過高可能增加毒性風險,包括神經毒性(如睡眠障礙和幻覺) [Articles:21288825, 22162992, 23734829, 23859571],而濃度過低則可能與病毒學失敗相關 [Articles:11192870, 15167626]。建議的治療 EFV 範圍為 1-4 &u; g/mL,儘管血漿濃度超過 4 &u; g/mL 的患者並未經歷比低濃度患者更顯著的副作用,且尚不清楚低於 1 &u; g/mL 的濃度是否與遵循 EFV 治療的患者病毒學失敗增加相關 [Articles:16433869, 23172109]。參與 EFV 分解的酶在這一平衡中扮演重要角色。HIV 患者同時服用的藥物可能通過抑制或誘導這些酶來影響 EFV 水平,而 EFV 本身則通過增加這些酶的表達或活性來誘導自身代謝。編碼這些酶的基因中的多態性也可能影響 EFV 濃度,幫助解釋在給予相同建議每日劑量時,個體之間觀察到的 EFV 血漿濃度的高變異性 [Articles:11192870, 16778716, 20723261, 24477223]。在本摘要中,我們專注於後者的相互作用:藥物基因體學 的 EFV。
藥效學
目前有多種抗逆轉錄病毒藥物可用,針對 HIV-1 生命週期的不同階段(詳見 [Article:22474613])。EFV 是針對 HIV-1 逆轉錄酶的分子之一,防止從單鏈病毒 RNA 基因組形成病毒雙鏈 DNA(圖 1) [Article:22474613]。這些藥物可分為兩類:核苷酸底物的類似物(核苷酸逆轉錄酶抑制劑:NRTIs)和非 NRTIs(NNRTIs),後者結合在逆轉錄酶酶的非催化位點;EFV 屬於後者 [Article:22474613]。編碼 HIV-1 逆轉錄酶的基因中的突變與對 NRTIs 和 NNRTIs 的耐藥性相關,包括 EFV [Article:22759796];然而,在本摘要中,我們專注於人類基因組中的變異及其對 EFV 藥物動力學 和治療的影響。
藥物動力學
[[KEEP_3bfd52c]] 的主要代謝途徑是生成 8-hydroxyefavirenz(8-羥基-EFV),主要由 CYP2B6 形成(圖 1) [Articles:12676886, 17559344, 20335270]。在人類肝微粒體中的研究顯示,8-羥基-EFV 的形成速率在不同樣本中顯示出相當大的變異性 [Article:20335270]。CYP3A4、CYP3A5、CYP1A2 和 CYP2A6 可能在這一外源代謝步驟中發揮次要作用 [Articles:12676886, 17559344, 20335270]。CYP2B6 也是形成次級代謝物 8,14-二羥基-EFV 的主要酶 [Articles:12676886, 17559344]。此外,EFV 可以被 CYP2A6 羥基化為 7-羥基-EFV,這是一種次要 途徑 的 EFV 代謝,約占整體 EFV 代謝的 23% in vitro [Articles:17559344, 20335270]。因此,存在三種羥基化的 EFV 代謝物:8-羥基-EFV、8,14-二羥基-EFV 和 7-羥基-EFV。
EFV 的主要排泄方式是以葡萄糖醛酸酯的形式通過尿液排出,其中 8-羥基-EFV-G葡萄糖醛酸酯是主要的代謝物 [Article:10534318]。多種 UDP-葡萄糖醛酸轉移酶 (UGT) 同種型(包括 UGT1A1、1A3、1A7、1A8、1A9、1A10 和 2B7)可以作用於三種羥基化的 EFV 代謝物,生成葡萄糖醛酸形式 [Articles:10534318, 21319958, 22252501]。in vitro 的研究顯示,EFV 可以直接被 EFV- N - 葡萄糖醛酸化,通過 UGT2B7(儘管這在第一次服用 EFV 後是次要 途徑) [Articles:10534318, 19487252, 21319958, 21282425, 22252501]。EFV- N - 葡萄糖醛酸酯的形成速率在不同的人類微粒體樣本之間顯示出較大的變異性,而 7-羥基-EFV-G、8-羥基-EFV-G 和 8,14-羥基-EFV-G 的形成則沒有顯著變異 [Article:21319958]。
EFV-酶相互作用和 藥物交互作用
孕烯 X 受體 (PXR、NR1I2) 和構成性雄烯受體 (CAR、NR1I3) 被不同藥物以不同程度激活。它們的靶基因包括參與外源物質代謝和排除的基因,因此可能是 藥物交互作用 的基礎 [Articles:16513849, 17041008, 23172109]。EFV 被認為通過誘導 CYP2B6 和 CYP3A4 的表達來增強自身代謝(自誘導),這是通過激活 NR1I3 和 NR1I2 實現的 [Articles:9878993, 15496645, 17041008, 20861742]。其他藥物也可以誘導 CYP2B6 和 CYP3A4 的表達,包括利福平(通常與 EFV 同時服用的抗結核藥物,在 HIV 和結核共感染的患者中)通過激活 NR1I2 [Articles:16513849, 17041008, 20861742]。in vitro,EFV 被觀察到通過 CYP2B6 競爭性抑制布普洛尼 4-羥基化,並抑制 CYP2C8、CYP2C9 和 CYP2C19 的活性 [Articles:11225565, 23385314]。
藥物基因體學的研究提供了對患者之間 EFV PK 變異性的見解 [Article:16863456]。EFV 對代謝酶的影響,以及 藥物交互作用 在 EFV 和其他抗逆轉錄病毒或 HIV 患者常用藥物之間的相互作用,可能影響治療的安全性、依從性和療效;然而,這些影響在患者之間變化,因此難以預測 [Article:16863456]。例如,在接受 EFV- 基於 HAART 的治療的患者中,當比較第 1 天和第 14 天的樣本時,一些患者表現出 EFV 口服清除率的增加(自誘導),而其他患者則沒有,並且在那些有增加的患者中,口服清除率的增加程度也存在變異 [Article:22107359]。重要的是,收集和比較樣本的時間點可能會影響觀察到的自誘導程度 [Article:20881953]。EFV 的自誘導也受到患者基因型的影響;例如,具有 CYP2B6 *1 等位基因 的患者可能會表現出長期的 EFV 自誘導 [Articles:20881953, 21846671]。在某些情況下,治療藥物監測(TDM) 的抗逆轉錄病毒療法可能有助於通過個性化劑量來解決這些問題,以最小化副作用,同時保持抗病毒療效 [Articles:16863456, 20720517],儘管需要注意的是,EFV 通常以固定劑量與抗病毒方案共同配方,這為劑量的個性化增加了一層複雜性。
藥物基因體學
涉及 EFV PK 的酶基因中的變異已被研究與 PK 參數、臨床結果和副作用(如神經學(CNS)毒性)相關,這是服用 EFV 的患者中最常報告的不良事件之一。
CYP2B6 變異
由於 CYP2B6 是參與 EFV 代謝的主要酶,因此 CYP2B6 基因中的多態性已被廣泛研究與 EFV PK 參數、毒性和治療反應的關聯。這些在表 1 中進行了總結,以下將詳細描述其中兩個變異。
[]大量研究調查了 CYP2B6 516G>T SNP 對 EFV PK、療效和副作用的影響,這是與 EFV PK 途徑 相關的最常研究的變異。該多態性中的 T 等位基因 存在於幾個 CYP2B6 單倍型:*6A-C、*7A、*7B、*9、*13A、*13B、*19、*20、*26、*34、*36、*37、*38。使用人類肝樣本的研究表明,它導致一種 CYP2B6 mRNA 剪接變異,缺少外顯子 4 到 6(稱為 SV1),因此導致功能性 CYP2B6 mRNA 水平降低 [Article:18171905]。與其對 CYP2B6 表達的影響相關,T 等位基因 與 EFV 血漿濃度的增加和中位數估計的 C min 值相關,與 G 等位基因 的患者相比 [Articles:18281305, 23080225, 23172109]。
許多研究報告了在 HIV- 感染患者中,TT 基因型與增加的 EFV 血漿濃度、降低的清除率或與 GG 和/或 GT 基因型患者相比的藥物暴露之間的關聯(表 1)。TT 基因型在非裔美國人和黑人中比在歐洲裔美國人或白人中更為常見,這可能解釋了這些人群之間觀察到的 EFV 血漿濃度的差異 [Articles:15622315, 19486190]。GT 基因型的患者與 GG 基因型患者相比,也有增加的 EFV 血漿濃度和暴露(表 1)。此外,許多研究中觀察到基因劑量效應,EFV 的清除率遵循 TT<GT<GG 的模式,EFV 的濃度遵循 TT>GT>GG 的模式 [Articles:15622315, 17356468]。TT 和 GT 基因型也與較高的細胞外周血單核細胞 (PBMC) EFV 濃度和暴露相關,與 GG 基因型相比(表 1)。
Clifford 等人顯示,EFV- 治療的患者在治療的第一週經歷了顯著更多的 CNS 症狀,與非 EFV 組相比,但兩組之間的差異迅速減少,並且在治療四週後不再顯著 [Article:20133265]。在 EFV 的患者中,T 等位基因 的增加暴露的臨床相關性已被研究;然而,結果對於毒性、治療終止或療效的關聯仍不清楚,一些研究發現顯著關聯,而其他研究則沒有(表 1)。
對於這一變異的基因分型可能有助於在某些情況下個性化 EFV 劑量。在一組 HIV- 感染的兒童中,GG 基因型與發展為亞治療性 EFV 血漿濃度的概率為 50-70% 相關,且 GG 基因型的患者需要更高的劑量調整 [Article:18839779]。相反,台灣的 GT 或 TT 基因型患者在與毒性相關的血漿 EFV 濃度(>4 mg/L)方面的風險顯著增加 - 兩名患者因神經毒性副作用中止 EFV 治療,且兩者的 EFV 血漿水平均高於 4mg/L [Article:24551111]。
有建議認為 CYP2B6 基因分型可以用作篩查,以識別可能是慢或快代謝者的個體,並可能最能從早期 治療藥物監測(TDM) (TDM) 中受益,以便在開始藥物治療之前或期間根據暴露優化劑量 [Articles:16392090, 20720517]。例如,一項回顧性研究報告稱,在 31 名具有一個或兩個 516 T 等位基因 的患者中,從標準的 600 mg/天劑量 EFV 減少到 400 mg/天,降低了平均 EFV C min(在 600 mg/天時為 5.7 ± 3.4 mg/l)至治療範圍內(在 400 mg/天時為 2.39 ± 1.28 mg/l) [Article:24956253]。作者還報告稱,對這些患者減少劑量也與報告 CNS 不良事件的患者百分比減少(從 89.3% 降至 9.7%)、CD4+ 淋巴細胞計數的增加(從 483.9-x10 6 細胞 / 微克增加至 600.8 x 10 6 細胞 / 微克),以及無法檢測到 HIV 病毒載量的患者百分比增加(從 93.5% 增加至 100%)。有趣的是,所有 516 T/T 基因型的患者都需要進一步減少至 200 mg/天 EFV,支持對慢代謝者減少 EFV 劑量的做法 [Article:24956253]。在考慮基於 藥物基因體學 測試的劑量調整之前,重要的警告是 EFV 和其他抗逆轉錄病毒藥物作為 ART 的一部分被處方,這是一個更複雜的方案 (ART 和 HAART),並且可能作為固定劑量共同配方的一部分給予。
總之,CYP2B6 516G>T 變異與 EFV 血漿濃度之間存在明顯的關聯,儘管這一變異與 EFV 治療反應之間缺乏明確的關係,可能表明寬廣的治療窗口,以及抗 HIV 方案的 藥物交互作用 的複雜性 [Article:16267764]。
- 983T>C, rs28399499
C 等位基因 是 *18 等位基因 的唯一變異,並且也存在於 CYP2B6 *16(連同 785A>G)。C 等位基因 與相比於 T 等位基因 的增加 EFV 血漿濃度相關 [Article:18281305]。基因型 CC 和/或 CT 已被報導與相比於 TT 基因型的增加 EFV 血漿濃度和藥物暴露相關,但其他研究報告 CT 基因型與 TT 基因型之間的 EFV 濃度沒有顯著差異(表 1)。可能需要對 CYP2B6 516G>T 基因型進行調整,以觀察到與 983T>C 之間的關聯(如在 [Article:[ 中顯示的 EFV 濃度)。影響研究之間差異的另一個因素可能是某些人群中 C 的低或缺失頻率:C 等位基因 在非洲、黑人或非裔美國人群中發現的頻率為 0.05-0.08,但在白人、亞洲或智利人群中未被識別 [Articles:17391322, 18281305, 23172109, 24316028]。這一多態性的臨床相關性尚不清楚。在一組 170 名黑人和白人個體中,只有兩名患者具有 CC 基因型,並因毒性而退出 EFV- 含 HAART 治療 [Article:18281305]。另一方面,CC 和 CT 基因型與與 TT 基因型相比,喪失免疫或中樞神經系統 (CNS) 毒性的風險無關,在接受 EFV 治療的加納患者中 [Article:24080498]。
表 1:EFV PGx 變異的關聯總結 CYP2B6 基因
| 變異通用名稱 | 變異映射信息 | 與 EFV 在 HIV- 感染患者中的關聯 | 關聯類型 | 參考文獻 | |
|---|---|---|---|---|---|
| *1) 516G>T__ | rs3745274, NM_000767.4:c.516G>T, NP_000758.1:p.Gln172His | TT 基因型與增加 EFV 血漿濃度、降低的清除率和與 GG 和/或 GT 基因型相比的藥物暴露或血漿暴露相關。 | PK | [Articles:19659438, 18281305, 15622315, 20625352, 20723261, 19779319, 24080498, 20860463, 19371316, 19779319, 24551111, 24316028, 23399569, 23172109, 23970651, 16267764, 18839779, 22927450, 24145522, 15864119, 23254426, 20441246, 15825040, 17356468, 22057858, 24956253, 20338069, 22950382, 22481606, 19704172, 18728241, 19124658, 20952418] | |
| TT 基因型與治療中斷後血漿濃度延長(最多 14 天)相關,相比之下 GG(約 6 天)和 GT(7 天)基因型。 | PK | [Article:16392089] | |||
| GT 基因型與相比於 GG 基因型的增加 EFV 血漿濃度或血漿暴露相關。 | PK | [Articles:24551111, 15622315, 24316028, 23399569, 23172109, 19371316, 23970651, 23254426, 15825040]. | |||
| 基因型 SNP 與治療 2 週時的 EFV 血漿濃度無關。 | PK | [Article:20723261]。 | |||
| GT 和 TT 基因型與 PBMC- 相關的 EFV 濃度/暴露相比於 GG 基因型。 | PK | [Articles:20860463, 15864119]。 | |||
| GG 基因型的患者可能需要更高的劑量調整。 | PK | [Article:18839779]。 | |||
| TT 基因型與在 EFV- 含量的方案中治療時的睡眠障礙和疲勞相關。 | 毒性 | [Articles:15864119, 23734829, 24956253]。 | |||
| GT 基因型與在 EFV 治療 6 個月時相比於 GG 的睡眠質量較差的可能性增加,但在 4 或 12 個月時則沒有(在這項研究中,睡眠質量與 EFV 血漿水平無關)。 | 毒性 | [Article:23970651]。 | |||
| 基因型 TT 和 GT 與在 EFV 治療第 1 週時相比於基因型 GG 的中樞神經系統副作用的中位症狀得分變化較高,但在第 24 週時未見基因型之間的差異。 | 毒性 | [Article:15622315]。 | |||
| TT 基因型的患者經歷的整體副作用數量較 GG 基因型的患者多,但這並不具有統計學意義。 | 毒性 | [Article:20723261]。 | |||
| TT 基因型與在治療的 3 個月內中止治療相關。 | 毒性 | [Article:21715435]。 | |||
| 基因型 SNP 與在 EFV- 含量的方案中治療時的毒性相關治療失敗無關。 | 毒性 | [Article:16267764]。 | |||
| 基因型 GT 和 TT 與中樞神經系統毒性風險無關。 | 毒性 | [Article:24080498]。 | |||
| 基因型 SNP 與在最初接受 EFV- 含量的方案治療時轉換到全新治療方案或終止治療無關。 | 毒性/療效 | [Articles:16267764, 15622315]。 | |||
| 基因型 SNP 與病毒學失敗、血漿 HIV-1 RNA 拷貝 數量、治療 3 或 6 個月的病毒載量或 CD4+ T 細胞計數無關,當接受 EFV- 含量的方案治療時。 | 療效 | [Articles:16267764, 15622315, 20723261, 20338069]。 | |||
| 與 EFV 治療的加納患者中,與免疫學失敗風險增加相關的因素包括:基因型 GG(與基因型 TT 相比)、治療依從性低於 95% 和基線 CD4+ T 細胞計數低。 | 療效 | [Article:24080498。 | |||
| *2) 983T>C__ | rs28399499, NM_000767.4:c.983T>C, NP_000758.1:p.Ile328Thr | CC 和/或 CT 基因型與相比於 TT 基因型的增加 EFV 血漿濃度和藥物暴露相關 [CIT_415e3c81] | PK | [Articles:24080498, 18281305, 22927450, 20860463, 22481606]。 | |
| 未發現 CT 和 TT 基因型之間的 EFV 濃度的顯著差異。 | PK | [Articles:19371316, 19779319, 19239339]。 | |||
| 基因型 CC 和 CT 與在接受 EFV 治療時相比於 TT 基因型的免疫學失敗或中樞神經系統毒性風險無關。 | 毒性 | [Article:24080498。 | |||
| *3) 785A>G__ | rs2279343], NM_000767.4:c.785A>G, NP_000758.1:p.Lys262Arg | GG 基因型與相比於 AA 基因型的增加 EFV 濃度相關。 | PK | [Articles:23399569, 23254426, 20441246, 22481606]。 | |
| AG 基因型與相比於 AA 基因型的增加 EFV 濃度相關。 | PK | [Articles:23399569, 23254426]。 | |||
| 這些基因型與 SNP 濃度無關。 | PK | [Article:20625352。 | |||
| *4) g.18492T>C__ | rs2279345] | 基因型 CC 和 CT 與相比於 TT 基因型的較低 EFV 血漿濃度相關。 | PK | [Articles:24477223, 24293076, 24492364, 23254426。 | |
| *5) g.27103G>A__ | rs36118214], NM_000767.4:c.1294+586G>A, NG_007929.1:g.27103G>A | 基因型 AA 與相比於 AG 或 GG 基因型的血漿水平顯著較低。 | PK | [Article:19659438。 | |
| *6) 1459C>T__ | rs3211371], Arg487Cys, NP_000758.1, NM_000767.4 | 這些基因型與血漿濃度或暴露無顯著相關。 | PK | [Articles:18281305, 16267764, 23254426, 16433869, 23399569。 | |
| *7) rs4803419__ | 485-18C>T: NM_000767.4 | 在沒有變異 等位基因 的患者中 rs3745274 (516C>T) 和 rs28399499 (983T>C),等位基因 T 與較高的中位估計 EFV Cmin 值相關,儘管效應大小小於 rs3745274] T 等位基因。 | PK | [Article:23080225。 | |
| *8) 64C>T__ | rs8192709], Arg22Cys, NP_000758.1, 64C>T, NM_000767.4 | 基因型 CC 與在泰國患者中較高的 EFV 濃度(在 12 週時的中劑量 EFV 血漿濃度較高)相關。 | PK | [Article:23399569。 | |
| *9) 136A>G__ | rs35303484], CYP2B6*11, NM_000767.4:c.136A>G | 在比利時 50 名患者的隊列中,只有一名患者具有 AG 基因型,沒有患者具有 GG 基因型,且與 AA 基因型相比,最低血漿或 PBMC 濃度的變異性未見顯著關聯。 | PK | [Article:20860463] | |
| 這些基因型與 SNP 在接受 EFV- 含量的 ART 治療時的神經毒性綜合症(睡眠障礙、幻覺和認知影響)無顯著相關。 | 毒性 | [Article:23734829] | |||
| 10) CYP2B6*6 | 根據 CYP 命名法,*6A 定義為 516G>T 和 785A>G。 | 雙倍型 *1/*6、*5/*6 和 *6/*6 與增加 EFV 血漿濃度和降低清除率相關,而 *1/*1 與低 EFV 血漿濃度相關。 | PK | [Articles:23254426, 23399569, 24142869, 25096076, 20952418] | |
| 在具有 CYP2B6 基因型 *1/*5、*1/*6、*5/*6、*6/*6 的白人微粒體中觀察到的蛋白質顯著較低,與 *1/*1 的 8-羥基化顯著較低相關。 | PK | [Article:17559344] |
| 基因 | 變異通用名稱 | 變異映射信息 | 與 EFV 在 HIV- 感染患者中的關聯 | 關聯類型 | 參考文獻 |
|---|---|---|---|---|---|
| CYP1A2 | -739T>G | 在 62 名同時接受 HIV 和結核感染治療的盧旺達患者中,基因型 TG 與較高的 EFV 血漿水平相關,持續 6 週,相比於 TT 基因型患者,儘管在多變量分析中,所調查的三個 CYP1A2 SNPs(-739T>G、-163C>A 和 2159G>A)對 EFV 血漿水平變異的貢獻並不顯著。 | PK | [Article:24316028。 | |
| HTR2A | 102C>T | rs6313] | 這一變異與在多變量回歸分析中治療時的悲傷風險降低相關。 | 毒性 | [Article:23859571。 |
| ABCG2 | 421C>A | rs2231142] | 與在多變量分析中調整最大 穩定狀態(Steady state) 血漿濃度和人口學共變量後,與 EFV 治療相關的異常夢境風險增加相關。 | 毒性 | [Article:23859571]。 |
多變量分析
多個參與 EFV 代謝的基因中的多態性可能對整體 EFV 血漿濃度和隨之而來的療效和毒性結果有所貢獻。最近的研究檢查了多種因素對 EFV PK 參數變異的影響;這些結果在下文中進行了總結。[[TAG
進行中:黃麴毒素 b 途徑,藥物動力學
概括
參與 the toxin aflatoxin b1 代謝之候選基因示意圖
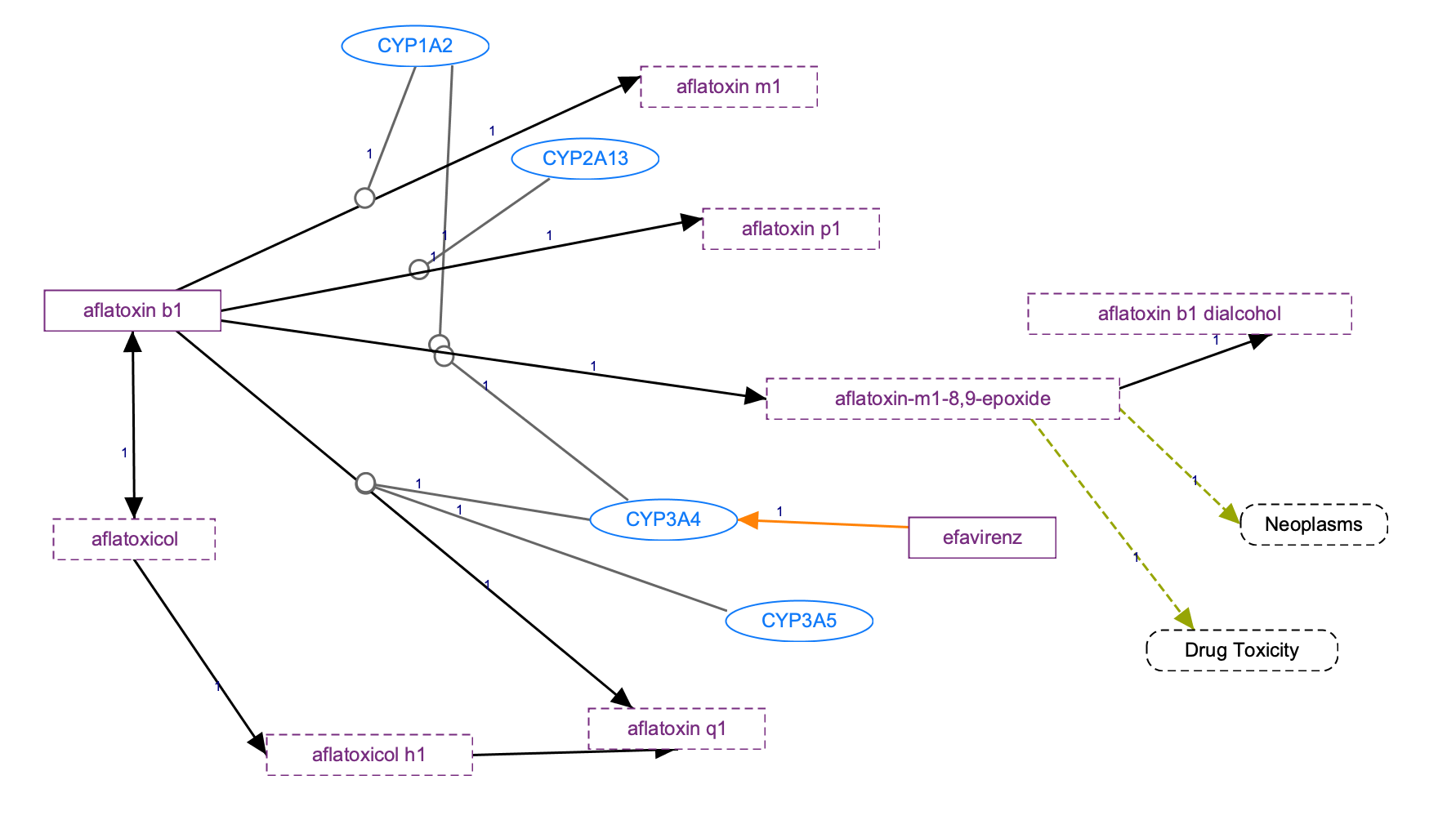
描述