CPIC 指南註解:aceclofenac、aspirin、diclofenac、dipyrone、indomethacin、lumiracoxib、nabumetone、naproxen 與 CYP2C9 基因
摘要
目前根據CYP2C9基因型對aceclofenac、aspirin、diclofenac、indomethacin、lumiracoxib、metamizole、nabumetone和naproxen的劑量進行無建議。
註釋
此註解係根據 CPIC® 關於非類固醇抗發炎藥物(Nonsteroidal Anti-inflammatory Drugs, NSAIDs)與 CYP2C9 的指引。CPIC 作者群已依據 CYP2C9 基因型,評估 aceclofenac、aspirin、diclofenac、indomethacin、lumiracoxib、metamizole、nabumetone 及 naproxen 的治療劑量建議。其結論指出,目前證據不足,尚無法提出可用於指引臨床實務的建議。
2020 年 3 月
-
關於 CYP2C9 與非類固醇抗發炎藥物的 CPIC 指引 發表於《Clinical Pharmacology and Therapeutics》期刊。
-
這些指引適用於:
-
兒科病人
-
成人病人
-
-
2020 年非類固醇抗發炎藥物劑量指引摘錄:
- "Aceclofenac、aspirin、diclofenac、indomethacin、lumiracoxib、metamizole、nabumetone 及 naproxen。表 S9 收錄了 CYP2C9 基因型與 aceclofenac、aspirin、diclofenac、indomethacin、lumiracoxib、metamizole、nabumetone 及 naproxen 表現型之間關聯的證據。這些藥物的藥物動力學在體內並未受到 CYP2C9 遺傳變異的顯著影響,且/或目前證據不足,無法提出可用於指引臨床實務的建議(CPIC 建議分類為「無建議」;CPIC 等級 C;表 S20)。"
-
下載並閱讀:
Platelet Aggregation Inhibitor 途徑, 藥效學
概括
抗血小板藥物對血小板聚集途徑的影響
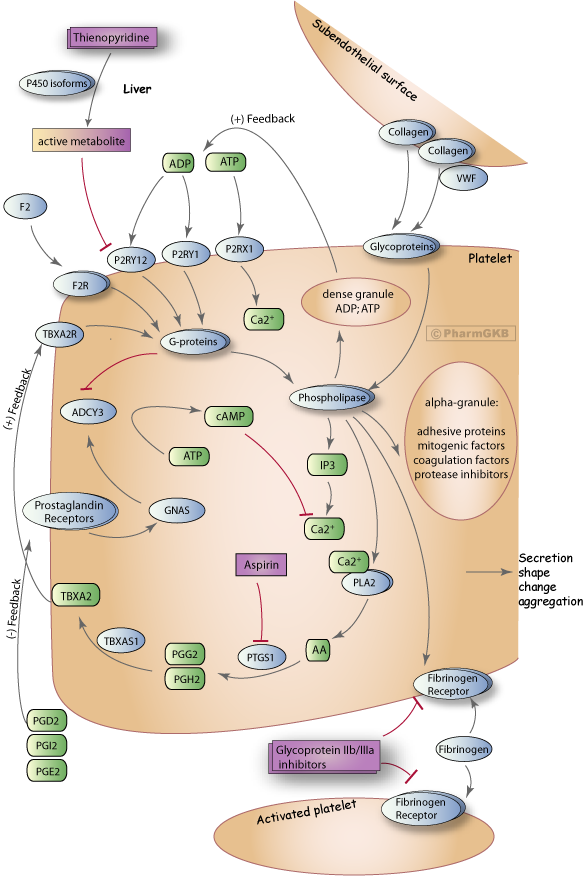
描述
血小板活化和凝血通常不會在完整的血管內發生。在血管壁受損後,血小板堵塞的形成是由血小板與內皮下膠原蛋白的黏附所啟動。在高剪切的動脈血流中,血小板首先因與膠原蛋白結合的冯·維爾布蘭因子 (VWF) 互動而減慢其血流速度,隨後通過其糖蛋白受體複合體直接與膠原蛋白結合而停止。這些膠原蛋白受體在血小板與膠原蛋白結合後的活化會啟動磷脂酶 C (PLC) 介導的級聯反應。這導致鈣從致密小管系統中動員。細胞內鈣的增加與多種激酶的活化有關,這些激酶對形態變化、促凝表面的呈現、血小板顆粒內容物的分泌、糖蛋白的活化以及磷脂酶 A2 (PLA2) 的活化都是必要的。PLA2 的活化釋放花生四烯酸 (AA),這是 TBXA2 合成的前體。PTGS1 催化 AA 轉化為 TBXA2 的第一步。這一反應被 aspirin 不可逆地阻斷,這也導致血小板聚集的阻斷。
這些過程導致如凝血酶、TBXA2 和 ADP 等分子的局部積累,這些分子對進一步招募血小板以及放大上述活化信號至關重要。分泌的激動劑活化其各自的 G 蛋白偶聯受體:凝血酶受體 (F2R)、血栓烷 A2 受體 (TBXA2R) 和 ADP 受體 (P2RY1 和 P2RY12)。P2RY12 受體與 Gi 偶聯,當被 ADP 活化時,抑制腺苷酸環化酶。這一互動抵消了內皮來源的前列腺素對 cAMP 形成的刺激,從而減輕 cAMP 對 IP3- 介導的鈣釋放的抑制作用。噻唑烷類藥物作為一類口服抗血小板藥物,永久性地抑制 P2RY12 信號,這足以阻止血小板活化。
F2R、TBXA2R 和 P2RY1 與 Gq-PLC-IP3-Ca2+ 途徑 偶聯,誘導形狀改變和血小板聚集。此外,通過 G12/13 (F2R; TBXA2R) 的受體信號也通過激活激酶促進形態變化。
血小板黏附、細胞骨架重組、分泌和放大迴路都是形成血小板堵塞的不同步驟。這些級聯反應導致在血小板細胞上表達的纖維蛋白原受體的活化。這一活化發展出纖維蛋白原的結合位點,這些位點在非活化的血小板中是不可用的。纖維蛋白原的結合導致活化血小板通過纖維蛋白原橋接連接,從而介導聚集。通過糖蛋白 IIb/IIIa 抑制劑抑制此受體可阻止任何激動劑誘導的血小板聚集。