CPIC 指南註解:lovastatin 與 SLCO1B1 基因
摘要
根據患者對SLCO1B1 功能減弱、可能為功能減弱或功能極低 表現型的需求,處方替代的他汀類藥物,取決於所需的效力。如果患者的SLCO1B1功能降低或可能降低,且需要使用lovastatin治療,劑量應限制在<20mg/天。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC® 指南,針對SLCO1B1、ABCG2和CYP2C9與他汀類藥物相關的肌肉骨骼症狀。
2025年9月
- 應CPIC成員的詢問,SLCO1B1藥物基因專家小組(PCEP)召集會議,重新評估在代表性不足的族群中頻率較高且有新興證據顯示與他汀類藥物引起的肌毒性相關的選定等位基因功能分配。*9和*31的證據摘要和證據強度分配已更新,而*39、*41和*45的功能分配已修訂,以反映其對SLCO1B1轉運蛋白活性影響的新數據。更多更新詳情,請參閱SLCO1B1 等位基因功能性參考文件的變更記錄。
2022年2月
-
CPIC指南,針對SLCO1B1、ABCG2和CYP2C9與他汀類藥物相關的肌肉骨骼症狀,已發表於《Clinical Pharmacology and Therapeutics》期刊。CPIC作者總結了支持如何應用SLCO1B1、ABCG2和CYP2C9基因型測試結果以優化新或現有他汀類療法以降低他汀類藥物相關肌肉骨骼症狀(SAMS)風險的文獻。當前文件取代了2012年原始指南和2014年針對SLCO1B1和辛伐他汀的更新。此指南新增了針對CYP2C9和ABCG2的建議以及所有他汀類藥物的建議。
-
此指南適用於:
- 成人患者
- 兒科患者
-
2022年他汀類藥物劑量指南摘錄:
-
「SLCO1B1促進他汀類藥物以及其他外源性和內源性化合物(例如膽紅素和17-β-葡萄糖醛酸酯雌二醇)的肝臟攝取。此轉運蛋白的功能減弱(通過基因變異遺傳或藥物介導的抑制獲得)可顯著增加他汀類藥物的全身暴露,這是與SAMS相關的推定因果因素。SLCO1B1基因位於12號染色體(Chr 12p12.2)上,雖然在此基因中已識別出許多單核苷酸變異(SNVs),但只有少數已知具有臨床相關的功能影響(SLCO1B1 等位基因 定義和功能表)」
-
「SLCO1B1中最常見且研究最透徹的變異是c.521T>C(rs4149056),可以單獨基因分型(例如,基於PCR的單一SNV測試)或在各種基於陣列的平台上進行多重測試。所有SLCO1B1基因測試應檢測c.521T>C;然而,儘管此基因中的其他較不常見的變異可能缺乏行動指導的證據,它們也可能很重要。」
-
-
下載並閱讀:
- 藥物基因體學臨床應用聯盟(CPIC)指南,針對SLCO1B1、ABCG2和CYP2C9與他汀類藥物相關的肌肉骨骼症狀
- 2022年補充文件
- 基因資訊表針對SLCO1B1
- Lovastatin Drug Resource Mappings
- Lovastatin Pre and Post Test Alerts
- Lovastatin CDS Flow Chart
表1:基於SLCO1B1 表現型的lovastatin推薦劑量
改編自2022年指南更新手稿的表1和表2。
| 表現型 | 基因型 | 雙倍型的例子a | 對lovastatin的影響 | lovastatin的劑量建議b,c | 建議等級 d |
|---|---|---|---|---|---|
| 功能正常 | 攜帶兩個功能正常 等位基因或一個正常加上一個功能增強 等位基因的個體 | *1/*1, *1/*14 | 典型的肌肉病變風險和他汀類藥物暴露 | 根據疾病別指南開立所需的起始劑量並調整劑量。 | 強烈建議 |
| 功能增強 | 攜帶兩個功能增強 等位基因的個體 | *14/*14 | 典型的肌肉病變風險和他汀類藥物暴露 | 根據疾病別指南開立所需的起始劑量並調整劑量。 | 強烈建議 |
| 功能減弱 | 攜帶一個正常或功能增強 等位基因加上一個功能缺失 等位基因的個體 | *1/*5, *1/*15 | 與功能正常相比,lovastatin酸暴露增加,這可能轉化為增加的肌肉病變風險 | 根據所需的效力開立替代他汀類藥物(見圖1中的替代他汀類藥物建議)。如果需要lovastatin治療,劑量限制在≤20mg/天。 | 中等建議 |
| 可能為功能減弱 | 攜帶一個功能缺失 等位基因加上一個不確定/功能未知 等位基因的個體 | *5/*6, *15/*10, *5/*43 | 與功能正常相比,lovastatin酸暴露增加,這可能轉化為增加的肌肉病變風險 | 根據所需的效力開立替代他汀類藥物(見圖1中的替代他汀類藥物建議)。如果需要lovastatin治療,劑量限制在≤20mg/天。 | 中等建議 |
| 功能極低 | 攜帶兩個功能缺失 等位基因的個體 | *5/*5, *5/*15, *15/*15 | 與正常和功能減弱相比,lovastatin酸暴露增加,這可能轉化為增加的肌肉病變風險 | 根據所需的效力開立替代他汀類藥物(見圖1中的替代他汀類藥物建議)。 | 中等建議 |
| 無法判定 | 攜帶一個功能正常 等位基因加上一個不確定或功能未知 等位基因或等位基因與不確定和/或功能未知 等位基因的組合的個體 | *1/*7, *1/*10, *7/*10 | 不適用 | 無建議。 | 無建議。 |
圖1:SLCO1B1建議,根據SLCO1B1 表現型分層的強度和他汀類藥物劑量;所有劑量均假設為成人劑量。
改編自2022年指南手稿的圖1
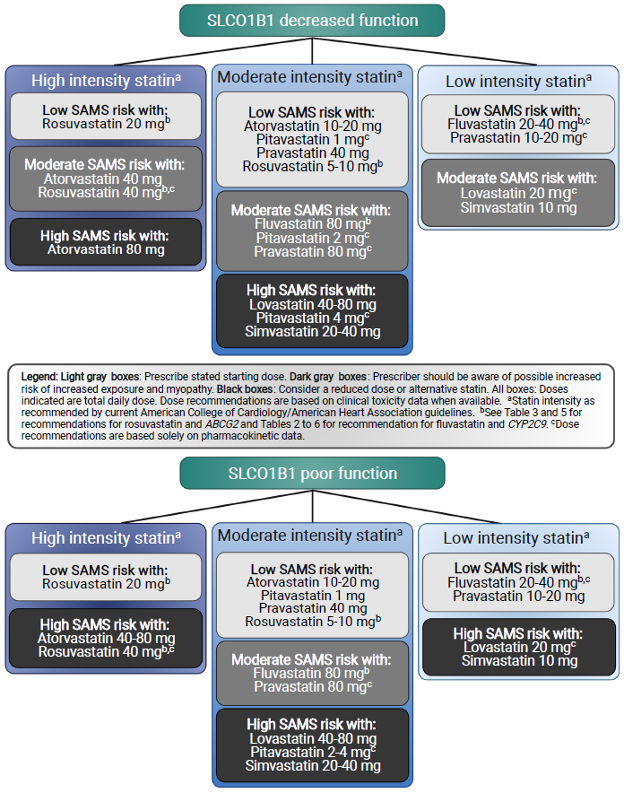
- 「治療建議:SLCO1B1。美國心臟病學會和美國心臟協會於2018年發布了更新的血膽固醇管理臨床實踐指南。在這些指南中,根據預期的LDL-膽固醇降低範圍,將不同日劑量的他汀類藥物分類為高、中或低強度他汀類藥物。例如,他們建議在有臨床動脈粥樣硬化性心血管疾病(ASCVD)證據的患者中啟動高強度他汀類藥物,這可能包括每天一次40或80 mg的atorvastatin或每天一次20或40 mg的rosuvastatin。圖1設計用於與上述指南結合使用,因為它提供了他汀類藥物建議,包括首選他汀類藥物強度和劑量,根據SLCO1B1 表現型(即減少或功能極低)分層。淺灰色框中指示的他汀類藥物和劑量可以以最低的SAMS風險開立。深灰色框中指示的他汀類藥物和劑量應謹慎使用(可能增加SAMS風險),而黑色框中指示的他汀類藥物和劑量應避免,因為現有證據表明它們與增加的危害風險相關。這些建議基於可用的藥代動力學和SAMS風險數據的組合,在大多數情況下,並根據每種強度內可用的他汀類藥物選擇數量提供信息。」
Lovastatin 途徑, 藥物動力學
概括
涉及Lovastatin的運輸和代謝的候選基因。
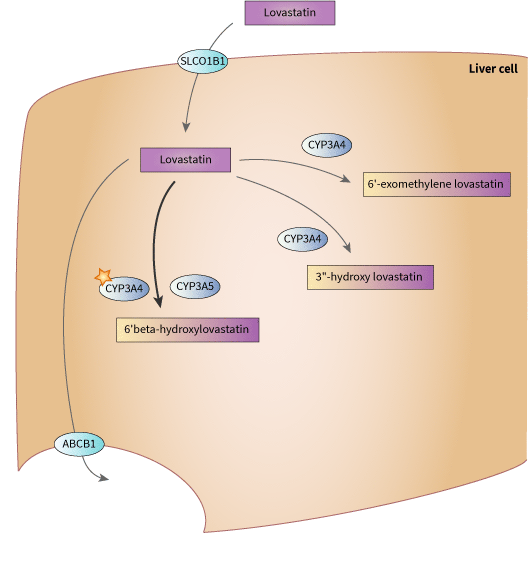
描述
背景
Lovastatin是一種HMG-CoA還原酶抑制劑(他汀類藥物),用於降低膽固醇。與其他他汀類藥物類似,pravastatin通過對3-羥基-3-甲基戊二酸輔酶A還原酶(HMGCR)的競爭性抑制來抑制內源性膽固醇的生成,該酶催化HMG-CoA轉化為美伐酸,如他汀藥效學途徑所示。
有關使用藥物基因組學信息進行Lovastatin劑量調整的指導方針已由臨床藥物基因體學實施聯盟(CPIC)發布。CPIC建議對於具有SLCO1B1 rs4149056 (521T>C) CC或TC基因型的患者,或具有SLCO1B1 功能減弱,或功能極低表現型的患者,考慮使用替代他汀類藥物。
代謝
Lovastatin以不活躍的內酯形式給藥,並在體內水解為相應的β羥基酸形式,這是一種強烈建議抑制劑,作用於HMG-CoA還原酶。肝臟中的廣泛首過代謝由CYP3A4和CYP3A5介導[Articles:17178259,10490896,20386561,7905377,2297361]。
運輸
Lovastatin是有機陰離子轉運蛋白SLCO1B1和外排轉運蛋白ABCB1的底物[Article:17178259]。SLCO1B1基因的遺傳變異與Lovastatin酸的暴露增加有關。攜帶rs4149056 (521T>C) C 等位基因的患者,其AUC的Lovastatin酸顯著增加[Articles:27967318,26020121],但對Lovastatin內酯沒有顯著影響。rs4149056 C 等位基因也與他汀類藥物引起的肌肉病變和橫紋肌溶解症的風險增加相關[Article:34114646]。