CPIC 指南註解:atorvastatin、fluvastatin、lovastatin、pitavastatin、pravastatin、simvastatin 與 ABCG2 基因
摘要
目前無基於ABCG2基因型的atorvastatin、lovastatin、fluvastatin、pravastatin、pitavastatin和simvastatin劑量建議。
註釋
此註釋基於CPIC® 指南,針對SLCO1B1、ABCG2和CYP2C9與他汀類藥物相關的肌肉骨骼症狀。
2022年2月更新
-
針對SLCO1B1、ABCG2和CYP2C9與他汀類藥物相關的肌肉骨骼症狀的CPIC指南已發表於《Clinical Pharmacology and Therapeutics》期刊。CPIC作者總結了文獻,支持如何應用SLCO1B1、ABCG2和CYP2C9基因型檢測結果來優化新的或現有的他汀類藥物治療,以降低他汀類藥物相關的肌肉骨骼症狀(SAMS)的風險。目前的文件取代了原始的2012年指南和2014年針對SLCO1B1和simvastatin的更新。此指南新增了針對CYP2C9和ABCG2的建議,以及針對所有他汀類藥物的建議。
-
此指南適用於:
- 成人患者
- 兒科患者
-
2022年他汀類藥物劑量指南摘錄:
- 「ABCG2。針對ABCG2的建議特定於rosuvastatin(表3)。對於具有ABCG2 功能極低的個體,建議rosuvastatin的起始劑量為≤20mg;然而,如果需要超過20mg的劑量以達到預期的療效,則建議使用替代他汀類藥物或聯合療法(例如,他汀類藥物+ezetimibe)。雖然肌肉病變的風險未知,但在具有c.421AA基因型的個體中,rosuvastatin的暴露量(AUC)比c.421CC基因型(野生型)高144%;因此,該建議主要基於藥代動力學數據。可能由於較高的肝臟暴露,ABCG2 c.421A變異也與在大型全基因組關聯研究中對rosuvastatin的膽固醇降低反應改善有關。rosuvastatin的選擇和劑量也應考慮亞洲祖源(表3,詳見補充材料中的更多討論)。Atorvastatin 藥物動力學也受ABCG2基因變異的影響;然而,目前證據不足以提供建議(無建議,CPIC等級C)。如前所述,基於ABCG2的基因變異提供其他他汀類藥物的建議的證據也有限。」
-
下載並閱讀:
Pitavastatin 途徑, 藥物動力學
概括
涉及Pitavastatin的運輸和代謝的候選基因表示。
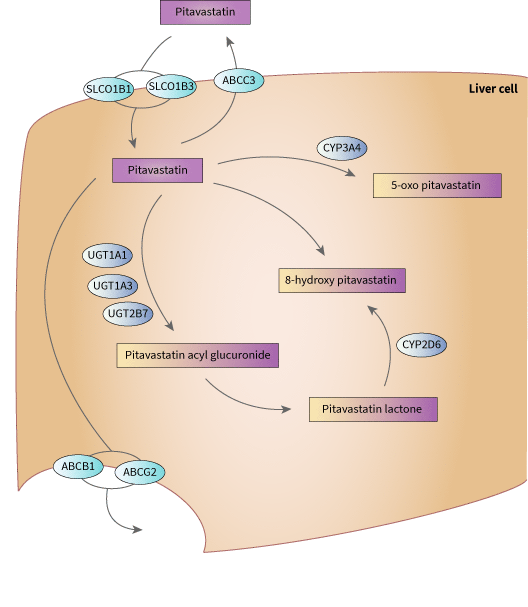
描述
背景
Pitavastatin是一種HMG-CoA還原酶抑制劑(他汀類藥物),用於降低高脂血症患者的膽固醇。與其他他汀類藥物類似,Pitavastatin通過競爭性抑制3-羥基-3-甲基戊二酸輔酶A還原酶(HMGCR)來抑制內源性膽固醇的生成,該酶催化HMG-CoA轉化為美伐酸,如他汀途徑、藥效學所示。
有關使用藥物基因組學信息進行Pitavastatin劑量調整的指導方針由臨床藥物基因體學實施聯盟(CPIC)發布。CPIC建議對於具有SLCO1B1rs4149056(521T>C)CC或TC基因型的患者,或具有SLCO1B1 功能減弱,或功能極低 表現型的患者,減少Pitavastatin的起始劑量。
代謝
Pitavastatin的主要代謝途徑是通過肝臟中的UDP-葡萄糖醛酸轉移酶(UGT1A1)、1A3和2B6進行葡萄糖醛酸化,隨後形成pitavastatin lactone。只有非常小的百分比的代謝是通過細胞色素P450系統進行的。它也稍微通過CYP2C9代謝。[Article:15118259]。
運輸
Pitavastatin是有機陰離子轉運蛋白的底物SLCO1B1和SLCO1B3 [Article:31699807]以及外排轉運蛋白ABCB1、ABCC3和ABCG2 [Articles:34045219、34162690]。
在SLCO1B1基因中的遺傳變異與Pitavastatin的暴露增加有關。攜帶rs4149056(521T>C)C 等位基因的患者具有增加的AUC和降低的Pitavastatin清除率。[Articles:16198653、17460607、18408565、30528195、23556337、23007012]。這一變異對Pitavastatin的降脂效果沒有顯著影響。[Article:20140004]。