CPIC 指南註解:atorvastatin、fluvastatin、lovastatin、pitavastatin、pravastatin、rosuvastatin、simvastatin 與 CYP3A4、CYP3A5、HMGCR 基因
摘要
目前有基於HMGCR、CYP3A4或CYP3A5基因型的atorvastatin、lovastatin、fluvastatin、pravastatin、pitavastatin、rosuvastatin和simvastatin劑量的無建議。
註釋
此註釋基於CPIC® 指南,涉及SLCO1B1、ABCG2和CYP2C9與他汀類藥物相關的肌肉骨骼症狀。
2022年2月更新
-
CPIC指南關於SLCO1B1、ABCG2和CYP2C9與他汀類藥物相關的肌肉骨骼症狀,已發表於《Clinical Pharmacology and Therapeutics》期刊。CPIC作者總結了文獻,支持如何應用SLCO1B1、ABCG2和CYP2C9基因型測試結果,以優化新的或現有的他汀類藥物治療,從而降低他汀類藥物相關的肌肉骨骼症狀(SAMS)的風險。目前的文件取代了原始的2012年指南和2014年關於SLCO1B1和simvastatin的更新。此指南新增了對CYP2C9和ABCG2的建議,並新增了對所有他汀類藥物的建議。由於證據薄弱且基於基因型的臨床行動缺乏結論性,無建議提供了關於他汀類藥物和CYP3A4/5及HMGCR的建議。
-
此指南適用於:
- 成人患者
- 兒科患者
-
2022年他汀類藥物劑量指南摘錄:
- 「我們審查了SLCO1B1、ABCG2、CYP2C9、CYP3A4/5和HMGCR的證據,並對每個證據進行分級,評估基因型與表現型之間的關聯(表S1-S5)。我們發現SLCO1B1(所有他汀類藥物)、ABCG2(rosuvastatin)和CYP2C9(fluvastatin)的證據水平最高,這些證據構成了當前指南中治療建議的基礎。CYP3A4/5和HMGCR的證據表格在補充資料中提供(表S4和S5)。基於證據薄弱且基於基因型的臨床行動缺乏結論性,無建議提供了關於他汀類藥物和CYP3A4/5及HMGCR的建議。」
-
下載並閱讀:
fluvastatin 藥物動力學途徑
概括
參與 fluvastatin 運輸、代謝與清除之候選基因示意圖
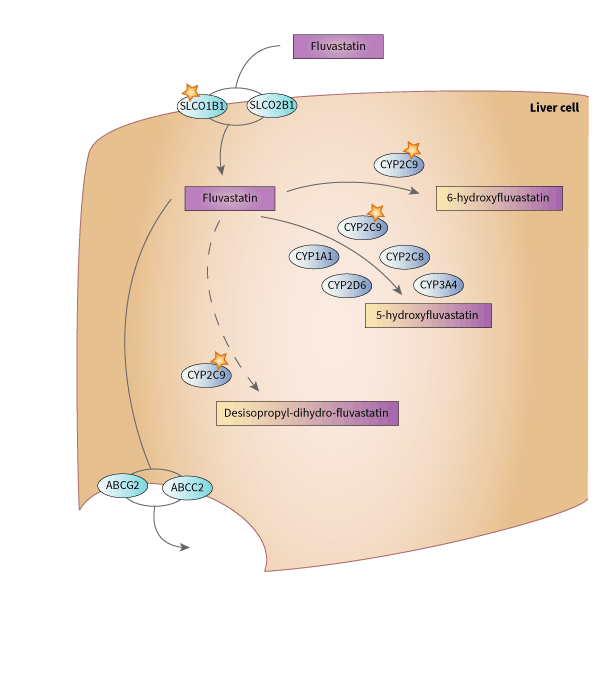
描述
背景
fluvastatin是一種HMG-CoA還原酶抑制劑(他汀類藥物),用於降低低密度脂蛋白(LDL)和總膽固醇的血液水平,並減緩動脈粥樣硬化的進展,降低接受血管重建手術的風險,適用於CHD患者。它通過競爭性抑制3-羥基-3-甲基戊二酸輔酶A還原酶(3-hydroxy-3-methylglutaryl coenzyme A reductase,HMGCR)來抑制內源性膽固醇的生成,該酶催化HMG-CoA轉化為mevalonate,如他汀類藥效學途徑所示。
關於在 rosuvastatin 劑量調整中如何運用藥物基因體學資訊,相關指引已由藥品仿單以及臨床專業學會(如臨床藥物基因體學實施聯盟,CPIC)發布。 對於功能降低的SLCO1B1或CYP2C9的患者,使用fluvastatin時可能面臨更高的他汀類肌肉病變風險。CPIC建議對這些患者減少起始劑量。如果需要更高劑量以達到期望的療效,應考慮使用其他他汀類藥物。荷蘭藥物基因體學工作小組(Dutch Pharmacogenetics Working Group, DPWG)已根據SLCO1B1基因型評估治療劑量的建議。他們得出結論,對於SLCO1B1 521TC或521CC和fluvastatine,這種基因-藥物相互作用不需要採取行動。“基因變異增加了fluvastatin的血漿濃度,但目前缺乏證據證明其對療效或副作用的影響。”
代謝
fluvastatin是一種脂溶性他汀類藥物,幾乎完全通過代謝排除[Article:17178259]。它在5位和6位進行羥基化(hydroxylation),並進行N-去異丙基化(N-deisopropylation),其中6羥基是最豐富的產物[Article:10064574]。體外實驗使用重組蛋白、微粒體和抑制劑顯示CYP2C9是主要的代謝酶,並能生成所有三種主要代謝物[Article:10064574]。其他酶能生成5-羥基,但效率較低[Article:10064574]。 fluvastatin是兩種對映異構體3R,5S‐fluvastatin和3S,5R‐fluvastatin的外消旋混合物,並且有證據表明這些對映異構體在藥物基因體學(PGx)上有輕微不同的影響[Article:30989645]。3R,5S‐fluvastatin的活性是3S,5R‐fluvastatin的30倍[Article:30989645]。
在CYP2C9的基因變異(*2, *3)與fluvastatin的暴露增加相關[Articles:30989645,22941809,32373204,19663817]。AUC的fluvastatin在拷貝的CYP2C9*2和CYP2C9*3變異中分別增加了25%和75%,其中CYP2C9*3的影響大於CYP2C9*2。此外,CYP2C9*2和CYP2C9*3 等位基因與增加的fluvastatin誘導的不良反應風險相關,包括肝臟和他汀類相關的肌肉毒性([Article:24024895])。CYP2C9的基因變異未被證明與fluvastatin的降脂反應相關[Articles:30363031,12891229]。SLCO1B1基因型可能對活性3R,5S‐fluvastatin有對映異構體特異性影響,rs4149056 (c.521T>C)與活性3R,5S‐fluvastatin的增加[Article:30989645]。
運輸
fluvastatin是肝臟運輸蛋白SLCO1B1和SLCO2B1的受質[Articles:16714062,15616150,24799396]。它也被確定為外排運輸蛋白ABCB1、ABCC2和ABCG2的受質[Articles:30989645,16198652,15548849]。