CPIC 指南註解:aminosalicylic acid、chloramphenicol、chloroquine、ciprofloxacin、dimercaprol、doxorubicin、furazolidone、glyburide、hydroxychloroquine、mafenide、nalidixic acid、norfloxacin、ofloxacin、phenazopyridine、quinine、sulfadiazine、sulfamethazine、sulfamethoxazole、sulfamethoxazole / trimethoprim、sulfanilamide、sulfasalazine、sulfisoxazole、tolbutamide、vitamin c、Vitamin K and analogues 與 G6PD 基因
摘要
對於具有G6PD 缺乏或G6PD 可變型(Variable) 表現型的患者,沒有理由避免使用低至無風險的藥物。在患有慢性非球形紅細胞溶血性貧血(chronic non-spherocytic hemolytic anemia, CNSHA)的G6PD 缺乏患者中,應謹慎使用低至無風險的藥物,並建議密切監測慢性溶血的急性加重。然而,CPIC不建議基於G6PD基因型改變低至無風險藥物的處方行為。
註釋
此註釋基於擴展的CPIC®指引,針對G6PD基因型的藥物使用。CPIC作者評估了攜帶G6PD變異的患者使用各種藥物的現有證據。
2022年9月
-
擴展的CPIC®指引,針對G6PD基因型的藥物使用已在《Clinical Pharmacology and Therapeutics》期刊中發表。作為該指引的一部分,作者將藥物按其在G6PD缺乏症患者中引起急性溶血性貧血(AHA)的風險進行分類。4-aminosalicylic acid, chloramphenicol, chloroquine, ciprofloxacin, dimercaprol, doxorubicin, furazolidone, glyburide, hydroxychloroquine, mafenide, nalidixic acid, norfloxacin, ofloxacin, phenazopyridine, quinine, sulfadiazine, sulfadimidine, sulfamethoxazole, sulfanilamide, sulfasalazine, sulfisoxazole, tolbutamide, vitamin C和vitamin K被分類為低至無風險藥物,如指引發表的表2所示。CPIC不建議基於基因型改變低至無風險藥物的處方行為,並且G6PD/低至無風險藥物基因/藥物對被CPIC分配為C級最終狀態。
-
這些指引適用於:
- 成人患者
- 兒科患者
-
指引摘錄:
- 「在此CPIC指引中增加了一個步驟,將藥物分為三組:在G6PD缺乏症存在下可被視為高風險的藥物(因此通常應避免),在G6PD缺乏症中被視為中等風險的藥物(因此應謹慎使用),以及可被視為低至無風險的藥物(在G6PD缺乏症患者中不會增加AHA風險)。」
- 「為了將藥物分配到風險組,作者不僅考慮了主要同行評審文獻中的證據強度,還考慮了藥物使用頻率、監管機構警告的存在以及是否存在可能產生活性氧物質並在G6PD缺乏症中促成溶血的機制(補充,分配風險等級)」
- 「Sulfamethoxazole(低至無風險藥物) 在G6PD缺乏症中sulfamethoxazole的風險類別。 Sulfamethoxazole被認為屬於低至無風險類別,因為將其與AHA聯繫起來的證據較弱(主要是病例報告,常常因感染、蠶豆或其他藥物的存在而混淆),且有幾項研究顯示在G6PD缺乏症中安全使用。一項研究報告顯示在10名缺乏嬰兒中未見此藥引起AHA。儘管有一些監管機構的警告,但大多數較弱。此外,sulfamethoxazole被廣泛使用,進一步證明缺乏支持顯著風險的研究。」
-
下載並閱讀:
- 擴展的藥物基因體學臨床應用聯盟(CPIC)指引,針對G6PD基因型的藥物使用
- 2022補充
- G6PD 基因資訊表
- 藥物資源映射
- 4-aminosalicylic acid
- chloramphenicol
- chloroquine
- ciprofloxacin
- dimercaprol
- doxorubicin
- furazolidone
- glyburide
- hydroxychloroquine
- mafenide
- nalidixic acid
- norfloxacin
- ofloxacin
- phenazopyridine
- quinine
- sulfadiazine
- sulfadimidine
- sulfamethoxazole/trimethoprim
- sulfanilamide
- sulfasalazine
- sulfisoxazole
- tolbutamide
- vitamin C
- vitamin K
- 測試前後警示
- 4-aminosalicylic acid
- chloramphenicol
- chloroquine
- ciprofloxacin
- dimercaprol
- doxorubicin
- furazolidone
- glyburide
- hydroxychloroquine
- mafenide
- nalidixic acid
- norfloxacin
- ofloxacin
- phenazopyridine
- quinine
- sulfadiazine
- sulfadimidine
- sulfamethoxazole/trimethoprim
- sulfanilamide
- sulfasalazine
- sulfisoxazole
- tolbutamide
- vitamin C
- vitamin K
- 低至無風險藥物流程圖
表1:低至無風險藥物在G6PD 表現型中的推薦治療使用
改編自指引的表1、2和6
| 預測表現型 | 基因型a | 基因型範例b | 影響 | 治療建議 | 建議等級c | 考量 |
|---|---|---|---|---|---|---|
| 正常 | 攜帶一個X染色體,帶有非缺乏(IV類)等位基因 或攜帶兩個非缺乏(IV類)等位基因者 |
B, Sao Boria, IV B/B, B/Sao Boria, B/A, IV/IV |
急性溶血性貧血的低至無風險 | 基於G6PD狀態,無理由避免低至無風險藥物 | 強烈建議 | |
| 缺乏 | 攜帶一個X染色體,帶有缺乏(II-III類)等位基因 或攜帶兩個缺乏(II-III類)等位基因者或一個I類等位基因和一個II或III類等位基因者 |
A-, Orissa, Kalyan-Kerala, Mediterranean, Canton, Chatham, II, III A-/A-, A-/Orissa, Orissa/ Kalyan-Kerala, Mediterranean/ Mediterranean, Chatham /Mediterranean, Canton/ Viangchan, II/II, II/III, III/III, I/II, I/III |
急性溶血性貧血的低至無風險 | 基於G6PD狀態,在標準劑量下無理由避免低至無風險藥物 | chloramphenicol, chloroquine, hydroxychloroquine, vitamin C, vitamin K: 中等建議 所有其他低至無風險藥物: 可選建議 |
對於高於正常劑量的情況,並在感染或其他氧化壓力的情況下,包括同時使用多種中等和低至無風險藥物時,可能需要更密切的監測。 |
| 嚴重缺乏合併慢性非球形紅細胞溶血性貧血(Deficient with CNSHA) | 攜帶一個X染色體,帶有缺乏(I類)等位基因 或攜帶兩個缺乏(I類)等位基因者d |
Bangkok, Villeurbanne, I Bangkok/Bangkok, Bangkok/Villeurbanne, I/I |
慢性溶血性貧血急性加重的高風險 | 在此組中應謹慎使用所有藥物;如果使用藥物,建議密切監測慢性溶血性貧血的急性加重。 | 可選建議 | 在G6PD 嚴重缺乏合併慢性非球形紅細胞溶血性貧血(Deficient with CNSHA) 表現型患者中數據不足,但由於潛在的病理生理學賦予慢性溶血性貧血急性加重的高風險,應仔細權衡使用任何藥物的風險與益處。 |
| 可變型(Variable)e | 攜帶一個非缺乏(IV類)等位基因和一個缺乏(I-III類)等位基因者 | B /Bangkok, B/Mediterranean, B/A-, IV/I, IV/II, IV/III | 急性溶血性貧血的低至無風險 | 基於G6PD狀態,在標準劑量下無理由避免低至無風險藥物 | 中等建議 | 由於X 染色體聯鎖嵌合現象(X-linked mosaicism),攜帶多於一個X染色體的個體(例如,女性,克氏綜合症患者)和異型合子(Heterozygous)一個非缺乏(IV類)和一個缺乏(I–III類)等位基因者可能顯示正常或缺乏 表現型。 |
| 無法判定 | 攜帶至少一個等位基因具有功能尚未確定 | Dagua B/Dagua |
急性溶血性貧血的未知風險 | 為確定G6PD狀態,必須測量酶活性。藥物使用應根據基於活性表現型的建議進行指導。 | 中等建議 |
CNSHA:慢性非球形紅細胞溶血性貧血
a WHO分類來自[文章:22293322], 其他細節來自[文章:4963040]。I類等位基因極為罕見;II類和III類等位基因之間的區分不明顯。幾乎所有患者都攜帶II、III或IV類等位基因。
b 由於G6PD 等位基因的數量龐大,除了此處給出的範例外,還可能存在其他基因型;請參閱G6PD 等位基因定義表以獲取更全面的等位基因和G6PD 等位基因功能表以了解其分配的功能(WHO類別)。請注意,一些實驗室使用“B 等位基因”的標示來指示不攜帶已知I-III類變異的等位基因。可參考G6PD頻率表以了解G6PD 等位基因在主要生物地理群體中的頻率。
c 評分方案在指引補充的建議強度部分中描述。
d 此類基因型從未見過,推測極為罕見。
e 由於X 染色體聯鎖嵌合現象(X-linked mosaicism),攜帶一個非缺乏(IV類)和一個缺乏(I-III 等位基因)等位基因的個體(通常為女性)可能顯示正常或缺乏 表現型。因此,很難預測這些個體的表現型(見補充,G6PD異合子)。
Doxorubicin 途徑 (癌細胞), 藥效學
概括
癌細胞示意圖中參與 doxorubicin 作用之候選基因示意圖
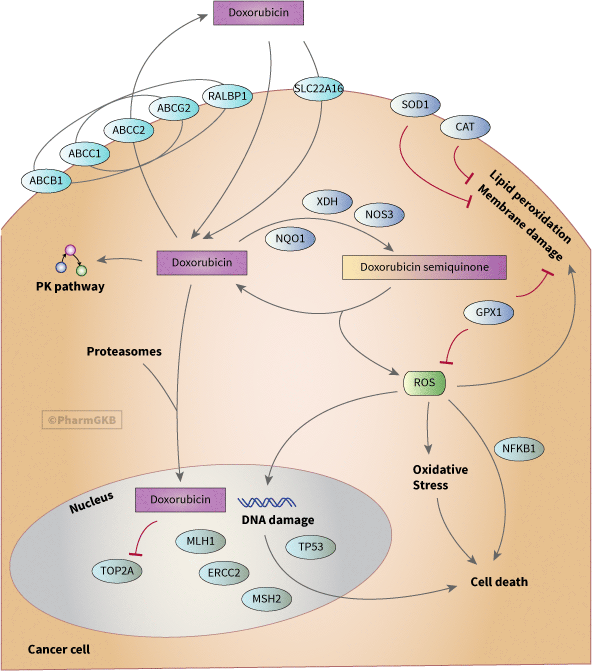
描述
蒽醌類藥物 Doxorubicin (DOX), 是由 Streptomyces peucetius var. caesius [Article:5365804] 開發的化療藥物,於1970年代問世 [Article:17652804],用於治療多種癌症,包括非霍奇金淋巴瘤、霍奇金淋巴瘤、多發性骨髓瘤、肺癌、卵巢癌、胃癌、甲狀腺癌、乳腺癌、肉瘤及小兒癌症 [Articles:17652804, 1462166]。這個 途徑 顯示了 藥效學 在一個風格化的 癌細胞 中,並描繪了候選藥物基因。
已提出幾種機制來解釋 DOX 的抗腫瘤活性 [Article:10075079]。在此我們描述兩個主要機制:一是插入 DNA,導致 DNA 合成的抑制或拓撲異構酶 II (TOP2A) 的中毒;二是自由基的生成,導致 DNA 和細胞膜損傷。我們還展示了一些 藥物動力學(更多細節請參見 Doxorubicin PK 途徑),並描繪了與 癌細胞 細胞系中藥物抗性相關的運輸蛋白。
插入 DNA
蒽醌類藥物已知能在體外插入 DNA,並且存在幾種 DNA 與 DOX 的晶體結構複合物(例如參見 PDB 條目 151D [Article:8142363] 和 1P20 [Article:12717724])。在早期的體外研究中,已顯示 DOX 會導致 DNA 斷裂 [Article:566561],並干擾 DNA 的合成 [Articles:1277199, 1089410]。其他研究顯示,DNA-DOX 的相互作用與拓撲異構酶 II (TOP2A) 的中毒有關 [Articles:2551497, 6093249],但與拓撲異構酶 I [Articles:2164630, 10385686] 無關。CAT 的轉運進入細胞核被認為是通過與蛋白酶體結合來實現的 [Article:11289116]。隨後的 TOP2A 中毒介導的細胞毒性被推測涉及不配對修復基因 MSH2 和 MLH1 [Article:11477562],因為失去 DNA 不配對修復功能會導致對 Doxorubicin 的抗性 [Articles:11477562, 9514047]。
拓撲異構酶 II- 介導的 DNA 損傷隨後導致細胞死亡 [Article:11172690]。 TP53,一個在 DNA- 損傷反應和凋亡中扮演重要角色的基因 [Article:11790556],已被認為與這一 DOX- 的凋亡 途徑 有關。幾項研究顯示,接受蒽醌類藥物治療的患者中 TP53 的上調現象 [Articles:12739000, 10914720],而 ERCC2 和 TP53 已被證明在 途徑 中與 DOX 治療的淋巴母細胞系功能性相互作用 [Article:10467415]。然而,其他研究者對 p53 在 DOX- 介導的凋亡中的實際參與提出了質疑 [Article:11172690]。
自由基的生成
DOX 可以通過幾種氧化還原酶進行單電子還原,形成 DOX- 半醌自由基 [Article:2555273]。這些酶包括存在於肌漿網和線粒體中的線粒體 NADH 脫氫酶: NDUFS2,3,7 EC 1.6.99.3 [Articles:12688675, 2850270, 9618942] 以及細胞質酶 NAD(P)H 脫氫酶 (NQO1) [Article:12688675],黃嘌呤氧化酶 (XDH EC 1.2.3.2) [Articles:12688675, 1911046] 和內皮一氧化氮合酶 (NOS3) [Article:9333325]。DOX- 半醌自由基的再氧化會導致 reactive oxygen species (ROS) 和過氧化氫的形成 [Article:9576481]。 ROS,造成氧化壓力,可以被谷胱甘肽過氧化物酶、CAT酶和超氧化物歧化酶 [Article:12751786]。
一些研究者將 DOX 自由基的形成與細胞毒性相關聯;這些研究將 DOX 細胞的抗性與去活化 ROS 的酶相關聯。DOX 已被證明能通過形成 ROS 和過氧化氫 [Article:12139490] 促進 DOX- 處理的內皮細胞和肌肉細胞的凋亡,這是通過激活 NF-kB (NFKB1, p50) 實現的。然而,激活 NF-kB 阻止了 DOX- 處理的細胞的凋亡 癌細胞 [Article:12139490],這表明細胞毒性和心臟毒性的可能不同機制。這些研究者及其他人認為,自由基形成的作用主要與心臟毒性相關,而非細胞毒性 [Article:10075079],部分原因是使用鐵螯合劑 dexrazoxane,該藥物能結合參與自由基形成的鐵,顯示出心臟保護特性而不影響臨床結果 [Articles:15038979, 9777314, 9193324, 9193323, 18425895]。
抗性
雖然 DOX 是一種有價值的臨床抗腫瘤藥物,但除了心臟毒性問題外,抗性也是限制其效用的問題 [Articles:2982511, 1462166]。抗性的機制被認為特別涉及 ABCB1 (MDR1, Pgp) 和 ABCC1 (MRP1) 以及其他運輸蛋白。
一般而言,ABCB1 通過作為 ATP- 依賴的藥物外排泵來賦予抗性,導致藥物外排增加 [Article:8763334],這是通過改變或增加表達 [Articles:8763334, 9073310]。抑制 ABCB1 會增加 DOX 的細胞毒性 [Articles:1352877, 15788683]。人類 ABCC1,最初從一個 DOX- 選擇的 癌細胞 細胞系中克隆 [Article:1360704],賦予對蒽醌類藥物的抗性。對 DOX- 抗性細胞系的各種研究顯示,通過抑制 ABCB1, ABCC1 和 ABCC2 可以克服抗性 [Articles:12370750, 15164094, 7214365, 1352877, 3180056, 17704753, 11172691, 7954421]。
研究還顯示抗性與其他運輸蛋白的活性之間存在關聯。例如,在一個 DOX- 敏感細胞系中,RALBP1 的活性被顯示為在 DOX 抗性細胞系中高出 2 倍 [Article:12527936]。在一項針對一組肺 癌細胞 細胞系的研究中,證明了 DOX 半醌水平與 ABCC3 和 ABCG2 蛋白水平之間的相關性 [Article:11410522]。在 DOX- 敏感的白血病細胞中,谷胱甘肽轉移酶的活性被發現高於 DOX- 抗性的白血病細胞 [Article:2897875]。
藥物基因體學
大多數有關 DOX 的體內藥物基因組學研究集中於心臟毒性而非療效(詳情請參見 Doxorubicin 心臟毒性藥效學 途徑 的藥物基因組學研究)。在 CYBA (rs4673)、GST1A (rs3957357) 和 NOS3 (rs1799983 和 rs2070744) 的多態性已與對 DOX 的癌症結果相關聯。 CYBA (rs4673), GST1A (rs rs3957357) 與接受 CHOP 治療的擴散性大B細胞淋巴瘤患者的事件無自由生存和結果相關聯,該方案包括 DOX [Article:19448608。在 NOS3 (rs1799983 和 rs2070744]) 中的變異與化療後癌症復發的風險增加相關,該化療包括 DOX [Article:19671875]。
有關 DOX 藥物基因組學的更多細節請參見 基因學標籤。
Doxorubicin 途徑, 藥物動力學
概括
POR的轉運及代謝的圖示表示。
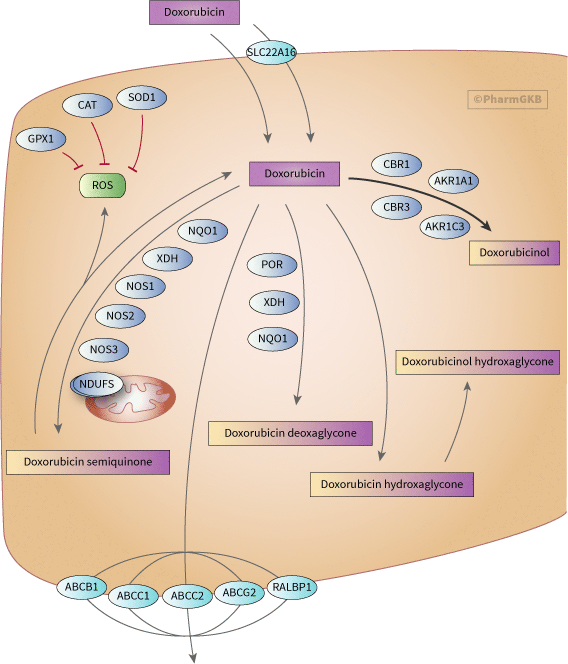
描述
蒽醌類藥物的代謝主要有三條途徑:單電子還原、雙電子還原和去糖苷化。然而,大約50%的DOX以未改變的形式從體內排出[Article:19442138]。
雙電子還原DOX形成次級醇DOX是主要的代謝途徑途徑[Article:19442138]。有幾種酶可以催化這一反應,且它們在不同細胞類型中的平衡不同[Article:18635746]。例如,AKR1A被認為在心臟組織中最為重要,而CBR1則是肝臟中的主要貢獻者[Articles:18635746, 12963485, 19442138]。CBR3也能形成DOX醇[Article:20007405]。AKR1C3的角色尚不明確,一些研究顯示其對DOX的代謝,而另一些則對此提出異議[Articles:18616992, 18635746, 12963485]。
單電子還原DOX是由幾種氧化還原酶催化,形成DOX-半醌自由基[Article:2555273]。這些酶包括存在於肌漿網和線粒體中的線粒體NADH脫氫酶:NDUFS2, NDUFS3, 和NDUFS7 (EC 1.6.99.3) [Articles:12688675, 2850270, 9618942],以及細胞質中的酶NADPH脫氫酶 (NQO1) [Article:12688675],黃嘌呤氧化酶 (XDH) [Articles:12688675],以及一氧化氮合酶 (NOS1, NOS2 和 NOS3) [Articles:9333325, 15054088]。DOX-半醌自由基的再氧化回到DOX會導致reactive oxygen species (ROS)和過氧化氫的形成[Article:9576481]。ROS,造成氧化壓力,可以被谷胱甘肽過氧化物酶 (GPX1)、CAT酶 (CAT) 和超氧化物歧化酶 (SOD1) [Article:12751786]。這一代謝途徑釋放的ROS,而非DOX-半醌,被認為是某些藥物效應和不良心臟毒性的原因。
第三條次要途徑,去糖苷化,約占DOX代謝的1-2%。這可以是還原性形成去氧苷醇,或水解形成羥基苷醇。這一過程的酶及其候選基因尚未被充分表徵[Articles:19442138, 10813659]。在心臟中,未檢測到DOX羥基苷醇;它似乎迅速轉化為DOX醇苷醇[Article:10813659]。在心臟中,NADPH對於苷醇的形成是必需的,這表明NADPH依賴的水解酶和還原酶型苷酸酶負責此過程[Article:10813659]。NADPH-細胞色素P450還原酶 (POR) 在體外被證明能將DOX代謝為DOX 7-去氧苷醇[Articles:6305277, 10860924]。XDH和NQO1也在此過程中被涉及[Article:10860924]。
轉運PORt
幾種轉運蛋白已被證明參與轉運Doxorubicin,包括ABCB1, ABCC1, ABCC2, ABCG2, RALBP1 (外POR運) 和 SLC22A16 (內POR運) [Articles:12370750, 15164094, 7214365, 1352877, 3180056, 17704753, 11172691, 7954421, 12527936, 11410522, 17559346]。轉運蛋白的遺傳變異與藥物抗性有關(詳情請參見Doxorubicin癌症藥物動力學途徑)。
藥物基因體學 (PGx)
長期以來已知DOX和DOX醇的藥物動力學參數存在相當大的個體間變異[Article:2265458]。然而,遺傳變異對DOX的代謝和反應,包括心臟毒性的影響,最近才開始受到研究。歷史上,只有累積的蒽醌類劑量被確認為DOX-引起心臟毒性的顯著風險因素[Article:6651020]。
Doxorubicin 途徑 (心肌細胞), 藥效學
概括
涉及Doxorubicin不良反應的候選基因在風格化心肌細胞中的表現。

描述
抗腫瘤藥物 Doxorubicin (DOX) 的主要不良反應包括急性和慢性心臟毒性/心臟肌肉病變。DOX 的使用受到累積性、劑量相關的進行性心肌損傷的限制,這可能導致充血性心力衰竭 (CHF) [Article:12767102]。由 DOX 引起的心臟毒性似乎是一個多因素過程,許多機制已被提出和研究 [Article:15169927]。DOX 的治療效果機制被認為與其心臟毒性機制不同。以下描述了兩種心臟毒性機制:自由基對心肌細胞造成的氧化壓力,涉及 DOX 和 DOX 代謝物,這些過程涉及鐵 [Articles:15038979, 15038980, 9777314] 以及該藥物對線粒體生物能量學的有害影響 [Articles:17652813, 16278810]。
DOX, ROS 和鐵
DOX 代謝為 doxorubicinol (DOXol),這一代謝物已被認為與心臟毒性有關。據報導,該代謝過程是通過醛酮還原酶 (AKR) 1C3 [Articles:18616992, 18635746],醛還原酶 (AKR1A1) [Article:12963485],以及碳基還原酶 CBR1 [Article:18635746] 和 CBR3 [Article:20007405]。然而,其他研究報導 AKR1C3 並未將 DOX 代謝為 DOXol [Article:12963485]。DOXol 似乎也會擾亂與 aconitase- 鐵調節蛋白-1 (ACO1) 相關的鐵穩態過程,可能導致心臟毒性 [Article:9576481]。dexrazoxane,一種鐵螯合劑,在臨床研究中顯示出明顯的心臟保護特性,當在 DOX 之前或與之同時給予時 [Articles:15038979, 9777314, 9193324, 9193323, 18425895]。此外,糖苷 DOX 鍵可以被切割以產生 7-deoxydoxorubicinone,再次產生 ROS 和過氧化氫 [Article:15169927]。而 DOX 本身也已被證明能與鐵形成複合物,產生自由基 [Article:3533644]。除了 ROS,reactive nitrogen species (RNS) 也與 DOX 的心臟毒性有關 [Article:15054088],這是通過干擾一氧化氮 (NO) 的調節。接受 DOX 治療的啮齿類動物顯示出心臟功能障礙,這是由於一氧化氮 (NO) 和超氧化物 (O2-) 的快速反應生成過氧亞硝酸鹽 [Articles:10871338, 12591762],這一機制涉及一氧化氮合成酶 (NOS1, NOS2, NOS3) [Articles:10871338, 12591762]。
心肌細胞可能比其他組織更易受損的原因之一是心臟相比於肝臟,對自由基攻擊的酶防禦濃度 (CAT, SOD1) 明顯較低,並且在暴露於 Doxorubicin 後,心臟的谷胱甘肽過氧化物酶活性(另一種抗氧化酶)會受到藥物相關的抑制 [Article:7350193](大鼠),[Article:2496064](大鼠)。DOX 已被證明會降低 SOD1 的蛋白質水平和活性 [Article:12030376]。
請注意,DOX、鐵和 ROS 的關聯並非沒有爭議 [Article:19307704]。由於其他鐵螯合劑,如去鐵酮,未能發揮 dexrazoxane 的保護作用 [Article:14642395],因此提出的另一種機制是通過與 TOP2B 的相互作用,防止 DOX 引起 DNA 的損傷 [Articles:17875725, 19442138]。
線粒體能量學
最近有研究提出,心臟毒性的主要機制是線粒體功能障礙 [Articles:16278810, 17652813],可能是通過干擾 calcium 的穩態 [Article:17652813](大鼠),[Article:12498738](大鼠)。線粒體在心臟組織中豐富(佔細胞體積的高達 35%),依賴 ATP 來維持收縮功能,干擾這一功能可能會導致心臟擇期 毒性 [Article:17652813]。DOX 和其他蒽環類藥物已被證明在線粒體電子傳遞鏈的複合體 I 被還原為半醌形式並形成自由基 [Articles:3005279, 3456345]。DOX 的苷元已被證明在內線粒體膜中積累,干擾呼吸鏈的電子載體,並可能導致細胞色素 c (CYCS) 的釋放 [Article:12894526],而來自與線粒體複合體 I 相互作用的 DOX 苷元半醌被發現形成羥基自由基,造成氧化壓力 [Article:9618942]。5-亞氨基多烯醇,這是一種結構相關的類似物,具有較低的心臟毒性,並不釋放氧自由基,且對線粒體呼吸沒有影響 [Articles:3005279, 3456345]。此外,DOX 已被證明在體內大鼠研究中抑制孤立心臟線粒體中 calcium 的淨積累 [Article:7527602]。DOXol,DOX 的代謝物,已被證明干擾肌漿網的 calcium 泵 (ATP2A2)、肌膜的 Na+ /K+ 泵 (RYR2) 和線粒體的質子泵 (EC 3.6.1.34) [Articles:2897122, 19442138]。
藥物基因體學
歷史上,只有累積的蒽環類劑量被確認為 DOX- 引起的心臟毒性的顯著風險因素 [Article:6651020。在 ABCC1 (rs45511401), ABCC2 (rs17222723, rs8187710), CAT (rs10836235), CBR3 (rs1056892), CYBA (rs4673), NCF4 (rs1883112) 和 RAC2 (rs13058338]) 的變異與體內心臟毒性相關 [Articles:16330681, 19448608, 18457324, 19863340]。
Wojnowski 等人在對 1697 名患者的 82 個基因 SNP 進行研究中,發現其中 3.2% 的患者發展為急性或慢性 DOX- 引起的心臟毒性,並發現心臟毒性與 NAD(P)H 氧化酶複合體 (CYBA, NCF4 和 RAC2) 的多態性之間存在 5 個顯著關聯,以及 DOX 運輸蛋白 [Article:16330681]。與此一致的是,與野生型小鼠相比,缺乏 NAD(P)H 氧化酶活性的老鼠對慢性 Doxorubicin 治療具有抵抗力 [Article:16330681。ROSsi 等人最近在接受 DOX- 含化療的淋巴瘤患者中進行的研究顯示,CYBA (rs4673) 和 NCF4 (rs1883112]) 與毒性相關 [Article:19448608]。
Blanco 等人建議 CBR3 Val244Met 多態性 (rs1056892) 可能會影響兒童癌症倖存者中與蒽環類相關的 CHF 風險,儘管承認需要更大規模的研究 [Article:18457324]。這一變異也與亞洲乳腺癌患者腫瘤組織中較高的 doxorubicinol AUC 和較高的 CBR3 表達相關 [Article:18551042]。然而,對於這一變異的體外研究結果存在一定的矛盾,有些顯示變異蛋白在以 DOX 作為底物時活性降低 [Articles:18457324, 20007405],而其他則顯示在以美托洛爾作為底物時活性增加 [Article:15537833]。
其他研究已檢查了各種變異和 表現型 的影響,包括體內和體外研究,詳情請參見遺傳學標籤。大多數 DOX PGx 研究仍需驗證。