CPIC 指南註解:vortioxetine 與 CYP2D6 基因
摘要
CPIC 對於 vortioxetine 的劑量指引建議,對於 CYP2D6 超快速代謝型(Ultrarapid metabolizer),選擇不主要由 CYP2D6 代謝的替代藥物。對於 弱代謝型(Poor metabolizer),起始劑量為原劑量的 50%,並逐漸增加至建議的最大劑量 10 mg,或考慮選擇一種臨床上適當的替代抗抑鬱藥,其不主要由 CYP2D6 代謝。
為特定註釋指定基因型或表現型
註釋
此註釋基於CPIC® 指南,針對CYP2D6、CYP2C19、CYP2B6、SLC6A4和HTR2A基因型與血清素再攝取抑制劑抗抑鬱藥。
2023年2月
-
CPIC® 指南的作者針對CYP2D6、CYP2C19、CYP2B6、SLC6A4和HTR2A基因型與血清素再攝取抑制劑抗抑鬱藥,評估了可用的證據以提供治療劑量對於venlafaxine和CYP2D6代謝者表現型的建議。
-
這些指南適用於:
- 成人患者
- 兒科考量:「Citalopram、escitalopram和sertraline在兒童中有最多的藥物基因體學數據支持潛在的基因型指導處方變更。基於這些證據,這些藥物的建議與兒科患者相關,並與此人群可用的較小藥代動力學研究一致。」.....「其他建議對兒科患者的普遍性需要確立。因此,治療兒童和青少年的臨床醫師應在考慮這些藥物在青少年中的獨特且更有限的證據基礎,以及兒科特有的耐受性差異(例如,激活)和疾病特定的反應軌跡時,確定其對年輕患者的適用性。由於CYP2D6、CYP2C19和CYP2B6的活性在幼兒期達到成人水平,因此可能適合將與CYP2D6、CYP2C19和CYP2B6相關的抗抑鬱藥的基因型指導建議推廣至青少年或可能更年幼的兒童,並進行密切監測。」
-
指南摘錄:
- 「在多項研究中,CYP2D6 UMs的paroxetine(31-34)和vortioxetine(35)的血漿濃度低或不可檢測,與NMs(31-34)相比。那些血漿濃度不可檢測或低的人臨床效益的可能性較低,儘管paroxetine的最低有效治療濃度尚未明確定義(36)。由於paroxetine和vortioxetine的藥物暴露降低導致臨床效益的可能性降低,應考慮選擇不主要由CYP2D6代謝的替代抗抑鬱藥。」
- 「當給予相似劑量時,CYP2D6 PMs的paroxetine、fluvoxamine、venlafaxine和vortioxetine的藥物暴露或母體與代謝物比率顯著高於NMs(表S1)。增加的藥物暴露增加了劑量/濃度依賴性副作用的風險。為了可能預防不良反應,基於表現型組之間藥代動力學參數差異的劑量推算建議paroxetine(表2a)和vortioxetine(表2d)減少50%劑量,fluvoxamine減少30%劑量是合理的(27)。」
- 「FDA的藥物基因體學關聯表列出venlafaxine和vortioxetine為需要在CYP2D6 PMs中調整劑量的藥物。」
-
下載並閱讀:
表1:基於CYP2D6 表現型的vortioxetine劑量建議
改編自指南的表1和2d。
| 表現型 | 活性分數 範圍 |
活性分數 | 範例 | 影響 | 治療 建議 |
建議的 分類a |
考量 |
|---|---|---|---|---|---|---|---|
| CYP2D6 超快速代謝型(Ultrarapid metabolizer) | >2.25 | >2.25 | *1/*1xN, *1/*2xN, *2/*2xNc | 與CYP2D6 正常代謝型(Normal metabolizer)s相比,vortioxetine代謝為不活性化合物的代謝增加。較低的血漿濃度降低臨床效益的可能性。 | 選擇不主要由CYP2D6代謝的替代藥物。如果需要使用vortioxetine,則以標準起始劑量開始治療,並根據療效和副作用進行劑量調整。為達到療效,可能需要將目標維持劑量增加50%或更多。 | 可選建議 | 藥物交互作用和其他患者特徵(例如,年齡、腎功能、肝功能)應在選擇替代療法時考慮。 |
| CYP2D6 正常代謝型(Normal metabolizer) | 1.25 <= x <= 2.25 | 1.25 1.5 1.75 2.0 2.25 |
*1/*10 *1/*41, *1/*9 *10/*41x3 *1/*1, *1/*2 *2x2/*10 |
正常代謝。 | 以建議的起始劑量開始治療。 | 強烈建議 | |
| CYP2D6 中間代謝型(Intermediate metabolizer) | 0 < x < 1.25 | 0.25 0.5 0.75 1.0 |
*4/*10 *4/*41, *10/*10 *10/*41 *41/*41, *1/*5 |
與CYP2D6 正常代謝型(Normal metabolizer)s相比,vortioxetine代謝為較不活性化合物的代謝減少。較高的血漿濃度可能增加副作用的可能性 | 以建議的起始劑量開始治療。 | 中等建議 | |
| CYP2D6 弱代謝型(Poor metabolizer) | 0 | 0 | *3/*4, *4/*4, *5/*5, *5/*6 | 與CYP2D6 正常代謝型(Normal metabolizer)s相比,vortioxetine代謝為不活性化合物的代謝大幅減少。較高的血漿濃度可能增加副作用的可能性。 | 以起始劑量的50%(例如,5 mg)開始治療,並調整至最大建議劑量10 mg,或考慮選擇不主要由CYP2D6代謝的臨床適當替代抗抑鬱藥。 | 中等建議 | 藥物交互作用和其他患者特徵(例如,年齡、腎功能、肝功能)應在調整劑量或選擇替代療法時考慮。 |
| CYP2D6 無法判定 | n/a | 攜帶一個或兩個未知或功能尚未確定 等位基因s的個體 | *1/*22, *1/*25, *22/*25 | 無建議 | 無建議 |
a 評分方案詳見補充材料。
vortioxetine 途徑, 藥物動力學
概括
候選基因在 vortioxetine 代謝中的表現。
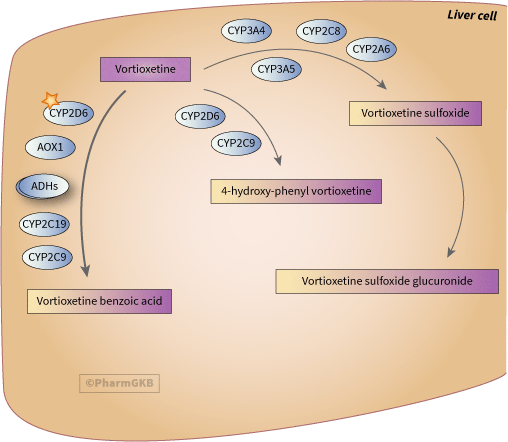
描述
背景
vortioxetine 是一種雙重血清素和去甲腎上腺素再攝取抑制劑,已獲得批准用於治療成人的重度抑鬱症。尚未評估其在兒童中的使用。FDA 仿單 對於 vortioxetine 有黑框警告,指出青少年、兒童和年輕人存在自殺意念的風險。關於 FDA 仿單 的藥物基因組學信息提供了已知 CYP2D6 弱代謝型(Poor metabolizer) 的建議最大劑量以及與 CYP2D6 抑制劑聯合使用時的劑量減少建議。
代謝
vortioxetine 經過廣泛的代謝,通過氧化和隨後的葡萄糖醛酸結合,主要代謝物為臨床上不活躍的 vortioxetine benzoic acid [Articles:24766668, 22448783, 22496396]。幾種酶能夠在體外代謝 vortioxetine,包括 CYP2D6、CYP3A4/5、CYP2C9、CYP2C19、CYP2A6、CYP2C8 和 CYP2B6,但在體內主要的酶是 CYP2D6 [Articles:24766668, 22448783, 22496396]。在 CYP2D6 弱代謝型(Poor metabolizer) 中,vortioxetine 的清除率約為在 CYP2D6 廣泛代謝型(Extensive metabolizer) 中觀察到的50% [Article:24766668]。苯甲酸代謝物的形成分為兩個步驟,第一步是主要由 CYP2D6 生成苯基醇,但 CYP2C9 和 CYP2C19 也可能具備此能力 [Article:22496396]。第二步是形成苯甲酸代謝物,主要的酶很可能是醇脫氫酶和醛脫氫酶,CYP2D6 是唯一在體外能夠進行此步驟的 CYP [Article:22496396]。
運輸
文獻中關於 vortioxetine 的運輸體證據有限。vortioxetine 是小鼠 ABCB1 運輸體的底物 [Article:30476727],儘管作者並未測試人類的 ABCB1。